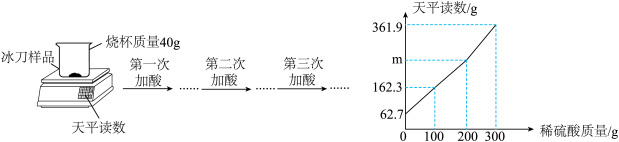
高速钢(一种铁合金)是制造冰鞋冰刀的重要材料。取一定质量的冰刀样品研成粉末后放于烧杯中,分3次每次加入100g溶质质量分数相同的稀硫酸,实验过程及每次充分反应后天平读数如图所示。(假设合金中只有铁和稀硫酸反应)
(1) =
=________ 。
(2)所取冰刀样品中铁的质量。
(1)
 =
=(2)所取冰刀样品中铁的质量。
更新时间:2023/07/23 23:49:21
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】某校化学兴趣小组的同学为测定当地石灰石中碳酸钙的质量分数(杂质不与酸反应),做了如下实验,向6.0g石灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体1.11L(该条件下二氧化碳气体的密度为1.977g/L)。试计算:
(1)反应生成二氧化碳的质量为_________g;(精确到0.1g)
(2)石灰石样品中碳酸钙的质量分数为多少_____?(写出计算过程,结果精确至0.1%)
(3)若要计算恰好完全反应时所消耗稀盐酸的质量,题中还缺少的一个数据是____。
(1)反应生成二氧化碳的质量为_________g;(精确到0.1g)
(2)石灰石样品中碳酸钙的质量分数为多少_____?(写出计算过程,结果精确至0.1%)
(3)若要计算恰好完全反应时所消耗稀盐酸的质量,题中还缺少的一个数据是____。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将适量二氧化碳通入100g氢氧化钠溶液中。恰好完全反应后,得到108.8g碳酸钠溶液。请计算:(反应方程式: )
)
(1)参加反应的二氧化碳的质量为___________ g。
(2)生成碳酸钠的质量。
 )
)(1)参加反应的二氧化碳的质量为
(2)生成碳酸钠的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】同学们用加热氯酸钾和二氧化锰的方法制取氧气,实验过程中的有关数据如图所示。请回答下列问题:_____ (填“a”、“b”或“c”)点时,氯酸钾恰好完全反应。
(2)计算混合物中的二氧化锰的质量。
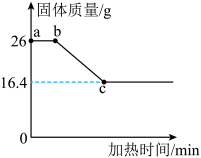
(2)计算混合物中的二氧化锰的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】煤是一种化石燃料,用煤作燃料生成的SO2气体会造成环境污染。有一种煤每燃烧1 t就会释放出53.3 kg SO2。如果将产生的SO2用熟石灰来完全吸收,其反应的化学方程式为:SO2+Ca(OH)2====CaSO3+H2O,那么燃烧5 t这种煤产生的SO2在理论上需用多少千克的Ca(OH)2来吸收?(计算结果取整数)__________
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验室加热氯酸钾和二氧化锰的混合物 6.5g 至完全反应,称得剩余固体的质量为 4.58g。求:
(1)反应生成的氧气的质量
(2)混合物中二氧化锰的质量。
(1)反应生成的氧气的质量
(2)混合物中二氧化锰的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】利用生活中的废弃材料来做家庭小实验,其乐无穷!小美同学设计了如图所示的装置来探究二氧化碳的制取和性质。(a,d处为浸有紫色石蕊溶液的湿润棉花,b、c处为用紫色石蕊溶液浸过的干燥棉花。垂直固定玻璃管的装置未画出)
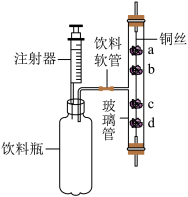
(1)玻璃管内观察到的现象为_________。
(2)用下面装置作为实验室制取二氧化碳的发生装置,其优点是_________。
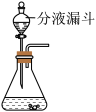
(3)小美向饮料瓶中加入某石灰石样品10g(杂质不反应),逐滴加入稀盐酸至恰好不再产生气体时,共消耗50g稀盐酸,测得反应后饮料瓶中物质总质量为57.8g。试求所用稀盐酸的溶质质量分数。

(1)玻璃管内观察到的现象为_________。
(2)用下面装置作为实验室制取二氧化碳的发生装置,其优点是_________。

(3)小美向饮料瓶中加入某石灰石样品10g(杂质不反应),逐滴加入稀盐酸至恰好不再产生气体时,共消耗50g稀盐酸,测得反应后饮料瓶中物质总质量为57.8g。试求所用稀盐酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定某鸡蛋壳中碳酸钙的含量,小明同学将鸡蛋壳洗净、干燥并捣碎后进行了如图所示的实验(假设鸡蛋壳中除碳酸钙外的其他物质不含钙元素,不与稀盐酸反应,也不溶于水),请计算:

(1)产生二氧化碳气体 g。
(2)该鸡蛋壳中碳酸钙的质量分数。(写出计算过程)
(3)该鸡蛋壳样品中钙元素的质量分数是 。

(1)产生二氧化碳气体 g。
(2)该鸡蛋壳中碳酸钙的质量分数。(写出计算过程)
(3)该鸡蛋壳样品中钙元素的质量分数是 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】小刚在实验室发现一瓶存放多年的氢氧化钙,为检验其变质情况,他取该氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,然后逐滴滴加14.6%的稀盐酸,加入稀盐酸的质量与锥形瓶中物质的质量关系如图所示。
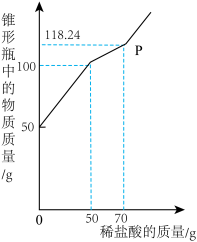
(1)氢氧化钙变质的原因是____________(用化学方程式表示)。
(2)与氢氧化钙反应的稀盐酸的质量为_________g。
(3)该样品中未变质的氢氧化钙的质量分数是多少_________(写出计算过程,结果精确到0.1%)。

(1)氢氧化钙变质的原因是____________(用化学方程式表示)。
(2)与氢氧化钙反应的稀盐酸的质量为_________g。
(3)该样品中未变质的氢氧化钙的质量分数是多少_________(写出计算过程,结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】某化学研究性学习小组为测定市场出售的食醋的总酸量(国家规定食醋中总酸量为3.5 g/100 mL~5 g/100 mL),拟配制一定质量分数的氢氧化钠溶液,然后进行测定。
请你参与该小组的实验研究,并回答相关问题。
(1)配制100 g质量分数为5%的氢氧化钠溶液,需要水多少mL。(水的密度为1 g/cm3)
(2)若食醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的化学方程式为CH3COOH+NaOH=CH3COONa+H2O。现有食醋500 mL,甲同学从中取出10 mL,加入5%的氢氧化钠溶液4.8 g,恰好完全反应。请通过计算判断该食醋是否合格。(写出计算过程)
请你参与该小组的实验研究,并回答相关问题。
(1)配制100 g质量分数为5%的氢氧化钠溶液,需要水多少mL。(水的密度为1 g/cm3)
(2)若食醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的化学方程式为CH3COOH+NaOH=CH3COONa+H2O。现有食醋500 mL,甲同学从中取出10 mL,加入5%的氢氧化钠溶液4.8 g,恰好完全反应。请通过计算判断该食醋是否合格。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】铜锌合金外观形似黄金,某化学兴趣小组为检测合金的成分,进行了如图所示的实验。
(1)生成氢气的质量为______ g。
(2)计算合金中锌的质量分数。(写出计算过程,结果精确到1%)

(1)生成氢气的质量为
(2)计算合金中锌的质量分数。(写出计算过程,结果精确到1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
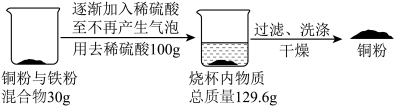
【推荐2】学习小组同学利用下图实验,回收实验室废弃的铜粉与铁粉混合物中的铜粉。_____ g。
(2)计算上述实验回收铜粉的质量。(忽略回收过程中铜粉的损失)
(3)上述实验所用稀硫酸的溶质质量分数_____ (填“可能”或“不可能”)是15%。
(2)计算上述实验回收铜粉的质量。(忽略回收过程中铜粉的损失)
(3)上述实验所用稀硫酸的溶质质量分数
您最近一年使用:0次



