某化学研究性学习小组为测定市场出售的食醋的总酸量(国家规定食醋中总酸量为3.5 g/100 mL~5 g/100 mL),拟配制一定质量分数的氢氧化钠溶液,然后进行测定。
请你参与该小组的实验研究,并回答相关问题。
(1)配制100 g质量分数为5%的氢氧化钠溶液,需要水多少mL。(水的密度为1 g/cm3)
(2)若食醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的化学方程式为CH3COOH+NaOH=CH3COONa+H2O。现有食醋500 mL,甲同学从中取出10 mL,加入5%的氢氧化钠溶液4.8 g,恰好完全反应。请通过计算判断该食醋是否合格。(写出计算过程)
请你参与该小组的实验研究,并回答相关问题。
(1)配制100 g质量分数为5%的氢氧化钠溶液,需要水多少mL。(水的密度为1 g/cm3)
(2)若食醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的化学方程式为CH3COOH+NaOH=CH3COONa+H2O。现有食醋500 mL,甲同学从中取出10 mL,加入5%的氢氧化钠溶液4.8 g,恰好完全反应。请通过计算判断该食醋是否合格。(写出计算过程)
2012九年级·全国·专题练习 查看更多[5]
更新时间:2017-12-05 20:36:55
|
相似题推荐
【推荐1】某黄铜样品的成分是铜、锌和4%的杂质(杂质中不含铜和锌,杂质不溶于水,且不与该题中其他物质发生反应),某化学小组为测定其中铜的质量分数进行如下实验:

请计算:
(1)该黄铜样品中铜的质量分数为_______ 。
(2)所得溶液甲的溶质质量分数(计算结果保留到0.1%)。

请计算:
(1)该黄铜样品中铜的质量分数为
(2)所得溶液甲的溶质质量分数(计算结果保留到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组利用废铁屑和稀盐酸进行如下实验请计算:

(1)生成氢气的总质量为_______ g。
(2)废铁屑中铁的质量分数_____ 。(铁屑中杂质不与稀盐酸反应,反应中水蒸气的挥发忽略不计。)

(1)生成氢气的总质量为
(2)废铁屑中铁的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】小明用表面被氧化的镁条和稀硫酸反应的实验来测定稀硫酸的溶质质量分数。实验中,他绘制了生成氢气的质量与所用稀硫酸质量的关系如图。请读图,计算:
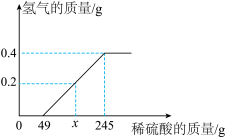
(1)x =____g。
(2)该稀硫酸的溶质质量分数。

(1)x =____g。
(2)该稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为了配制50g 5%的氯化钠溶液,需进行如下操作:
①计算;
②用托盘天平称量_________ g 氯化钠;
③用______________ (填“10mL”或“50mL”)量筒量取________________ mL水;
④将两者置于烧杯中,用玻璃棒搅拌。(写出计算过程)
①计算;
②用托盘天平称量
③用
④将两者置于烧杯中,用玻璃棒搅拌。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某医生为病人输液时,使用的是0.9%的生理盐水,若某病人输液1000g,则进入病人体内的NaCl的质量为多少克?若用50g溶质质量分数为18%的NaCl溶液配制0.9%的生理盐水,需要水的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】兴趣小组同学要测定一瓶失去标签的稀硫酸的溶质质量分数。取10g稀硫酸样品,将10%的氢氧化钠溶液逐滴加入到样品中,不断搅拌,测得溶液pH随滴入氢氧化钠溶液量的变化情况如图所示。
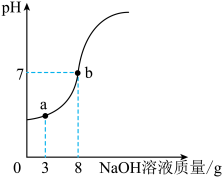
请分析并计算下列问题:
(1)该反应的实质是___________ 。
(2)当pH=7时,消耗氢氧化钠的质量是___________ 。
(3)计算该稀硫酸的溶质质量分数。

请分析并计算下列问题:
(1)该反应的实质是
(2)当pH=7时,消耗氢氧化钠的质量是
(3)计算该稀硫酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定某石灰石样品中碳酸钙的含量,小丽进行实验,测得相关数据如下图所示:

(1)完全反应生成二氧化碳的质量为_____。
(2)该石灰石样品中碳酸钙的质量分数是多少?
(3)反应后溶质质量分数是多少?

(1)完全反应生成二氧化碳的质量为_____。
(2)该石灰石样品中碳酸钙的质量分数是多少?
(3)反应后溶质质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】常温下,一锥形瓶中盛有20g溶质质量分数为4%的氢氧化钠溶液,再逐滴滴加溶质质量分数为3.65%的稀盐酸,用pH传感器测得溶液的pH与加入稀盐酸的关系曲线如图。请回答问题:_______ g。
(2)图中a点对应的溶液中溶质的化学式是________ 。
(3)pH=7时,此时消耗3.65%稀盐酸的质量是多少________ ?(写出计算过程)。
(4)若改用溶质质量分数为7.3%的稀盐酸进行本实验,pH传感器测得的曲线可能经过_______ (填“甲”“乙”或“丙”)点。

(2)图中a点对应的溶液中溶质的化学式是
(3)pH=7时,此时消耗3.65%稀盐酸的质量是多少
(4)若改用溶质质量分数为7.3%的稀盐酸进行本实验,pH传感器测得的曲线可能经过
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某工厂化验室常用10%的氢氧化钠溶液测定工业废水中硫酸的含量。
(1)若配制10%的氢氧化钠溶液150 g,需称取NaOH的质量是________ g。
(2)取该氢氧化钠溶液40 g恰好能将100 g废水中的H2SO4中和,求废水中硫酸的质量分数。
(1)若配制10%的氢氧化钠溶液150 g,需称取NaOH的质量是
(2)取该氢氧化钠溶液40 g恰好能将100 g废水中的H2SO4中和,求废水中硫酸的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室中有一瓶标签被腐蚀的盐酸,小丽为了测定溶液中溶质的质量分数,在烧杯中配制了 10g 8%的 NaOH 溶液,然后往烧杯中滴加该盐酸。反应过程中溶液的 pH 与滴入盐酸的质量关系如图所示。请回答下列问题:
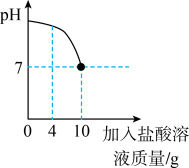
(1)配制了 10g 8%的 NaOH 溶液,需要水的质量为______ ;
(2)计算该盐酸的溶质质量分数;(写出计算过程)
(3)当滴入 4g 盐酸时,烧杯内溶液中钠元素的质量为______ g。

(1)配制了 10g 8%的 NaOH 溶液,需要水的质量为
(2)计算该盐酸的溶质质量分数;(写出计算过程)
(3)当滴入 4g 盐酸时,烧杯内溶液中钠元素的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】在研究“酸与碱之间发生的反应”过程中,取一洁净的锥形瓶,往其中加入25克氢氧化钠溶液,然后逐滴滴入质量分数为7.3%的稀盐酸。
(1)为了获取酸能与碱反应的证据,滴加稀盐酸前,锥形瓶中还需加入的是_____ 。
(2)酸与碱之间反应的实质是_____ 。
(3)滴加稀盐酸至恰好完全反应,锥形瓶及溶液总质量随加入稀盐酸质量的变化关系如图所示。
①a的值是_____ 。
②求反应后溶液中溶质的质量分数_____ 。
(1)为了获取酸能与碱反应的证据,滴加稀盐酸前,锥形瓶中还需加入的是
(2)酸与碱之间反应的实质是
(3)滴加稀盐酸至恰好完全反应,锥形瓶及溶液总质量随加入稀盐酸质量的变化关系如图所示。
①a的值是
②求反应后溶液中溶质的质量分数

您最近一年使用:0次



