溶液在工农业生产和科学研究中具有广泛的用途。请依据题意回答下列问题。
【资料】 和
和 两种物质在不同温度时的溶解度
两种物质在不同温度时的溶解度
(1)生活在盐湖、碱湖附近的人们传承下来的劳动经验是“夏天晒盐,冬天捞碱”。
① 俗称苏打或
俗称苏打或______ 。分析表中数据,冬天更适合“捞碱”的原因是:冬季温度降低, 的溶解度随温度的降低而
的溶解度随温度的降低而______ ,有利于 的析出。
的析出。
②夏天“晒盐”,当有大量盐析出后,所得溶液为该温度下 的
的______ (填“饱和”或“不饱和”)溶液。
(2)在实验室进行粗盐提纯时,使用蒸发皿蒸发过程中,有时会出现液滴飞溅现象,导致该现象的原因可能是______ (答一点即可)。
(3)在实验室用质量分数为 的
的 溶液(密度约为
溶液(密度约为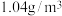 )配制
)配制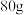 质量分数为
质量分数为 的
的 溶液。
溶液。
①计算所需质量分数为 的
的 溶液的质量为
溶液的质量为______ g。
②在配制该溶液的过程中,下列实验仪器不需要选用的是______ (填字母序号)。______ (填“ ”或“
”或“ ”)的量筒量取所需水(密度约为
”)的量筒量取所需水(密度约为 )的体积。
)的体积。
【资料】
 和
和 两种物质在不同温度时的溶解度
两种物质在不同温度时的溶解度温度/ | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g |  | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
 | 7.1 | 12.2 | 21.8 | 39.7 | 53.2 | |
①
 俗称苏打或
俗称苏打或 的溶解度随温度的降低而
的溶解度随温度的降低而 的析出。
的析出。②夏天“晒盐”,当有大量盐析出后,所得溶液为该温度下
 的
的(2)在实验室进行粗盐提纯时,使用蒸发皿蒸发过程中,有时会出现液滴飞溅现象,导致该现象的原因可能是
(3)在实验室用质量分数为
 的
的 溶液(密度约为
溶液(密度约为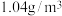 )配制
)配制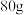 质量分数为
质量分数为 的
的 溶液。
溶液。①计算所需质量分数为
 的
的 溶液的质量为
溶液的质量为②在配制该溶液的过程中,下列实验仪器不需要选用的是
A.量筒 B.玻璃棒
B.玻璃棒
C.烧杯 D.天平
D.天平
 ”或“
”或“ ”)的量筒量取所需水(密度约为
”)的量筒量取所需水(密度约为 )的体积。
)的体积。
2023·辽宁丹东·中考真题 查看更多[7]
2023年辽宁省丹东市中考化学真题(已下线)专题12 溶液(第03期)-学易金卷:2023年中考化学真题分项汇编(全国通用)2024口袋书系列-题型专练-专题8化学实验-提高练习(已下线)重难点08 酸碱盐-2024年中考化学【热点·重点·难点】专练(全国通用)(已下线)专题03 ?教材基础实验(10大题型)-2024年中考化学二轮热点题型归纳与变式演练(辽宁专用)(已下线)专题09 推断题、工业流程题、溶解度曲线题-2024年中考化学二轮热点题型归纳与变式演练(辽宁专用)(已下线)02 押辽宁卷第6-10题 燃烧和灭火、反应类型、化学方程式、实验基本操作、化学式及计算、溶解度曲线等-备战2024年中考化学临考题号押题(辽宁卷)
更新时间:2023-08-02 22:41:32
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】A、B、C三种物质的溶解度曲线如下图所示,请回答下列问题。

(1)N点对应的是在t2℃时物质A的______ (填 “饱和”或“不饱溶和”)溶液。
(2)加热某温度下物质C的饱和溶液,出现浑浊现象,其原因是______ 。
(3)|除去物质A中混有的少量物质B,步骤是加水溶解、蒸发浓缩、______ 、过滤、洗涤、干燥。

(1)N点对应的是在t2℃时物质A的
(2)加热某温度下物质C的饱和溶液,出现浑浊现象,其原因是
(3)|除去物质A中混有的少量物质B,步骤是加水溶解、蒸发浓缩、
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】甲、乙、丙三种物质的溶解度曲线如图所示,请回答。

(1)气体的溶解度随温度变化的趋势与_____ (填“甲”、“乙”或“丙”)相似。
(2)t3℃时,将40g甲物质加到50g水中充分溶解后,所得溶液中溶质与溶剂的质量比是______ 。
(3)若甲中含有少量乙,提纯甲的方法是_______ 。
(4)将t3℃时等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,对所得溶液的分析正确的是_______(填字母序号)。

(1)气体的溶解度随温度变化的趋势与
(2)t3℃时,将40g甲物质加到50g水中充分溶解后,所得溶液中溶质与溶剂的质量比是
(3)若甲中含有少量乙,提纯甲的方法是
(4)将t3℃时等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,对所得溶液的分析正确的是_______(填字母序号)。
| A.溶解度:乙>甲=丙 | B.溶剂质量:丙>乙>甲 |
| C.溶液质量:乙>甲>丙 | D.溶质质量分数:乙>甲>丙 |
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
名校
解题方法
【推荐1】硫酸亚锡(SnSO4)广泛应用于电镀工业。该物质易与氧气反应而变质。实验室模拟工业上制取SnSO4的一种实验方案如下。
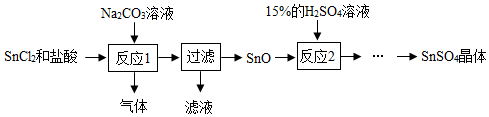
(1)SnCl2由Sn与盐酸反应制得,同时生成氢气,该反应的化学方程式为_____ 。
(2)过滤所得滤液中的溶质为_____ (填化学式)。
(3)用已知质量分数和密度的浓硫酸配制质量分数为15%的稀硫酸,所需玻璃仪器有烧杯、玻璃棒、胶头滴管和_____ 。稀释浓硫酸的正确操作为 _____ 。
(4)反应2属于基本反应类型中的_____ 反应。从反应2所得溶液中获得SnSO4晶体的部分操作须在隔绝空气条件下进行的原因是 _____ 。

(1)SnCl2由Sn与盐酸反应制得,同时生成氢气,该反应的化学方程式为
(2)过滤所得滤液中的溶质为
(3)用已知质量分数和密度的浓硫酸配制质量分数为15%的稀硫酸,所需玻璃仪器有烧杯、玻璃棒、胶头滴管和
(4)反应2属于基本反应类型中的
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】实验室里有密度为1.84g/cm3的溶质质量分数为98%的浓硫酸,欲用来配制溶质质量分数为9.2%的稀硫酸196g;然后用这种稀硫酸除去铁锈。请回答下列问题:
(1)需要98%浓硫酸的体积为_______ mL。
(2)配制过程中,下列仪器不需要的有_______ (填写仪器名称)。

(3)实验时,如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后再涂上3%-5%的溶液_______ (填名称)。
(4)经测定,配制的稀硫酸中溶质的质量分数小于9.2%,其原因可能是下列中的_______。
①所用98%的浓硫酸在实验桌上敞口放置一段时间
②稀释前,用蒸馏水润洗配制稀硫酸的烧杯
③量取水的体积时,俯视读数
④把量好的水倒入烧杯时,有少量水浅出烧杯
⑤量取浓硫酸的体积时,仰视读数
(1)需要98%浓硫酸的体积为
(2)配制过程中,下列仪器不需要的有

(3)实验时,如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后再涂上3%-5%的溶液
(4)经测定,配制的稀硫酸中溶质的质量分数小于9.2%,其原因可能是下列中的_______。
①所用98%的浓硫酸在实验桌上敞口放置一段时间
②稀释前,用蒸馏水润洗配制稀硫酸的烧杯
③量取水的体积时,俯视读数
④把量好的水倒入烧杯时,有少量水浅出烧杯
⑤量取浓硫酸的体积时,仰视读数
| A.①③⑤ | B.③④⑤ | C.①② | D.②④ |
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐3】城市立体农场无土栽培可将农业环节融入高层建筑,实现城市粮食与果蔬的自给自足。农业上配制无土栽培营养液时,常使用KNO3作为氮源和钾源的补充。
(1)试计算:KNO3中氮元素的质量分数为_____ (计算结果精确到0.1%)。
(2)无土栽培营养液一般配制成浓缩贮备液后,再用大量水稀释使用。某校实验小组欲在实验室配制浓缩营养液100g,该营养液中硝酸钾质量分数为16%。请回答:

①配制该营养液应选择____ (填10、50或100)mL的量筒量取。
②图1中还缺少的一种玻璃仪器是_____ ;若该小组同学按图2进行实验,则该实验小组实际配制的硝酸钾溶质质量分数为(水的密度为1g/cm3)_______ 。
③下列实验操作与目的分析均正确的是______ (填字母序号)
(3)黄瓜无土栽培营养液中含硝酸钾(KNO3)的溶质质量分数为2%,若将100g16%的浓缩液加水稀释,可获取成2%的溶液______ g。
(1)试计算:KNO3中氮元素的质量分数为
(2)无土栽培营养液一般配制成浓缩贮备液后,再用大量水稀释使用。某校实验小组欲在实验室配制浓缩营养液100g,该营养液中硝酸钾质量分数为16%。请回答:

①配制该营养液应选择
②图1中还缺少的一种玻璃仪器是
③下列实验操作与目的分析均正确的是
| 选项 | 实验操作 | 目的分析 |
| A | 称量时,将取出的过量的硝酸钾放回原瓶 | 节约药品 |
| B | 称取硝酸钾时,在天平两边托盘上各放一张质量相等的纸 | 整洁美观 |
| C | 量取水时,视线与量筒内凹液面的最低处保持水平 | 准确读数 |
(3)黄瓜无土栽培营养液中含硝酸钾(KNO3)的溶质质量分数为2%,若将100g16%的浓缩液加水稀释,可获取成2%的溶液
您最近一年使用:0次
【推荐1】水是一种宝贵的资源,根据所学知识回答下列问题。
(1)把少量下列物质放入水中,充分搅拌,可得到溶液的是_______
(2)电解水实验中用_______ 检验正极产生的气体。
(3)生活中可用加了洗涤剂的水清洗油污,因为洗涤剂具有_______ 作用。
(4)我国淡水资源缺乏,下图是太阳能海水淡化装置示意图:

在该装置中将一定量的海水暴晒一段时间后,剩余海水中溶质的质量分数会_______ (填“变大”、“变小”或“不变”),淡化后的水可用_______ 检验是否是软水。
(5)配制100g溶质质量分数为6%的氯化钠溶液时需用玻璃棒不断搅拌,其目的是_______ ,若需将其稀释为溶质质量分数为2%的氯化钠溶液,需要加水的质量为_______ g。
(1)把少量下列物质放入水中,充分搅拌,可得到溶液的是_______
| A.碘 | B.牛奶 | C.橄榄油 | D.乙醇 |
(2)电解水实验中用
(3)生活中可用加了洗涤剂的水清洗油污,因为洗涤剂具有
(4)我国淡水资源缺乏,下图是太阳能海水淡化装置示意图:

在该装置中将一定量的海水暴晒一段时间后,剩余海水中溶质的质量分数会
(5)配制100g溶质质量分数为6%的氯化钠溶液时需用玻璃棒不断搅拌,其目的是
您最近一年使用:0次
填空与简答-流程题
|
较易
(0.85)
解题方法
【推荐2】某工厂将矿物燃料燃烧产生的废气中的SO2收集起来,既可以生产稀硫酸,又能制备氢气,其反应过程如图所示:(碘的相对原子质量是127)

(1)写出反应器中发生的化学反应方程式_____________ ,
(2)膜反应器中发生的化学反应属于__________ 反应(填写化学反应类型名称);
(3)此制备过程中可循环利用的物质是__________ (填物质名称)。
(4)硫酸用途广泛,汽车铅酸蓄电池中含有硫酸,其中需要用到溶质质量分数为24.5%的硫酸溶液。
①同学们在实验室用浓硫酸配制稀硫酸,除用到胶头滴管、量筒、烧杯外,还需要用到的仪器有________ 。
②实验室用98%的浓硫酸(密度1.84g/mL)配制24.5%的硫酸溶液1200g。需要水的质量为______ 克,需要98%浓硫酸的体积为_______ mL(计算结果保留至0.1)。

(1)写出反应器中发生的化学反应方程式
(2)膜反应器中发生的化学反应属于
(3)此制备过程中可循环利用的物质是
(4)硫酸用途广泛,汽车铅酸蓄电池中含有硫酸,其中需要用到溶质质量分数为24.5%的硫酸溶液。
①同学们在实验室用浓硫酸配制稀硫酸,除用到胶头滴管、量筒、烧杯外,还需要用到的仪器有
②实验室用98%的浓硫酸(密度1.84g/mL)配制24.5%的硫酸溶液1200g。需要水的质量为
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
名校
解题方法
【推荐3】2020年7月1日沪苏通高铁通车,苏州所辖的张家港、常熟和太仓三市,同时接入长三角铁路网,进入高铁时代。请回答下列问题:
(1)高铁轨道焊接时,可用铝热反应 ,该反应属于
,该反应属于______ 反应(填基本反应类型)。
(2)高铁站的主体结构钢筋混凝土属于______ (填字母)。
A.无机非金属材料 B.金属材料 C.有机合成材料 D.复合材料
(3)高铁刹车制动盘使用合金锻钢制作,说明该合金具有耐高温、耐磨、______ 等特性。
(4)高铁上提供的餐点食品包括米饭、鸡肉、蔬菜、牛奶等,其中富含糖类的是______ 。
(5)高铁站欲配制2%的过氧乙酸溶液1500g用于喷雾消毒,需要15%的过氧乙酸溶液______ g。若量取水时仰视读数,则配制溶液的溶质质量分数______ (填“偏大”或“偏小”或“无影响”)。
(1)高铁轨道焊接时,可用铝热反应
 ,该反应属于
,该反应属于(2)高铁站的主体结构钢筋混凝土属于
A.无机非金属材料 B.金属材料 C.有机合成材料 D.复合材料
(3)高铁刹车制动盘使用合金锻钢制作,说明该合金具有耐高温、耐磨、
(4)高铁上提供的餐点食品包括米饭、鸡肉、蔬菜、牛奶等,其中富含糖类的是
(5)高铁站欲配制2%的过氧乙酸溶液1500g用于喷雾消毒,需要15%的过氧乙酸溶液
您最近一年使用:0次
【推荐1】家用清洁产品中蕴含着丰富的酸碱盐的化学知识。根据下表完成下面小题。
(1)去污粉与除垢净不能混合使用,其原因是________ 。(写化学方程式)
(2)管道通内含有氢氧化钠,使用时不能接触皮肤,因氢氧化钠具有________ 性。
(3)管道通使用时利用Al与NaOH溶液反应放出大量的热,以加快NaOH与淤积物的作用,该反应的化学方程式为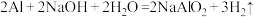 。该反应中属于氧化物的是
。该反应中属于氧化物的是_______ (填化学式)。
(4)硝酸钾、氯化钾是常见的盐,常用于作化学肥料。如图所示是硝酸钾(KNO3)和氯化钾(KCl)的溶解度曲线,请回答下列问题。

①10℃时,KNO3和KCl的溶解度大小关系是:KNO3_______ KCl(填“>”、“<”或“=”)。
②KNO3中混有少量的KCl,可用_______ 的方法提纯KNO3(填“降温结晶”或“蒸发结晶”)。
③60℃时,将210gKNO3的饱和溶液稀释成10%,需加水________ g;
清洁产品 | 除垢净 | 去污粉 | 管道通 |
主要成分 | 盐酸 | 碳酸钠 | 氢氧化钠、铝粉 |
(2)管道通内含有氢氧化钠,使用时不能接触皮肤,因氢氧化钠具有
(3)管道通使用时利用Al与NaOH溶液反应放出大量的热,以加快NaOH与淤积物的作用,该反应的化学方程式为
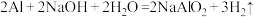 。该反应中属于氧化物的是
。该反应中属于氧化物的是(4)硝酸钾、氯化钾是常见的盐,常用于作化学肥料。如图所示是硝酸钾(KNO3)和氯化钾(KCl)的溶解度曲线,请回答下列问题。

①10℃时,KNO3和KCl的溶解度大小关系是:KNO3
②KNO3中混有少量的KCl,可用
③60℃时,将210gKNO3的饱和溶液稀释成10%,需加水
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】按要求书写正确的化学方程式
(1)“湿法炼铜”原理__________ 。
(2)赤铁矿炼铁____________ 。
(3)工业制取二氧化碳________ 。
(1)“湿法炼铜”原理
(2)赤铁矿炼铁
(3)工业制取二氧化碳
您最近一年使用:0次


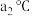 时,将
时,将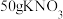 放入50g水中充分搅拌,所得溶液质量为
放入50g水中充分搅拌,所得溶液质量为

