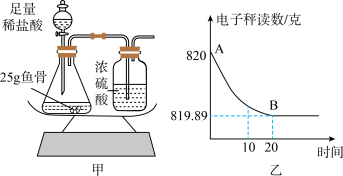
同学们把一定量的石灰石样品放入烧杯中,并加入一定质量分数的稀盐酸至不产生气体时为止,加入稀盐酸和烧杯内物质的质量关系如图所示。(已知:其他成分不参与反应且不溶于水)_______ g。
(2)反应后,向烧杯中再加入5.4g水,求所得溶液中溶质的质量分数。(写出计算过程)

(2)反应后,向烧杯中再加入5.4g水,求所得溶液中溶质的质量分数。(写出计算过程)
2023·内蒙古呼伦贝尔·二模 查看更多[6]
2023年内蒙古呼伦贝尔市海拉尔区中考二模化学试题内蒙古巴彦淖尔市第二中学2023-2024学年九年级上学期期末化学试卷 (已下线)黄金卷01(烟台专用)-【赢在中考·黄金8卷】备战2024年中考化学模拟卷(山东专用)2024年陕西省乾县中考一模考试化学试题(已下线)信息必刷卷01(武汉专用)-2024年中考化学考前信息必刷卷山东省滨州市沾化区下河乡实验学校2023-2024学年九年级下学期第一次月考化学试题
更新时间:2023-09-28 21:11:29
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】取一定量NaHCO3固体样品(杂质不参与反应)放入烧杯中,然后将一定溶质质量分数的盐酸逐滴加入样品中,边加边搅拌,测得生成气体的质量与所加盐酸的质量关系如图所示。(发生反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑)
请分析并计算:
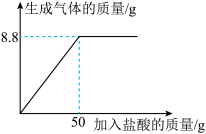
(1)恰好完全反应时产生气体的质量是______ g;
(2)计算所加盐酸的溶质质量分数______ 。
请分析并计算:

(1)恰好完全反应时产生气体的质量是
(2)计算所加盐酸的溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】化学兴趣小组的同学对某铁的合金(杂质全部为碳)进行组成分析。取该合金样品17.5g于烧杯中,向烧杯中加入某浓度的稀硫酸200g,恰好完全反应,反应的化学方程式为Fe+H2SO4=FeSO4+H2↑,测得烧杯中剩余物质的质量为216.9g。请计算该铁的合金样品中铁的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】某同学欲配制溶质质量分数为3%的过氧化氢溶液作为消毒液。现有一瓶标签已破损的过氧化氢溶液,为测定瓶内溶液中溶质的质量分数,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g。
(1) 生成氧气的质量;
(2) 瓶内过氧化氢溶液中溶质的质量分数;
(3) 若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液1000g,需加入水的质量。
(1) 生成氧气的质量;
(2) 瓶内过氧化氢溶液中溶质的质量分数;
(3) 若取一定量的瓶内溶液配制成溶质质量分数为3%的过氧化氢溶液1000g,需加入水的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】实验室中取2.5g石灰石于烧杯中,将20g足量稀盐酸分批次加入样品中,充分反应后经过滤、干燥、称重,得到如下数据:请计算:(已知杂质既不与酸反应也不溶于水)
求最后所得溶液中氯化钙的质量分数(结果精确到0.1%)。
| 实验次序 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 稀盐酸用量/g | 4.0 | 4.0 | 4.0 | 4.0 | 4.0 |
| 剩余固体质量/g | 2.0 | 1.5 | 1.0 | 0.5 | 0.5 |
求最后所得溶液中氯化钙的质量分数(结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】学习小组的同学想测定某种大理石中碳酸钙的质量分数。取大理石样品25g,逐渐缓慢向其中加入150g溶质质量分数为14.6%的稀盐酸(杂质难溶于水,且不与酸反应),测得剩余固体的质量与加入稀盐酸的质量关系如图所示。
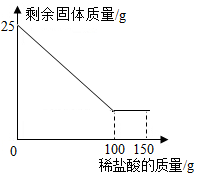
请完成下列分析与计算:
(1)恰好完全反应时消耗稀盐酸的质量是_______g。
(2)计算该大理石中碳酸钙的质量分数。

请完成下列分析与计算:
(1)恰好完全反应时消耗稀盐酸的质量是_______g。
(2)计算该大理石中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】BaCl2是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl2溶液可立即服用MgSO4溶液解毒。为测定某BaCl2溶液的溶质质量分数,现取100 g 该BaCl2溶液,不断加入MgSO4溶液至恰好完全反应,此时用去MgSO4溶液的质量为100 g,反应后所得溶液的质量为176.7g。请回答:
(1)反应后所得溶液中的溶质是______(填化学式);
(2)计算原BaCl2溶液的溶质质量分数(保留到0.1%)。
(1)反应后所得溶液中的溶质是______(填化学式);
(2)计算原BaCl2溶液的溶质质量分数(保留到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入92g稀硫酸,恰好完全反应,测得剩余固体的质量为2g(杂质不溶于水也不与酸反应)。
(1)样品中Fe2O3的质量为 g。
(2)计算反应后所得溶液中溶质的质量分数(要求写出计算过程)。
(1)样品中Fe2O3的质量为 g。
(2)计算反应后所得溶液中溶质的质量分数(要求写出计算过程)。
您最近一年使用:0次