现有100g溶质的质量分数为10%的硝酸钾溶液,若要使溶液中溶质的质量分数增大一倍,可加入硝酸钾______ g或蒸发水______ g(假定溶质不析出)。
更新时间:2023/10/16 16:10:47
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
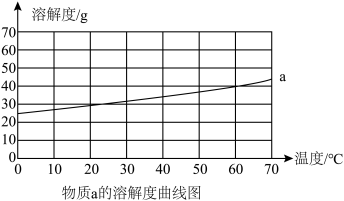
【推荐1】a、b是常见的两种固体物质,根据图表的信息回答下列问题:
物质b的溶解度表
(1)60℃时,物质a的溶解度是______ g。
(2)20℃时,将20g物质b加入到50g水中,充分溶解后得到溶液的质量为________ g。
(3)将50℃时a、b两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数大小关系为a______ b(填“>”、“=”或者“<”)。
(4)下列说法正确的组合是_______ (填字母序号)。
①所有物质的溶解度都随温度的升高面增大
②30℃时,物质的溶解度a小于b
③物质b中含有少量a时,可以采用降温结晶的方法提纯b
④40℃时,分别将物质a、b的饱和溶液降温至10℃,析出物质的质量b大于a
A ①④
B ①③
C ②③
D ②④

物质b的溶解度表
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| b的溶解度/g | 14 | 20 | 30 | 45 | 65 | 85 | 110 |
(1)60℃时,物质a的溶解度是
(2)20℃时,将20g物质b加入到50g水中,充分溶解后得到溶液的质量为
(3)将50℃时a、b两物质的饱和溶液分别降温至20℃,所得溶液的溶质质量分数大小关系为a
(4)下列说法正确的组合是
①所有物质的溶解度都随温度的升高面增大
②30℃时,物质的溶解度a小于b
③物质b中含有少量a时,可以采用降温结晶的方法提纯b
④40℃时,分别将物质a、b的饱和溶液降温至10℃,析出物质的质量b大于a
A ①④
B ①③
C ②③
D ②④
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】在一定温度下,向100g水中依次加入一定质量的KC1固体,充分溶解,加入KCl固体质量与所得溶液质量的关系如图所示:

(1)该温度下,实验①所得溶液是______ 溶液(填“饱和”或“不饱和”);
(2)该温度下,KCl的溶解度为______ 。
(3)实验③所得溶液中溶质的质量分数是______ 。

(1)该温度下,实验①所得溶液是
(2)该温度下,KCl的溶解度为
(3)实验③所得溶液中溶质的质量分数是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】溶液与人类生产、生活密切相关。
(1)如表为硝酸钾和氯化钠的部分溶解度数据,某同学进行了如图所示的两个溶解实验。
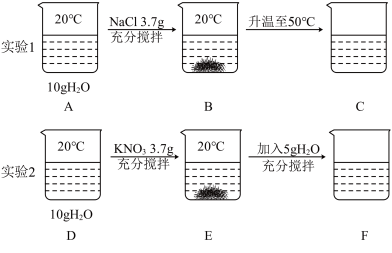
①由表格数据可知,溶解度随温度升高变化显著的物质是_________ (选填“NaCl”或“KNO3”)。
②上述溶液中属于饱和溶液的是______ (填A-F序号)。
③B、C、E、F溶液中溶质质量分数由大到小的关系是__________ 。
(2)t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成图中的斜线。下列说法错误的是( )
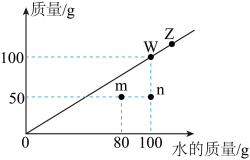
a. t℃时该物质的溶解度为50g
b.图中4个点表示的溶液中只有z是饱和溶液
c.点z向点w移动的一种方法是恒温蒸发一定量的水
d.将m点表示的溶液变为饱和溶液的一种方法是再加入20g溶质
(3)机动车一般使用铅酸蓄电池。某铅酸蓄电池用的酸溶液是质量分数为28%的稀硫酸,若用1L溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸时,需要蒸馏水(密度为1g/cm3的体积为_______ L,配得的稀硫酸质量为_____________ kg。(计算结果保留位小数)
(1)如表为硝酸钾和氯化钠的部分溶解度数据,某同学进行了如图所示的两个溶解实验。
| 物质/溶解度/g/温度 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ | 80℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |

①由表格数据可知,溶解度随温度升高变化显著的物质是
②上述溶液中属于饱和溶液的是
③B、C、E、F溶液中溶质质量分数由大到小的关系是
(2)t℃时,根据某物质在不同质量的水中达到饱和状态时所溶解的质量绘制成图中的斜线。下列说法错误的是

a. t℃时该物质的溶解度为50g
b.图中4个点表示的溶液中只有z是饱和溶液
c.点z向点w移动的一种方法是恒温蒸发一定量的水
d.将m点表示的溶液变为饱和溶液的一种方法是再加入20g溶质
(3)机动车一般使用铅酸蓄电池。某铅酸蓄电池用的酸溶液是质量分数为28%的稀硫酸,若用1L溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸时,需要蒸馏水(密度为1g/cm3的体积为
您最近一年使用:0次
【推荐1】水是最常见的溶剂。
(1)下列溶液用水作溶剂的是___________ (填字母序号)。
a、生理盐水b、碘酒c、葡萄糖溶液
(2)将100g溶质质量分数为98%的浓硫酸稀释为溶质质量分数为10%的稀硫酸,需加水的质量为___________ g。
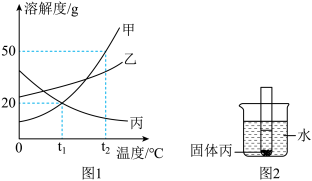
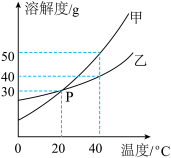
(3)如图1是甲、乙、丙三种固体物质的溶解度曲线。请回答:
①t2℃时,将甲、丙的饱和溶液分别降温至t1℃,仍然饱和的是___________ 的溶液。
②欲从含有少量乙的甲的饱和溶液中提纯甲,可采用___________ 结晶的方法。
③某温度下,为使图2试管中丙的固体溶解,可向烧杯中加入___________ (填字母)。
A.NaOH固体B.NH4NO3固体C.NaCl固体
(1)下列溶液用水作溶剂的是
a、生理盐水b、碘酒c、葡萄糖溶液
(2)将100g溶质质量分数为98%的浓硫酸稀释为溶质质量分数为10%的稀硫酸,需加水的质量为

(3)如图1是甲、乙、丙三种固体物质的溶解度曲线。请回答:
①t2℃时,将甲、丙的饱和溶液分别降温至t1℃,仍然饱和的是
②欲从含有少量乙的甲的饱和溶液中提纯甲,可采用
③某温度下,为使图2试管中丙的固体溶解,可向烧杯中加入
A.NaOH固体B.NH4NO3固体C.NaCl固体
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化钠是一种重要的化工原料,利用海水可制得氯化钠并进而可以制得氢氧化钠、氢气和氯气(Cl2)。其主要工艺流程如图所示。
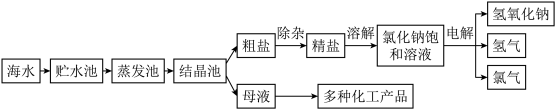
(1)氯原子的结构示意图为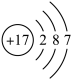 ,其核电荷数为
,其核电荷数为______ ,在化学反应中,该原子容易得到电子,形成氯离子,氯离子的符号为______ 。
(2)粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。
①实验室进行粗盐中难溶性杂质的去除,多步操作需要用到的同一种玻璃仪器是______ 。
②实验室要除去粗盐中的氯化钙,可加入适量的______ (填标号)。
A. 溶液 B.AgNO3溶液 C.Na2CO3溶液
溶液 B.AgNO3溶液 C.Na2CO3溶液
(3)常温下,配制1000kg质量分数为0.9%的氯化钠溶液,需要18%的氯化钠溶液的质量为______ kg。
(4)电解氯化钠饱和溶液的化学方程式是______ 。

(1)氯原子的结构示意图为
 ,其核电荷数为
,其核电荷数为(2)粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。
①实验室进行粗盐中难溶性杂质的去除,多步操作需要用到的同一种玻璃仪器是
②实验室要除去粗盐中的氯化钙,可加入适量的
A.
 溶液 B.AgNO3溶液 C.Na2CO3溶液
溶液 B.AgNO3溶液 C.Na2CO3溶液(3)常温下,配制1000kg质量分数为0.9%的氯化钠溶液,需要18%的氯化钠溶液的质量为
(4)电解氯化钠饱和溶液的化学方程式是
您最近一年使用:0次