碘化银( )是当前我国实施人工增雨的主要物质,下列是碘化银的有关描述:①在常温下为黄色晶体。②几乎不溶于水。③熔点为
)是当前我国实施人工增雨的主要物质,下列是碘化银的有关描述:①在常温下为黄色晶体。②几乎不溶于水。③熔点为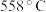 ,沸点为
,沸点为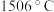 。④在光照条件下可分解为碘(
。④在光照条件下可分解为碘( )和银(
)和银( )
)
(1)上述材料中属于碘化银物理性质的是______ (填序号,下同):
(2)属于碘化银化学性质的是______ ;
(3)为防止碘化银变质,保存时应注意______ 。
 )是当前我国实施人工增雨的主要物质,下列是碘化银的有关描述:①在常温下为黄色晶体。②几乎不溶于水。③熔点为
)是当前我国实施人工增雨的主要物质,下列是碘化银的有关描述:①在常温下为黄色晶体。②几乎不溶于水。③熔点为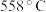 ,沸点为
,沸点为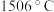 。④在光照条件下可分解为碘(
。④在光照条件下可分解为碘( )和银(
)和银( )
)(1)上述材料中属于碘化银物理性质的是
(2)属于碘化银化学性质的是
(3)为防止碘化银变质,保存时应注意
更新时间:2023-11-07 20:43:06
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】《中国消防网》报道:一辆储运电石的汽车因未做好防水的工作,行驶过程中天降小雨,引发车厢着火。已知电石(CaC2)不可燃,但与水剧烈反应产生乙炔(C2H2)气体,乙炔气体在空气中可以燃烧。
(1)乙炔在燃烧条件中属于______ ;
(2)电石与水反应的化学方程式为:CaC2+2H2O=X+C2H2↑,由此可知X的化学式为______ ;
(3)请从物质组成和化学性质角度,说说你对乙炔的认识(各一点):
组成:______ ;化学性质:______ 。
(1)乙炔在燃烧条件中属于
(2)电石与水反应的化学方程式为:CaC2+2H2O=X+C2H2↑,由此可知X的化学式为
(3)请从物质组成和化学性质角度,说说你对乙炔的认识(各一点):
组成:
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】请阅读下面的短文,然后回答有关问题。
钠是一种活泼金属,其原子的结构示意图为 ,钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目;银白色有金属光泽,钠的密度是0.97g/cm3。钠还能与水反应,生成氢氧化钠和氢气。
,钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目;银白色有金属光泽,钠的密度是0.97g/cm3。钠还能与水反应,生成氢氧化钠和氢气。
目前,世界上多数采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。电解时,正极放出氯气,负极产生的金属钠和金属钙同时浮在共熔物,从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出, 通过过滤可以分离出金属钠。
金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物。还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生成钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
依据文章内容,回答下列问题:
(1)钠具有的物理性质有_______ 、_______ (写出两点即可)。
(2)在钠的原子结构中,与钠元素化学性质密切相关的是_______ 。
(3)工业常用电解熔融 NaCl 的方法来制得金属钠,方程式为2NaCl 2Na+Cl2↑,该反应属于基本反应类型中的
2Na+Cl2↑,该反应属于基本反应类型中的_______ 反应。
(4)金属钠的用途_______ (写出一点即可)。
(5)实验室中的金属钠通常保存在煤油中的原因是(填字母序号)。
钠是一种活泼金属,其原子的结构示意图为
 ,钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目;银白色有金属光泽,钠的密度是0.97g/cm3。钠还能与水反应,生成氢氧化钠和氢气。
,钠在空气中极易被氧化,用小刀一切,就能观察到它的本来面目;银白色有金属光泽,钠的密度是0.97g/cm3。钠还能与水反应,生成氢氧化钠和氢气。目前,世界上多数采用电解熔融氯化钠的方法来制得金属钠,氯化钠的熔点为801℃,将氯化钠和氯化钙按质量比2:3混合共熔,可得到熔融温度约为580℃的共熔物,降低了电解所需的温度。电解时,正极放出氯气,负极产生的金属钠和金属钙同时浮在共熔物,从管道溢出,把熔融的金属混合物冷却到105-110℃,金属钙结晶析出, 通过过滤可以分离出金属钠。
金属钠的应用非常广泛,可以用于制造过氧化钠(Na2O2)等化合物。还能用于生产更加昂贵的金属钾,以钠和氯化钾为原料,在高温条件下,生成钾和氯化钠,生成的钾能以蒸汽的形式分离出来。
依据文章内容,回答下列问题:
(1)钠具有的物理性质有
(2)在钠的原子结构中,与钠元素化学性质密切相关的是
(3)工业常用电解熔融 NaCl 的方法来制得金属钠,方程式为2NaCl
 2Na+Cl2↑,该反应属于基本反应类型中的
2Na+Cl2↑,该反应属于基本反应类型中的(4)金属钠的用途
(5)实验室中的金属钠通常保存在煤油中的原因是(填字母序号)。
| A.钠是金属 | B.钠能与氧气反应 |
| C.钠能与水反应 | D.钠的密度比煤油的密度(0.8g/cm3)大 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】以煤粉灰(主要成分为 、
、 及少量
及少量 等)为原料制取
等)为原料制取 的部分工艺流程如图1。
的部分工艺流程如图1。


【查阅资料】 溶液中滴入
溶液中滴入 溶液会呈血红色。
溶液会呈血红色。 不溶于水也不与酸反应。
不溶于水也不与酸反应。
(1)“酸浸”过程中所得滤渣的主要成分是______ ,“酸浸”时温度不宜过高的原因是______ 。
(2)“除铁”时,发生的反应为 ;检验溶液中铁元素已除尽的方法是
;检验溶液中铁元素已除尽的方法是______ 。
(3)“结晶”是向浓溶液中通入 气体,从而获得
气体,从而获得 晶体的过程。溶液中
晶体的过程。溶液中 和盐酸的浓度随通气时间的变化如图2所示。由此可得出的结论是
和盐酸的浓度随通气时间的变化如图2所示。由此可得出的结论是______ 。
(4)流程中可循环利用的物质为______ (写化学式)
(5)高温烧结的氧化铝,又称人造刚玉或人造宝石,可用于制机械轴承、钟表中的钻石、坩埚、高强度陶瓷等。由此可推知氧化铝的性质有______(填标号)
 、
、 及少量
及少量 等)为原料制取
等)为原料制取 的部分工艺流程如图1。
的部分工艺流程如图1。

【查阅资料】
 溶液中滴入
溶液中滴入 溶液会呈血红色。
溶液会呈血红色。 不溶于水也不与酸反应。
不溶于水也不与酸反应。(1)“酸浸”过程中所得滤渣的主要成分是
(2)“除铁”时,发生的反应为
 ;检验溶液中铁元素已除尽的方法是
;检验溶液中铁元素已除尽的方法是(3)“结晶”是向浓溶液中通入
 气体,从而获得
气体,从而获得 晶体的过程。溶液中
晶体的过程。溶液中 和盐酸的浓度随通气时间的变化如图2所示。由此可得出的结论是
和盐酸的浓度随通气时间的变化如图2所示。由此可得出的结论是(4)流程中可循环利用的物质为
(5)高温烧结的氧化铝,又称人造刚玉或人造宝石,可用于制机械轴承、钟表中的钻石、坩埚、高强度陶瓷等。由此可推知氧化铝的性质有______(填标号)
| A.硬度大 | B.熔点高 | C.性质稳定 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】我国女科学家屠呦呦荣获2016年度国家最高科学技术奖,青蒿素复方药物被世界卫生组织正式将列为治疗疟疾的首选药物,中国神药在世界各地显示了奇效。请回答:
(1)由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的过程中,主要是_____ (填“物理”或“化学”)性质发生变化,从微观角度解释原因为______ 。
(2)人类对付疟疾的最有力药物还有一种是从植物金鸡纳树皮上提取出的奎宁,俗名金鸡纳霜,微溶于水,在阳光下逐渐变为黄色,保存奎宁药品的方法是_____ 。
(3)在1984年实现了青蒿素的人工合成。青蒿素的相对分子质量为_____ ,其中碳、氢、氧元素质量的最简比为______ ,其中碳元素的质量分数为_____ (精确到0.1%)。
(1)由青蒿酸(C15H22O2)合成青蒿素(C15H22O5)的过程中,主要是
(2)人类对付疟疾的最有力药物还有一种是从植物金鸡纳树皮上提取出的奎宁,俗名金鸡纳霜,微溶于水,在阳光下逐渐变为黄色,保存奎宁药品的方法是
(3)在1984年实现了青蒿素的人工合成。青蒿素的相对分子质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】人类的日常生活处处与化学紧密相连,请按要求回答下列问题。
(1)在书写具有保存价值的档案时,规定使用碳素墨水的原因是______ 。
(2)医疗上的生理盐水是用水和______ 配制的(写名称)。
(3)衣服、餐具上的油污可以用加入洗涤剂的水洗掉,是利用洗涤剂的______ 作用。
(4)疫情防控。佩戴口罩能有效阻挡病毒的传播,其原理类似于化学实验中的______ 操作。测量体温时,水银温度计的汞柱随温度的升高而变长,其微观原因是______ 。
(5)实践感悟。物质的______ 决定用途,化学在保证人类生存并提高生活质量方面起着重要的作用。
(1)在书写具有保存价值的档案时,规定使用碳素墨水的原因是
(2)医疗上的生理盐水是用水和
(3)衣服、餐具上的油污可以用加入洗涤剂的水洗掉,是利用洗涤剂的
(4)疫情防控。佩戴口罩能有效阻挡病毒的传播,其原理类似于化学实验中的
(5)实践感悟。物质的
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
【推荐3】金刚石和石墨都由碳元素组成,但是你知道金刚石是从何而来的吗?现在有两种观点:①通过探查与实验。人们认为金刚石是岩石本身具有的游离碳在剧烈上升和发生爆炸的过程中,在高温高压的条件下结晶形成的,人们也依此成批量的生产人造金刚石。②我们在自然界中发现的所有金刚石都是来自红巨星在富氢与高温的条件下,由炭气浓缩而成的。
(1)依据以上两种观点,在一定条件下红巨星上的炭气转化为金刚石的微观实质为_____ 。
(2)证明金刚石中含有碳元素的方法是_____ 。
(1)依据以上两种观点,在一定条件下红巨星上的炭气转化为金刚石的微观实质为
(2)证明金刚石中含有碳元素的方法是
您最近一年使用:0次



