某化学兴趣小组在实验室利用氯酸钾和二氧化锰的混合物制取氧气,甲同学进行了如下图所示的实验。根据以下信息回答下列问题:
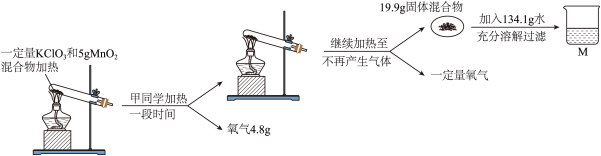
(1)写出实验中发生反应的方程式_______ 。
(2)根据已知条件列出求解甲同学第一次实验时生成氯化钾质量(X)的比例式_______ ;
(3)甲同学两次实验中分解氯酸钾的质量比为_______ ;
(4)甲同学第二次实验前后装置内固体物质质量变化情况为_______ ;
(5)溶液M中溶质的质量分数为_______ 。

(1)写出实验中发生反应的方程式
(2)根据已知条件列出求解甲同学第一次实验时生成氯化钾质量(X)的比例式
(3)甲同学两次实验中分解氯酸钾的质量比为
(4)甲同学第二次实验前后装置内固体物质质量变化情况为
(5)溶液M中溶质的质量分数为
更新时间:2023-11-29 21:35:42
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】中国空间站“天和核心舱”有一定量的过氧化钠(Na2O2)以备不时之需,已知过氧化钠与二氧化碳反应生成碳酸钠和氧气,则反应的化学方程式为___________ ;若100kg过氧化钠在使用前后钠元素的质量分数之比为53:39,则产生氧气的质量为___________ kg(准确到0.1)。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】为测定某生铁样品中铁的含量,现将20g生铁样品加入到200g稀盐酸中恰好完全反应(杂质不溶于水,也不与酸反应,杂质中不含铁元素),实验过程及测得的数据如下:

(1)写出上述反应的化学方程式______ 。
(2)求解该铁样品中参加反应的铁的质量(x)的比例式是______ 。
(3)向过滤后所得滤液中加入43.2g水,则最终所得溶液中溶质的质量分数______ 。
(4)若用14.6%的浓盐酸配制上述实验中所用的稀盐酸,需14.6%的浓盐酸的质量为______ 。
(5)若工业上用含氧化铁80%的赤铁矿10t,(假设炼制过程中铁矿石的利用率为90%)。能炼出上述生铁的质量为______ 。

(1)写出上述反应的化学方程式
(2)求解该铁样品中参加反应的铁的质量(x)的比例式是
(3)向过滤后所得滤液中加入43.2g水,则最终所得溶液中溶质的质量分数
(4)若用14.6%的浓盐酸配制上述实验中所用的稀盐酸,需14.6%的浓盐酸的质量为
(5)若工业上用含氧化铁80%的赤铁矿10t,(假设炼制过程中铁矿石的利用率为90%)。能炼出上述生铁的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】为了探究影响金属与酸反应速率的因素,某实验小组用足量形状相同的镁片和铝片分别与40g溶质质量分数为7.3%的稀盐酸反应,用数据采集器测得装置内压强随时间变化的关系图(如图)。已知在相同温度下,装置内压强与气体体积成正比。

(1)写出铝与稀盐酸反应的化学方程式______ 。
(2)曲线BC段下降的原因是______ 。
(3)根据图乙可知,充分反应后产生氢气的质量:Mg_____ (填“>”“<”或“=”)Al。
(4)计算镁片与稀盐酸反应产生氢气的质量(写出计算过程,6分)。

(1)写出铝与稀盐酸反应的化学方程式
(2)曲线BC段下降的原因是
(3)根据图乙可知,充分反应后产生氢气的质量:Mg
(4)计算镁片与稀盐酸反应产生氢气的质量(写出计算过程,6分)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】面粉是制作美食的原材料。在发面团的过程中会生成酸而影响口味,为使食品更美味,可以加碱面处理。碱面的主要成分为碳酸钠(Na2CO3),为测定某品牌碱面中碳酸钠的质量分数,小金按照如图甲所示实验装置,利用碱面与盐酸反应生成二氧化碳气体的质量来计算碱面中碳酸钠的质量分数(杂质不与盐酸反应)。小金各取11.0克碱面样品与一定量的稀盐酸进行三次实验,三次实验所采集的数据见表。


合理选择表中数据并请完成下列问题:
(1)三次实验中第______次实验碱面样品与一定量的稀盐酸恰好完全反应,生成______g二氧化碳。
(2)计算碱面中碳酸钠的质量分数。(写出计算步骤)
(3)为完成碳酸钠质量分数的测定实验,气体发生装置应选择图乙中的______装置(填字母)。
(4)按照图甲实验装置测定的CO2气体质量,可能导致CO2质量测定结果偏小的原因______(写出一种即可)。


| 实验次数 | 碱面样品质量/克 | 稀盐酸质量/克 | 气体的质量/克 |
| 1 | 11.0 | 50.0 | 1.1 |
| 2 | 11.0 | 200.0 | 4.4 |
| 3 | 11.0 | 250.0 | 4.4 |
合理选择表中数据并请完成下列问题:
(1)三次实验中第______次实验碱面样品与一定量的稀盐酸恰好完全反应,生成______g二氧化碳。
(2)计算碱面中碳酸钠的质量分数。(写出计算步骤)
(3)为完成碳酸钠质量分数的测定实验,气体发生装置应选择图乙中的______装置(填字母)。
(4)按照图甲实验装置测定的CO2气体质量,可能导致CO2质量测定结果偏小的原因______(写出一种即可)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,他们取了6g石灰石(其中杂质不反应,也不溶于水)放入烧杯中,再将80g稀盐酸分4次加入该烧杯中,充分反应后测得实验数据如下表(不考虑CO2溶解于水)。
(1)表格中m的值为____________ 。
(2)大理石中CaCO3的质量分数是_____ ?
(3)恰好反应后所得溶液中溶质的质量是______ ?(写出计算过程)
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
| 烧杯中剩余物质的质量/g | 25.2 | m | 63.8 | 83.8 |
(2)大理石中CaCO3的质量分数是
(3)恰好反应后所得溶液中溶质的质量是
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】化学兴趣小组的同学在实验室中用加热4.9g氯酸钾和1.58g高锰酸钾混合物的方法进行了制取氧气的研究,得到如图所示的曲线图。试回答:

(1)b~c段产生氧气的速度明显比O~b段加快,其原因是______。
(2)反应结束后所得固体混合物中质量分数最大的物质的质量分数是多少?___(写出计算过程,精确到小数点后一位)

(1)b~c段产生氧气的速度明显比O~b段加快,其原因是______。
(2)反应结束后所得固体混合物中质量分数最大的物质的质量分数是多少?___(写出计算过程,精确到小数点后一位)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某化学小组加热氯酸钾和二氧化锰混合物制取氧气,用分析天平称得试管中固体的质量随时间变化的数据见下表。实验结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体(二氧化锰难溶于水)。通过计算回答:
(1)共制得氧气质量为______________g。
(2)回收二氧化锰的质量为______________g。(要求有计算过程)
(3)计算加热前的固体混合物中氯酸钾的质量分数(要求有计算过程)。
| 加热时间/min | 0 | t1 | t2 | t3 | t4 |
| 试管中固体质量/g | 28.0 | 23.2 | 21.8 | 18.4 | 18.4 |
(1)共制得氧气质量为______________g。
(2)回收二氧化锰的质量为______________g。(要求有计算过程)
(3)计算加热前的固体混合物中氯酸钾的质量分数(要求有计算过程)。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,俊充分反应,实验数据如下:
求:(1)黄铜样品中锌的质量分数____;(写出计算步骤,下同)
(2)完全反应后产生氢气的质量_____;
(3)所用稀硫酸的质量分数____。
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
求:(1)黄铜样品中锌的质量分数____;(写出计算步骤,下同)
(2)完全反应后产生氢气的质量_____;
(3)所用稀硫酸的质量分数____。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】现有一块锌铜合金,某同学对其成分进行分析。取10g此样品,向其中分五次加入相同溶质质量分数的稀盐酸,使之充分反应,每次所用稀盐酸的质量及剩余固体的质量记录于下表:
试计算:
(1)表格中m的值为___________ 。
(2)所加入稀盐酸中溶质的质量分数。
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
充分反应后剩余固体的质量/g | 8.7 | 7.4 | 6.1 | 5.6 | m |
试计算:
(1)表格中m的值为
(2)所加入稀盐酸中溶质的质量分数。
您最近一年使用:0次





