请回答下列问题。
(1)“富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗、炼钢等,这主要利用了氧气的______ 性质(填“物理”或“化学”)。
季节交替期间容易得感冒等疾病,在医院重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和“富氧空气”差不多,化学兴趣小组欲混制“富氧空气”并开展探究,进行以下实验:
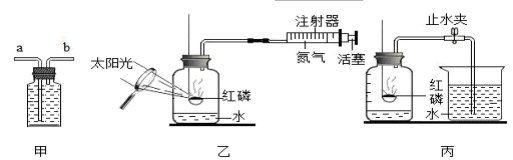
实验一:混制“富氧空气”用纯氮气及氧气,混制一瓶(集气瓶容积为250 mL)氧气体积分数为40%的“富氧空气”。
(2)先在图甲装置中装满水,再从导管______ (填“a”或“b”),先通入氮气排出120 mL水,再通入氧气排出______ mL水。
实验二:测定上述“富氧空气”中氧气的含量。用如图乙装置测定“富氧空气”中氧的含量(实验前注射器中有35 mL氮气,100 mL集气瓶中已收集好实验一中“富氧空气”)加入20 mL水,导管的体积忽略不计,燃烧匙内有足量红磷。实验数据记录如下:
(3)根据以上实验过程和数据综合分析,集气瓶内空气中氧气的体积是______ mL;开始体积增大的原因是______ 。
(4)图乙相较于课本上测定空气中氧气的含量装置(图丙),优点______ 。
(1)“富氧空气”是指氧气含量高于普通空气的气体,可用于航天、医疗、炼钢等,这主要利用了氧气的
季节交替期间容易得感冒等疾病,在医院重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质也和“富氧空气”差不多,化学兴趣小组欲混制“富氧空气”并开展探究,进行以下实验:

实验一:混制“富氧空气”用纯氮气及氧气,混制一瓶(集气瓶容积为250 mL)氧气体积分数为40%的“富氧空气”。
(2)先在图甲装置中装满水,再从导管
实验二:测定上述“富氧空气”中氧气的含量。用如图乙装置测定“富氧空气”中氧的含量(实验前注射器中有35 mL氮气,100 mL集气瓶中已收集好实验一中“富氧空气”)加入20 mL水,导管的体积忽略不计,燃烧匙内有足量红磷。实验数据记录如下:
| 时间/min | 0 | 1 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| 注射器读数/mL | 35.0 | 44.0 | 44.2 | 30.6 | 22.8 | 16.4 | 13.6 | 11.2 | 10.0 | 10.0 | 10.0 |
(4)图乙相较于课本上测定空气中氧气的含量装置(图丙),优点
更新时间:2023-11-30 11:45:11
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】人类生活生产离不开金属,不仅因为其物理性能优良,还与其化学性质密切相关。

(1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高。主要用于航天和航海工业。上述描述中属于钛化学性质的是____________ 。
(2)某小组用如图甲所示装置进行探究。4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是____________ 。
(3)图乙实验:试管①、②中装有铁粉,分别加入一定量氯化锌溶液和氯化铜溶液,该对比实验的目的可能是____________ ;充分反应后,将试管①、②内的物质全部倒入同一烧杯中搅拌、混合,发现烧杯中的红色固体物质明显增多。下列说法不正确的是____________ 。
A.混合前试管②反应后固体中一定只有铜
B.混合后烧杯固体中一定没有铁
C.混合后烧杯液体中一定含有Zn2+、Fe2+、Cu2+

(1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高。主要用于航天和航海工业。上述描述中属于钛化学性质的是
(2)某小组用如图甲所示装置进行探究。4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是
(3)图乙实验:试管①、②中装有铁粉,分别加入一定量氯化锌溶液和氯化铜溶液,该对比实验的目的可能是
A.混合前试管②反应后固体中一定只有铜
B.混合后烧杯固体中一定没有铁
C.混合后烧杯液体中一定含有Zn2+、Fe2+、Cu2+
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
【推荐2】阅读下面科普短文
饮茶在我国具有悠久历史,茶叶中含有一类叫茶多酚的物质。茶多酚是茶叶中酚类物质及其衍生物的总称,并不是一种物质,因此常称为多酚类。茶多酚为淡黄色至茶褐色略带茶香的粉状固体或结晶,易落于水、乙醇,在空气中易氧化变色,略有吸水性。耐热性及耐酸性好,在碱性条件下易氧化褐变。从茶叶中提取茶多酚可未用下列办法。

不同茶叶中茶多酚的含量不同,人们常利用茶多酚能与亚铁离子反应形成紫蓝色物质,依据溶液颜色的深浅与茶多酚含量成正比的原理,测定不同种类、不同品质的茶叶中茶多酚含量。下图1和图2为不同种类、不同品质的茶叶中茶多酚含量。

酚类物质一般都是生长在最新鲜的叶子上,茶叶越鲜嫩,茶多酚含量越高,随着茶叶生长和变老,茶多酚含量会降低。A类绿茶所选用的原料一般为一芽一叶或一芽二叶,芽的含量高,它们是茶叶中最鲜嫩的部分,生长周期短,最接近阳光能够充分与阳光进行光合作用,又具有顶端优势,叶内能合成较多的酚类物质。B类绿茶以一芽二三叶为主,C类绿茶所用的原料是生长周期更长的叶子,芽少且瘦薄。图3所示。

研究表明,茶多酚是茶叶中有保健功能的主要成分之一。茶多酚能够抗衰老、抗辐射、抗菌杀菌等。茶多酚对重金属具有较强的吸附作用,能与重金属形成沉淀,有利于减轻重金属叶人体产生的毒害作用。
依据文章内容回答下列问题
(1)茶多酚的物理性质有_______
(2)提取茶多酚的过程中,操作①的名称是_______
(3)由图1和图2可知,茶多酚含量最高的茶叶是____ ,依据文中内容解释其中茶多酚含量较高的原因是_______
(4)下列关于茶多酚的说法正确的是_______ (填序号)。
A用热水泡茶会降低茶多酚含量 B茶多酚可与氧气、亚铁离子发生化学反应
C新鲜茶叶中茶多酚含量较高 D多喝绿茶有利于减少重金属的毒害作用
饮茶在我国具有悠久历史,茶叶中含有一类叫茶多酚的物质。茶多酚是茶叶中酚类物质及其衍生物的总称,并不是一种物质,因此常称为多酚类。茶多酚为淡黄色至茶褐色略带茶香的粉状固体或结晶,易落于水、乙醇,在空气中易氧化变色,略有吸水性。耐热性及耐酸性好,在碱性条件下易氧化褐变。从茶叶中提取茶多酚可未用下列办法。

不同茶叶中茶多酚的含量不同,人们常利用茶多酚能与亚铁离子反应形成紫蓝色物质,依据溶液颜色的深浅与茶多酚含量成正比的原理,测定不同种类、不同品质的茶叶中茶多酚含量。下图1和图2为不同种类、不同品质的茶叶中茶多酚含量。

酚类物质一般都是生长在最新鲜的叶子上,茶叶越鲜嫩,茶多酚含量越高,随着茶叶生长和变老,茶多酚含量会降低。A类绿茶所选用的原料一般为一芽一叶或一芽二叶,芽的含量高,它们是茶叶中最鲜嫩的部分,生长周期短,最接近阳光能够充分与阳光进行光合作用,又具有顶端优势,叶内能合成较多的酚类物质。B类绿茶以一芽二三叶为主,C类绿茶所用的原料是生长周期更长的叶子,芽少且瘦薄。图3所示。

研究表明,茶多酚是茶叶中有保健功能的主要成分之一。茶多酚能够抗衰老、抗辐射、抗菌杀菌等。茶多酚对重金属具有较强的吸附作用,能与重金属形成沉淀,有利于减轻重金属叶人体产生的毒害作用。
依据文章内容回答下列问题
(1)茶多酚的物理性质有
(2)提取茶多酚的过程中,操作①的名称是
(3)由图1和图2可知,茶多酚含量最高的茶叶是
(4)下列关于茶多酚的说法正确的是
A用热水泡茶会降低茶多酚含量 B茶多酚可与氧气、亚铁离子发生化学反应
C新鲜茶叶中茶多酚含量较高 D多喝绿茶有利于减少重金属的毒害作用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】“科技梦”助推“中国梦”,新材料的研发、科技的发展都离不开化学。
(1)我国科研人员自主设计的“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
①氘和氚属于___________ (填“同种”或“不同种”)元素的原子。
②贮存氘气的钢瓶禁止靠近明火,据此推测氘气具有的化学性质是___________ 。
(2)我国神舟十三号载人航天飞船使用的SiC颗粒增强铝基复合材料、超高强度钢等材料引起了全世界的关注。
①SiC俗名“金刚砂”,硬度非常大,有类似金刚石的结构,则构成SiC的粒子为___________ (填“原子”、“离子”或“分子”)。
②如果要比较超高强度钢材料中锰(Mn)和铁的金属活动顺序,以下方法不能达到目的的是___________ (填序号)。
A.查阅九年级化学课本上的金属活动性顺序表
B.利用金属锰和FeSO4溶液进行实验
C.利用金属铁和MnSO4溶液进行实验
D.利用锰、铁与稀硫酸进行实验
(1)我国科研人员自主设计的“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
| 原子种类 | 质子数 | 中子数 | 核外电子数 |
| 氘 | 1 | 1 | 1 |
| 氚 | 1 | 2 | 1 |
②贮存氘气的钢瓶禁止靠近明火,据此推测氘气具有的化学性质是
(2)我国神舟十三号载人航天飞船使用的SiC颗粒增强铝基复合材料、超高强度钢等材料引起了全世界的关注。
①SiC俗名“金刚砂”,硬度非常大,有类似金刚石的结构,则构成SiC的粒子为
②如果要比较超高强度钢材料中锰(Mn)和铁的金属活动顺序,以下方法不能达到目的的是
A.查阅九年级化学课本上的金属活动性顺序表
B.利用金属锰和FeSO4溶液进行实验
C.利用金属铁和MnSO4溶液进行实验
D.利用锰、铁与稀硫酸进行实验
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】用“化学的视角”认识身边的物质.
I.空气
(1)空气中含量最多的气体是____ .
(2)利用图 所示装置分别测得木炭磷充分燃烧过程中“压强-时间”关系如图2,其中P0是集气瓶内初始气压;P1和P2分别是反应结束后恢复到室温时两瓶内的气压.
所示装置分别测得木炭磷充分燃烧过程中“压强-时间”关系如图2,其中P0是集气瓶内初始气压;P1和P2分别是反应结束后恢复到室温时两瓶内的气压.
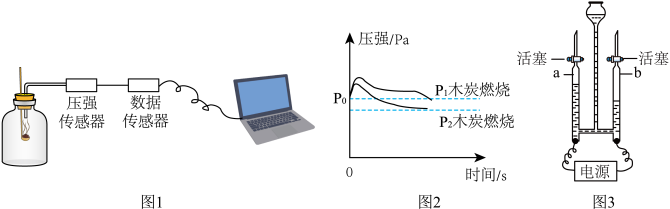
①反应开始时,两个集气瓶中压强都瞬间变大的原因是_____ .
②下列关于该实验的说法正确的有______ (填标号).
A红磷或木炭的用量多少对实验测定结果均没有影响
B实验测得P1=P0,说明木炭在氧气中燃烧只生成二氧化碳
C实验测得P2˂P0,原因是反应生成物状态为固态
D利用图2中的两个实验结果均可推算出空气中氧气的含量
II.水
(3)下列“水”属于纯净物的是_____ (填标号).
A蒸馏水B矿泉水C自来水
(4)用图3装置进行电解水的实验.
①与b管中相连接的是电源_____ (填“正”或“负”)极.该实验过程中,不发生变化的微粒是 ____ (填标号).
A H2O B H2和O2C H和O
②在电解水过程中,图4所示关系正确的是_____ (填标号).
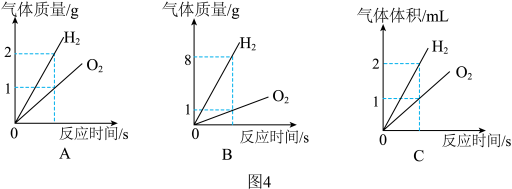
(5)据报道,科学家已发现一种新型复合催化剂可高效分解水,有望克服利用水制氢气的高成本难题.该反应的化学方程式为_____ .
III.金属
(6)下列与金属相关的说法正确的是_____ (填标号).
A常温下所有金属均为固态
B不锈钢的抗腐蚀性强于纯铁,硬度小于纯铁
C生铁和钢都是铁的合金,性能不同的原因是二者含碳量不同
(7)往含有硫酸铜的工业废液中加入铁粉可以回收铜,写出反应的化学方程式_____ .
(8)铁粉用于食品保鲜时常被称为“双吸剂”,原因是其发生缓慢氧化时,可同时吸收食品包装盒内的_____ ,从而达到保鲜效果.
I.空气
(1)空气中含量最多的气体是
(2)利用图
 所示装置分别测得木炭磷充分燃烧过程中“压强-时间”关系如图2,其中P0是集气瓶内初始气压;P1和P2分别是反应结束后恢复到室温时两瓶内的气压.
所示装置分别测得木炭磷充分燃烧过程中“压强-时间”关系如图2,其中P0是集气瓶内初始气压;P1和P2分别是反应结束后恢复到室温时两瓶内的气压.
①反应开始时,两个集气瓶中压强都瞬间变大的原因是
②下列关于该实验的说法正确的有
A红磷或木炭的用量多少对实验测定结果均没有影响
B实验测得P1=P0,说明木炭在氧气中燃烧只生成二氧化碳
C实验测得P2˂P0,原因是反应生成物状态为固态
D利用图2中的两个实验结果均可推算出空气中氧气的含量
II.水
(3)下列“水”属于纯净物的是
A蒸馏水B矿泉水C自来水
(4)用图3装置进行电解水的实验.
①与b管中相连接的是电源
A H2O B H2和O2C H和O
②在电解水过程中,图4所示关系正确的是

(5)据报道,科学家已发现一种新型复合催化剂可高效分解水,有望克服利用水制氢气的高成本难题.该反应的化学方程式为
III.金属
(6)下列与金属相关的说法正确的是
A常温下所有金属均为固态
B不锈钢的抗腐蚀性强于纯铁,硬度小于纯铁
C生铁和钢都是铁的合金,性能不同的原因是二者含碳量不同
(7)往含有硫酸铜的工业废液中加入铁粉可以回收铜,写出反应的化学方程式
(8)铁粉用于食品保鲜时常被称为“双吸剂”,原因是其发生缓慢氧化时,可同时吸收食品包装盒内的
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学就在我们身边,与我们的生活息息相关。
Ⅰ、根据①氦气②氢气③铜丝④氧气等物质的性质或用途,填写下列空格(填序号):
(1)密度最小的气体是______ ;
(2)医疗急救时用到的气体是______ ;
(3)可填充霓虹灯且通电时会发出有色光的气体是______ ;
(4)能用于导线的是______ 。
Ⅱ、空气是一种重要的资源。
(5)氮气是空气中含量最多的气体。食品包装袋中常充氮气以防腐,所利用的氮气的性质是______ 。
(6)氧气是比较活泼的气体。氧家族的“生长树”如图所示。

①树上的果子中,属于空气污染物的是______ 。
②树上有种“果子”为黑色固体,写出由单质生成该“果子”的化学反应的文字表达式:______ 。
(7)装有空气的密闭容器,欲用燃烧的方法除去其中的氧气,又不混入其它气体,可以使用的燃烧物是______(填字母)。
Ⅰ、根据①氦气②氢气③铜丝④氧气等物质的性质或用途,填写下列空格(填序号):
(1)密度最小的气体是
(2)医疗急救时用到的气体是
(3)可填充霓虹灯且通电时会发出有色光的气体是
(4)能用于导线的是
Ⅱ、空气是一种重要的资源。
(5)氮气是空气中含量最多的气体。食品包装袋中常充氮气以防腐,所利用的氮气的性质是
(6)氧气是比较活泼的气体。氧家族的“生长树”如图所示。

①树上的果子中,属于空气污染物的是
②树上有种“果子”为黑色固体,写出由单质生成该“果子”的化学反应的文字表达式:
(7)装有空气的密闭容器,欲用燃烧的方法除去其中的氧气,又不混入其它气体,可以使用的燃烧物是______(填字母)。
| A.木炭 | B.硫 | C.红磷 | D.蜡烛 | E.铁丝 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐3】化学实验是进行科学探究的重要手段。请填写下列空格:
(1)黄铜是铜锌合金,将外形完全相同的纯铜片和黄铜片相互刻划,该实验的目的是比较它们的______ 大小。
(2)用坩埚钳夹取一小块木炭,在酒精灯上加热至燃烧,然后将木炭插入盛有氧气的集气瓶内,观察现象。 据此可知,可燃物燃烧的剧烈程度与______ 有关。

(3) 用图 A 所示的装置可测定空气中氧气的含量。 该实验的原理是通过________ (选填“ 化学” 或“ 物理”)方法分离或除去混合物中的一种成分,从而测定混合物中某成分的含量。
(4)用图B 所示的装置探究酸碱中和反应。将稀盐酸滴入氢氧化钠溶液(滴有酚酞试液) 中至过量,观察到的现象是________ 。从微观角度分析,中和反应的实质是________ 。 请另外写出一个符合上述反应实质的化学方程式________ 。
(1)黄铜是铜锌合金,将外形完全相同的纯铜片和黄铜片相互刻划,该实验的目的是比较它们的
(2)用坩埚钳夹取一小块木炭,在酒精灯上加热至燃烧,然后将木炭插入盛有氧气的集气瓶内,观察现象。 据此可知,可燃物燃烧的剧烈程度与

(3) 用图 A 所示的装置可测定空气中氧气的含量。 该实验的原理是通过
(4)用图B 所示的装置探究酸碱中和反应。将稀盐酸滴入氢氧化钠溶液(滴有酚酞试液) 中至过量,观察到的现象是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】空气是宝贵的自然资源,化学小组以“探究空气的奥秘”为主题开展项目式学习。
【任务一】认识空气的组成
(1)二百多年前,拉瓦锡用汞定量研究了空气的成分,选择汞的理由是______;
(2)化学课上,老师用红磷燃烧法测定空气中氧气的含量(如图)

①红磷燃烧的文字或符号表达式______ ;
②红磷熄灭并冷却后,打开弹簧夹的现象是______ ;
③若造成实验结果出现明显偏差,其原因有______ (填序号)。
A.装置漏气
B.红磷较多
C.没有冷却就打开弹簧夹
D.燃着的红磷缓慢伸入集气瓶
(3)现代化学中,可利用图1装置(红磷燃烧)结合传感器精准地测定空气中氧气的含量,同时实验过程中可得知集气瓶内气体温度和压强的变化趋势,如图2所示:


①按照正确操作进行实验,反应刚开始,集气瓶内压强升高的原因是______ ;
②图2中,a点处压强突然增大,导致“压强突然增大”的操作是______ 。
【任务二】保护空气
(4)请写出一种空气污染物______ ;
(5)图3是某地PM2.5来源分布图,下列措施有利于降低PM2.5的是______。
【任务一】认识空气的组成
(1)二百多年前,拉瓦锡用汞定量研究了空气的成分,选择汞的理由是______;
| A.生成物氧化汞是固体 | B.不和空气中的其他物质发生反应 |
| C.汞蒸气有毒 | D.能将密闭装置内空气中的氧气几乎耗尽 |
(2)化学课上,老师用红磷燃烧法测定空气中氧气的含量(如图)

①红磷燃烧的文字或符号表达式
②红磷熄灭并冷却后,打开弹簧夹的现象是
③若造成实验结果出现明显偏差,其原因有
A.装置漏气
B.红磷较多
C.没有冷却就打开弹簧夹
D.燃着的红磷缓慢伸入集气瓶
(3)现代化学中,可利用图1装置(红磷燃烧)结合传感器精准地测定空气中氧气的含量,同时实验过程中可得知集气瓶内气体温度和压强的变化趋势,如图2所示:


①按照正确操作进行实验,反应刚开始,集气瓶内压强升高的原因是
②图2中,a点处压强突然增大,导致“压强突然增大”的操作是
【任务二】保护空气
(4)请写出一种空气污染物
(5)图3是某地PM2.5来源分布图,下列措施有利于降低PM2.5的是______。
| A.减少私家车的使用,积极倡导绿色出行 |
| B.用风能与太阳能发电替代燃煤发电 |
| C.工业生产的废气直接排放到空气中 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验回答:

(1)A实验,“用凸透镜聚光引燃红磷”测定空气中氧气含量,其优点是______ 。
(2)B实验中,若玻璃片用水洗后没擦于,会导致待测的稀硫酸pH的数值______ 。
(3)C实验,电解水的实验得出的结论是______ 。
(4)由D实验中的对比可知,铁生锈的条件之一是______ 。

(1)A实验,“用凸透镜聚光引燃红磷”测定空气中氧气含量,其优点是
(2)B实验中,若玻璃片用水洗后没擦于,会导致待测的稀硫酸pH的数值
(3)C实验,电解水的实验得出的结论是
(4)由D实验中的对比可知,铁生锈的条件之一是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】2015年冬,扬州迎来有史以来最冷的天气。
(1)由于积雪严重,工人沿路撒融雪剂,原理___________ ;
(2)城内大多户都出现自来水龙头冻坏,常用的铁制水龙头属于____________ 材料,为防止其生锈,常在表面镀一活泼性比其强的金属____________ (填字母);
A.Cu B.Zn C.Ag
(3)家长们纷纷购买暖宝宝,其中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见如图)。

①以下对此改进实验的叙述,正确的是__________ (填字母);
A.此实验中发热剂的多少不影响测量结果
B.氯化钠的作用是加快铁生锈
C.此实验测出氧气的体积分数比实际小
②暖宝宝使用时是___________ 能转化为___________ 能,该过程是铁粉、空气和水相互作用,最终转化为氢氧化铁,请写出该反应的化学方程式____________________ ,属于___________ 反应。
(1)由于积雪严重,工人沿路撒融雪剂,原理
(2)城内大多户都出现自来水龙头冻坏,常用的铁制水龙头属于
A.Cu B.Zn C.Ag
(3)家长们纷纷购买暖宝宝,其中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见如图)。

①以下对此改进实验的叙述,正确的是
A.此实验中发热剂的多少不影响测量结果
B.氯化钠的作用是加快铁生锈
C.此实验测出氧气的体积分数比实际小
②暖宝宝使用时是
您最近一年使用:0次
【推荐1】根据图示及所学知识回答下列问题:
(1)图一实验中的药品俗称为①___________ ,该药品是②___________ 色的固体。
(2)图二用于潜水的氧气的化学符号是___________ 。
(3)用酒精灯加热时应该使用___________ 。(选图中的某层火焰名称)
(4)图四中仪器A的名称是①___________ 图示收集气体的方法是②___________ 。
 |  |  |  |
| 图一 | 图二 | 图三 | 图四 |
(1)图一实验中的药品俗称为①
(2)图二用于潜水的氧气的化学符号是
(3)用酒精灯加热时应该使用
(4)图四中仪器A的名称是①
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】阅读下面的科普短文
空气质量与氮氧化物有着密切的关系。一氧化氮和二氧化氮是两种重要的氮氧化物。一氧化氮(化学式为NO)是一种无色气体,熔点-163.6℃,沸点-151℃,密度比空气略大,微溶于水。NO不稳定,易与空气中氧气发生反应,生成红棕色有刺激性气味的二氧化氮(NO2)。
实验室用铜与稀硝酸反应来制备NO。工业上可用氨气与氧气为原料,在加热和催化剂条件下制得一氧化氮。
汽车尾气(含有CO与NO等物质)是城市空气的污染源,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO与NO反应,生成两种可参与大气生态环境循环的无毒气体。
NO被发现广泛分布于生物体内各组织中、1992年被美国Science杂志评选为“明星分子”。NO在心、脑血管调节等方面有着十分重要的生物学作用,是心脑血管的保护神。
依据文章内容,回答下列问题:
(1)NO的物理性质______ (任写一点)。
(2)NO不稳定的原因是______ (用反应的文字表达式表示)。
(3)NO可用______ 法收集。
(4)治理汽车尾气的方法是______ 。
(5)NO对人类有利的一面主要体现在______ 。
空气质量与氮氧化物有着密切的关系。一氧化氮和二氧化氮是两种重要的氮氧化物。一氧化氮(化学式为NO)是一种无色气体,熔点-163.6℃,沸点-151℃,密度比空气略大,微溶于水。NO不稳定,易与空气中氧气发生反应,生成红棕色有刺激性气味的二氧化氮(NO2)。
实验室用铜与稀硝酸反应来制备NO。工业上可用氨气与氧气为原料,在加热和催化剂条件下制得一氧化氮。
汽车尾气(含有CO与NO等物质)是城市空气的污染源,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO与NO反应,生成两种可参与大气生态环境循环的无毒气体。
NO被发现广泛分布于生物体内各组织中、1992年被美国Science杂志评选为“明星分子”。NO在心、脑血管调节等方面有着十分重要的生物学作用,是心脑血管的保护神。
依据文章内容,回答下列问题:
(1)NO的物理性质
(2)NO不稳定的原因是
(3)NO可用
(4)治理汽车尾气的方法是
(5)NO对人类有利的一面主要体现在
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】2011年云南曲靖的铬(Cr)污染事件,说明含铬废渣(废液)的随意排放对人类生存环境有极大的危害。电解法是处理铬污染的一种方法,其处理过程发生的反应可表示为:
6Fe+K2Cr2O7+H2SO4+17H2O = 6Fe(OH)3↓+2Cr(OH)3↓+6X+K2SO4
(1)K2Cr2O7中Cr元素的化合价为_____ 。
(2)物质X的化学式为_____ 。
(3)实验室收集X时,可用向下排空气法,则利用了X____ 的物理性质。
6Fe+K2Cr2O7+H2SO4+17H2O = 6Fe(OH)3↓+2Cr(OH)3↓+6X+K2SO4
(1)K2Cr2O7中Cr元素的化合价为
(2)物质X的化学式为
(3)实验室收集X时,可用向下排空气法,则利用了X
您最近一年使用:0次



