老师在实验室发现一种固体样品,是氯酸钾和氯化钾的混合物,为了测定该样品中氯酸钾和氯化钾的质量比,小松同学取100g固体样品,加入10g二氧化锰充分混合后,加热至固体质量不再改变,称得剩余固体质量为90.8g,根据以上信息帮助小松同学计算:
(1)发生反应的化学方程式是______ 。
(2)生成氧气的质量是______ 。
(3)根据数据列出求解100g固体样品中氯酸钾质量(x)的比例式______ 。
(4)固体样品中氯酸钾和氯化钾的质量比是______ 。
(1)发生反应的化学方程式是
(2)生成氧气的质量是
(3)根据数据列出求解100g固体样品中氯酸钾质量(x)的比例式
(4)固体样品中氯酸钾和氯化钾的质量比是
更新时间:2023-12-05 14:47:07
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】好奇的同学们为了探测鸡蛋壳中碳酸钙的含量,从家里收集了鸡蛋壳清洗干燥后带到学校实验室。取11g鸡蛋壳样品于烧杯中,加入稀盐酸至不再产生气泡(假设鸡蛋壳中其他成分不与稀盐酸反应,生成气体全部逸出),共加入稀盐酸100g,此时烧杯内混合物的质量为106.6g。请计算。
(1)生成二氧化碳的质量为_____ g。
(2)该鸡蛋壳中碳酸钙的质量分数。(结果保留到0.1%)
(1)生成二氧化碳的质量为
(2)该鸡蛋壳中碳酸钙的质量分数。(结果保留到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】碳酸钾可以从草木灰中提取,主要用于食品中作膨松剂。小芳同学研究反应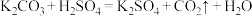 中K2CO3与CO2之间量的关系。
中K2CO3与CO2之间量的关系。
(1)理论计算:2.76 g K2CO3粉末与足量稀硫酸反应,计算生成CO2的质量。___________ (写出计算过程)。
(2)实验分析:小芳用如图装置进行实验,向盛有足量稀硫酸的锥形瓶中加入2.76 g K2CO3粉末,完全反应至不再产生气泡。称取反应前后质量如下表,发现反应前后质量变化值___________ (填“大于”、“小于”或“等于”)生成CO2质量的理论值,原因可能是___________ 。

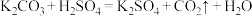 中K2CO3与CO2之间量的关系。
中K2CO3与CO2之间量的关系。(1)理论计算:2.76 g K2CO3粉末与足量稀硫酸反应,计算生成CO2的质量。
(2)实验分析:小芳用如图装置进行实验,向盛有足量稀硫酸的锥形瓶中加入2.76 g K2CO3粉末,完全反应至不再产生气泡。称取反应前后质量如下表,发现反应前后质量变化值

| 反应前 | 反应后 | |
| K2CO3/g | 锥形瓶+稀硫酸/g | 锥形瓶+反应后溶液/g |
| 2.76 | 124.59 | 126.53 |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】现有一份纯碱样品,其中只含有一种可溶性杂质。为了测定样品中纯碱的含量,做了如下的实验,请你回答下列问题:

(1)写出上述反应的化学方程式____________________________________ ;
(2)根据已知条件列出求解样品中纯碱的质量(x)比例式_____________________ ;
(3)样品中纯碱的质量分数为___________ ;
(4)若将反应后的滤液恒温蒸发掉123.5g水,则最终所得溶液中溶质的质量分数为____ ;
(5)加入氯化钙溶液的过程中溶液中溶质的质量变化情况为___________________________ ;
(6)若用上述纯碱样品265t制取烧碱,则可制得纯度为80%的烧碱_____ t。

(1)写出上述反应的化学方程式
(2)根据已知条件列出求解样品中纯碱的质量(x)比例式
(3)样品中纯碱的质量分数为
(4)若将反应后的滤液恒温蒸发掉123.5g水,则最终所得溶液中溶质的质量分数为
(5)加入氯化钙溶液的过程中溶液中溶质的质量变化情况为
(6)若用上述纯碱样品265t制取烧碱,则可制得纯度为80%的烧碱
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组同学想测定实验室制取二氧化碳的剩余固体混合物(其成分是不溶于水也不与水反应的杂质、碳酸钙和氯化钙)中碳酸钙的质量,做了如下实验:___________ 。
(2)根据已知条件列出反应生成氯化钙的质量(x)的比例式为___________ 。
(3)固体混合物中碳酸钙的质量是___________ 。
(4)若向滤液中加入___________ g水,可以使最终所得溶液溶质质量分数为10%;
(5)若按上述实验过程用该固体混合物522g,可以制得氯化钙___________ g。

(2)根据已知条件列出反应生成氯化钙的质量(x)的比例式为
(3)固体混合物中碳酸钙的质量是
(4)若向滤液中加入
(5)若按上述实验过程用该固体混合物522g,可以制得氯化钙
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】化学研究性学习小组同学取10g石灰石样品,用足量的稀盐酸测定石灰石中碳酸钙的质量分数(假设石灰石中杂质不与盐酸反应)。测量5分钟内生成CO2质量的数据如表:
请回答下列问题:
(1)石灰石中的CaCO3完全反应时,生成二氧化碳气体的质量是 g;
(2)该石灰石中CaCO3的质量分数是多少?(计算结果精确到0.1%)
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 生成CO2的质量/g | 1.5 | 2.5 | 3.0 | 3.3 | 3.3 |
(1)石灰石中的CaCO3完全反应时,生成二氧化碳气体的质量是 g;
(2)该石灰石中CaCO3的质量分数是多少?(计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】石灰石是生产水泥、玻璃等建筑材料的重要原料。我国石灰石资源富,某课外兴趣小组的同学为了测定某地石灰石中碳酸钙的质量分数,判断是否有开采使用价值。取一定样品于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后过滤得剩余固体的质量如下表:(杂质不溶于水且不与稀盐酸反应)
请完成下列问题:
(1)表中X的值______ ,过滤操作中用到的玻璃仪器有______ 。
(2)该石灰石样品中碳酸钙的质量分数是______ 。
(3)实验中共产生二氧化碳多少克。______ (写出计算过程)
(4)实验中,稀盐酸与碳酸钙恰好完全反应时的质量比为______ 。
加入稀盐酸质量/g | 10 | 10 | 10 | 10 | 10 |
剩余固体质量/g | X | 2.0 | 1.0 | 0.5 | 0.5 |
请完成下列问题:
(1)表中X的值
(2)该石灰石样品中碳酸钙的质量分数是
(3)实验中共产生二氧化碳多少克。
(4)实验中,稀盐酸与碳酸钙恰好完全反应时的质量比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】侯氏制碱法生产的碳酸钠中常含有少量的氯化钠。现有碳酸钠和氯化钠的混合物样品12.5g,将其放入干净的烧杯中,加入100g水,使其完全溶解。向所得溶液中加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与加入稀盐酸的质量关系曲线如图所示。请回答下列问题:
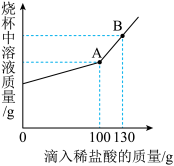
(1)通过已有数据,能求出的量有______ 。
①混合样品中,碳酸钠的质量
②混合样品中,氯化钠的质量分数
③B点时,溶液的总质量
(2)A点时,求此温度下所得不饱和溶液中溶质质量分数______ (写出具体计算过程,计算结果精确至0.1%)。

(1)通过已有数据,能求出的量有
①混合样品中,碳酸钠的质量
②混合样品中,氯化钠的质量分数
③B点时,溶液的总质量
(2)A点时,求此温度下所得不饱和溶液中溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某同学取一定质量的氯酸钾和二氧化锰加热,记录产生氧气的质量与反应时间的关系如图所示,请回答下列问题:

(1)t3时,产生氧气的质量是______;试管内固体的成分是______。
(2)______时,氯酸钾恰好完成分解,一共产生了______氧气。
(3)计算原混合物中氯酸钾的质量(写出计算过程,结果准确到0.1g)

(1)t3时,产生氧气的质量是______;试管内固体的成分是______。
(2)______时,氯酸钾恰好完成分解,一共产生了______氧气。
(3)计算原混合物中氯酸钾的质量(写出计算过程,结果准确到0.1g)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】化学兴趣小组的同学用一定量的氯酸钾和二氧化锰0.5g的混合物加热制取氧气,测得反应过程产生的气体质量与加热时间关系如图所示。请计算:

(1)氯酸钾相对分子质量为:_______ 。
(2)氯酸钾中钾、氯、氧原子的个数比为:_______ 。
(3)0-t1时间段为什么产生的氧气质量是不变的?_______ 。
(4)从图中可知,反应过程产生的氧气质量_______ g。
(5)求一定量的氯酸钾是多少?(写出计算过程)

(1)氯酸钾相对分子质量为:
(2)氯酸钾中钾、氯、氧原子的个数比为:
(3)0-t1时间段为什么产生的氧气质量是不变的?
(4)从图中可知,反应过程产生的氧气质量
(5)求一定量的氯酸钾是多少?(写出计算过程)
您最近一年使用:0次



