实验室有一份在空气中潮解部分变质的氢氧化钠样品,质量为1.86g。某实验小组将这份样品完全溶解,配成 50g 溶液,然后缓慢滴入 7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液 pH 和溶液总质量,部分数据如下表所示:
请分析计算:
(1)实验中生成二氧化碳的质量为_______ g。
(2)求样品中氢氧化钠的质量(请写出计算过程)。
(3)请在下图中画出稀盐酸质量与二氧化碳质量关系的图像(标出关键点的数据)。
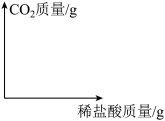
(4)当恰好完全反应时,该溶液的溶质质量分数是____ 。(结果保留两位小数)。
| 测量次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 | 第 5 次 |
| 滴加的盐酸总质量/g | 0 | 5 | 20 | 30 | 35 |
| 溶液总质量/g | 50 | 55 | 69.56 | 79.56 | 84.56 |
| 溶液 pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
(1)实验中生成二氧化碳的质量为
(2)求样品中氢氧化钠的质量(请写出计算过程)。
(3)请在下图中画出稀盐酸质量与二氧化碳质量关系的图像(标出关键点的数据)。

(4)当恰好完全反应时,该溶液的溶质质量分数是
2021·广东·一模 查看更多[1]
更新时间:2023-12-08 21:13:12
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】为了测定石灰石样品中钙元素的质量分数(杂质不含钙元素,不溶于水,也不与其他物质发生反应),进行了如下实验:请回答下列问题:

(1)写出上述实验中发生反应的化学方程式为______ ;
(2)根据稀盐酸中氯化氢的质量列出求解石灰石样品中碳酸钙质量(x)的比例式为______ ;
(3)该石灰石样品中钙元素的质量分数是______ ;
(4)配制实验中所需要稀盐酸,需要质量分数为36.5%的浓盐酸的质量是______ ;
(5)最后得到固体纯净物的名称和质量分别是______ ;
(6)某工厂要想制得140t的氧化钙,理论上需要这种石灰石的质量为______ 。

(1)写出上述实验中发生反应的化学方程式为
(2)根据稀盐酸中氯化氢的质量列出求解石灰石样品中碳酸钙质量(x)的比例式为
(3)该石灰石样品中钙元素的质量分数是
(4)配制实验中所需要稀盐酸,需要质量分数为36.5%的浓盐酸的质量是
(5)最后得到固体纯净物的名称和质量分别是
(6)某工厂要想制得140t的氧化钙,理论上需要这种石灰石的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】将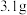 红磷分别在给定质量的氧气中充分反应,其实验数据如下:
红磷分别在给定质量的氧气中充分反应,其实验数据如下:
通过计算回答:
(1)这三次实验____(是、否)符合质量守恒定律,其原因是____。
(2)第一次实验为什么不生成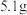 五氧化二磷,其原因是____。
五氧化二磷,其原因是____。
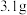 红磷分别在给定质量的氧气中充分反应,其实验数据如下:
红磷分别在给定质量的氧气中充分反应,其实验数据如下:| 第一次 | 第二次 | 第三次 | |
给定氧气的质量/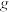 | 2 | 8 | 14 |
生成五氧化二磷的质量/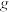 | 3.55 | 7.1 | 7.1 |
(1)这三次实验____(是、否)符合质量守恒定律,其原因是____。
(2)第一次实验为什么不生成
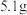 五氧化二磷,其原因是____。
五氧化二磷,其原因是____。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】为测定某化工厂排放的废水中CuSO4的含量,化学小组同学取150g废水,平均分为三份,每一份样品均按如图所示装置进行实验,实验数据记录如下表:

试分析并计算:
(1)50g废水完全反应时,所得沉淀的质量为____ g。
(2)计算该化工厂废水中CuSO4的质量分数_____ 。

| 实验1 | 实验2 | 实验3 | |
| 样品质量/g | 50 | 50 | 50 |
| NaOH溶液质量/g | 20 | 40 | 60 |
| m/g | 44.9 | 49.8 | 49.8 |
(1)50g废水完全反应时,所得沉淀的质量为
(2)计算该化工厂废水中CuSO4的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】为测定石灰石中碳酸钙的含量,取25g石灰石样品,与100g稀盐酸在烧杯中恰好完全反应(杂质不溶于水也不与酸反应),反应过程中数据变化情况如图所示,请回答回题:
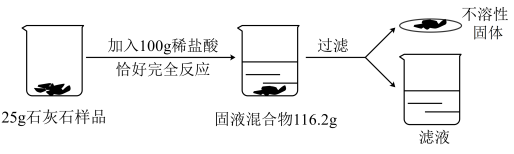
(1)发生反应的化学方程式为______ ;
(2)根据已知条件求解25g石灰石样品中碳酸钙质量(x)的比例式______ ;
(3)石灰石样品中碳酸钙的含量为______ ;
(4)若样品换成碳酸钠粉末,与上述稀盐酸反应生成等质量的二氧化碳,需要碳酸钠粉末的质量为______ ;
(5)用1000t该石灰石样品可制得含杂质的生石灰的质量为______ 。

(1)发生反应的化学方程式为
(2)根据已知条件求解25g石灰石样品中碳酸钙质量(x)的比例式
(3)石灰石样品中碳酸钙的含量为
(4)若样品换成碳酸钠粉末,与上述稀盐酸反应生成等质量的二氧化碳,需要碳酸钠粉末的质量为
(5)用1000t该石灰石样品可制得含杂质的生石灰的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
名校
【推荐2】为测定久置于空气中的氢氧化钠样品的变质程度,某化学活动小组称取该固体样品6.5g放入锥形瓶中,加水溶解,配成50g溶液,再向锥形瓶中滴加稀硫酸,反应过程中产生气体质量的部分实验数据和锥形瓶中溶液质量变化的图象如表所示:
(1)6.5g样品与稀硫酸完全反应产生气体的质量是________g。
(2)6.5g样品中碳酸钠的质量分数是________。(结果精确至0.1%)
(3)以上三次的实验数据中,只有一次加入的稀硫酸与锥形瓶中溶液的溶质恰好完全反应。
①如图图象中a的数值是________。

②求该实验中所用稀硫酸的溶质质量分数____。(写出计算过程)
| 加入稀硫酸的质量/g | 40 | 65 | 75 |
| 产生气体的质量/g | 1.1 | 2.2 | 2.2 |
(2)6.5g样品中碳酸钠的质量分数是________。(结果精确至0.1%)
(3)以上三次的实验数据中,只有一次加入的稀硫酸与锥形瓶中溶液的溶质恰好完全反应。
①如图图象中a的数值是________。

②求该实验中所用稀硫酸的溶质质量分数____。(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】为了确定 Na2CO3 和 NaHCO3 混合物样品的组成,称取四份该样品溶于水后分别滴加相同浓度盐酸 50.0g,充分反应,产生 CO2 的质量,如表:
已知 Na2CO3 和盐酸反应可分成以下两步: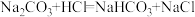 ,
, 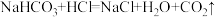
求:
(1)样品 Na2CO3 和 NaHCO3 的质量之比_____ ;
(2)盐酸的质量分数_____ 。
| 实验序号 | I | II | Ⅲ | IV |
| 盐酸质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 样品质量(g) | 2.96 | 3.70 | 5.18 | 6.66 |
| CO2的质量(g) | 1.32 | 1.65 | 1.76 | 1.32 |
已知 Na2CO3 和盐酸反应可分成以下两步:
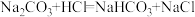 ,
, 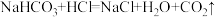
求:
(1)样品 Na2CO3 和 NaHCO3 的质量之比
(2)盐酸的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】将25.6 g NaCl和MgCl2固体混合物完全溶于126 g水中配成溶液,再将200 g一定溶质质量分数的NaOH溶液不断加入该溶液中。充分反应后,测得的实验数据如下表。求:
(1)上表中m的值为多少。___________
(2)恰好完全反应时,所得溶液中溶质的质量分数。___________
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 加入NaOH 溶液质量/g | 40 | 40 | 40 | 40 | 40 |
| 共生成沉 淀的质量/g | 2.9 | 5.8 | m | 11.6 | 11.6 |
(1)上表中m的值为多少。___________
(2)恰好完全反应时,所得溶液中溶质的质量分数。___________
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】某班同学在做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其它杂质)。为了对废液进行处理,某同学做了如下实验:取废液缸上层清液20.0g于烧杯中,逐滴滴入溶质质量分数为5.3%的碳酸钠溶液直至过量,滴入碳酸钠溶液的质量与生成沉淀的质量的变化关系如图所示。

请回答下列问题:
(1)当加入碳酸钠溶液20.0g时,溶液中的溶质为___________ ;
(2)当废液中盐酸完全反应时,生成的二氧化碳的质量为__________ ;
(3)实验过程中实际参加反应的碳酸钠溶液的质量为__________ ;
(4)当废液中两种物质刚好消耗完毕时,所得溶液中氯化钠的质量分数为_____________ 。(计算结果精确到0.1%)

请回答下列问题:
(1)当加入碳酸钠溶液20.0g时,溶液中的溶质为
(2)当废液中盐酸完全反应时,生成的二氧化碳的质量为
(3)实验过程中实际参加反应的碳酸钠溶液的质量为
(4)当废液中两种物质刚好消耗完毕时,所得溶液中氯化钠的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】小明用溶质质量分数为5%的过氧化氢溶液和二氧化锰的混合物制取氧气,若消耗6.8g该过氧化氢溶液,能生成氧气的质量是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某化工产品的成分是氯化钾和氢氧化钾的固体混合物。20℃时,在实验室里,甲、乙、丙三位同学分别取该固体样品放入锥形瓶中,然后再向锥形瓶中加入氯化铜溶液,振荡,充分反应后过滤,称量沉淀的质量。测得实验数据如下表:
请回答下列问题:
(1)表中m的数值为____ ;_____ 同学所做的实验中,反应物恰好完全反应。
(2)恰好完全反应时,计算所得溶液中溶质的质量分数____ 。
| 甲 | 乙 | 丙 | |
| 所取固体样品的质量/g | 20 | 20 | 30 |
| 加入氯化铜溶液的质量/g | 100 | 89.8 | 89.8 |
| 反应后生成沉淀的质量/g | 9.8 | m | 9.8 |
请回答下列问题:
(1)表中m的数值为
(2)恰好完全反应时,计算所得溶液中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】为测定某铜锌合金的成分含量进行了如下实验:将320.0g20.0%的硫酸铜溶液分成四等份,逐次加入至50.3g的合金粉末中,充分反应后得到如下数据。
(1)第______次加入硫酸铜溶液时反应恰好完全,此时消耗的硫酸铜溶液总质量为______g。
(2)计算合金粉末中金属锌的质量分数(结果精确至0.1%)。
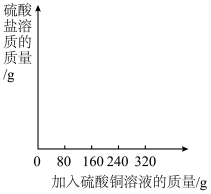
(3)在下图中画出加入硫酸铜溶液质量0~320.0g过程中,溶液中硫酸盐溶质的总质量对应的变化图,并标注必要的数值。
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入硫酸铜溶液的质量/g | 80.0 | 80.0 | 80.0 | 80.0 |
| 剩余固体的质量/g | 50.2 | 50.1 | 50.0 | 50.0 |
(2)计算合金粉末中金属锌的质量分数(结果精确至0.1%)。
(3)在下图中画出加入硫酸铜溶液质量0~320.0g过程中,溶液中硫酸盐溶质的总质量对应的变化图,并标注必要的数值。
您最近一年使用:0次




