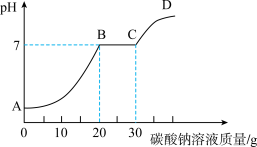
默默同学为测定一定质量的过氧化氢溶液中溶质的质量,进行实验,测得相关数据如下图:

请根据要求回答问题:
(1)发生反应的化学方程式是___________ ;
(2)反应生成的氧气的质量为___________ g;
(3)根据氧气的质量求解参加反应的过氧化氢质量(X)的比例式为___________ ;
(4)该过氧化氢溶液中水的质量为___________ g。

请根据要求回答问题:
(1)发生反应的化学方程式是
(2)反应生成的氧气的质量为
(3)根据氧气的质量求解参加反应的过氧化氢质量(X)的比例式为
(4)该过氧化氢溶液中水的质量为
更新时间:2024-01-16 20:42:00
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在实验室中可以用加热KClO3和MnO2固体混合物的方法制取氧气,MnO2在反应中起到了催化作用,反应生成了氯化钾和氧气。反应过程中固体质量发生变化如图所示,请计算:
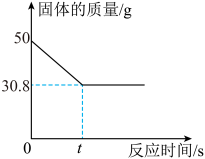
(1)制取O2的质量是_______g。
(2)原混合物中KClO3的质量(写出计算过程)。

(1)制取O2的质量是_______g。
(2)原混合物中KClO3的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组用大理石与稀盐酸反应制取二氧化碳:取15g大理石于烧杯中,逐渐加入稀盐酸(杂质难溶于水,且不与酸反应),充分反应,实验数据如图。
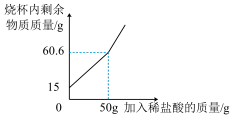
(1)15g大理石完金反应时生成二氧化碳的质量为______ g。
(2)计算该大理石中碳酸钙的质量分数。(写出计算过程,结果精确到0.1%)

(1)15g大理石完金反应时生成二氧化碳的质量为
(2)计算该大理石中碳酸钙的质量分数。(写出计算过程,结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室利用下图装置及仪器制取氧气。___________ (填仪器名称)才能进行实验,该反应的化学方程式为___________ ;
(2)若实验中消耗氯酸钾0.02mol,理论上可制得氧气_______ g;

(2)若实验中消耗氯酸钾0.02mol,理论上可制得氧气
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学储氢材料研发是当下科技研究的热点之一。
(1)下列化学储氢材料中含氢量(氢的质量分数)最高的是______。
(2)我国科学家发明了一种将甲烷中的氢转化为氢气的工艺(原理如图所示)。

总反应的化学反应方程式为CH4+H2O=CO+3H2
①反应器I中的化学反应方程式为______ 。
②计算:理论上0.8t甲烷与足量水蒸气反应生成氢气的总质量是多少?
(1)下列化学储氢材料中含氢量(氢的质量分数)最高的是______。
| A.NH3 | B.N2H4 | C.CH4 |
(2)我国科学家发明了一种将甲烷中的氢转化为氢气的工艺(原理如图所示)。

总反应的化学反应方程式为CH4+H2O=CO+3H2
①反应器I中的化学反应方程式为
②计算:理论上0.8t甲烷与足量水蒸气反应生成氢气的总质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】下图是实验室中一瓶过氧化氢溶液的标签。某同学为了测定该溶液中溶质的质量分数是否与标签上相符,用烧杯取该溶液50g,加入二氧化锰1g,完全反应后,称得烧杯内剩余物的总质量为49.4g。请回答下列问题:

(1)二氧化锰在反应中的作用是_______
(2)完全反应后生成氧气的质量为_______
(3)通过计算回答,该过氧化氢溶液中的溶质质量分数(已知质量分数=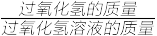 ×100%)是否与标签上相符?
×100%)是否与标签上相符?

(1)二氧化锰在反应中的作用是_______
(2)完全反应后生成氧气的质量为_______
(3)通过计算回答,该过氧化氢溶液中的溶质质量分数(已知质量分数=
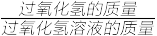 ×100%)是否与标签上相符?
×100%)是否与标签上相符?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验小组的同学在用二氧化锰做催化剂制氧气的实验过程中遇到困惑,通过老师讲解,他们厘清了思路,找到了解决问题的办法,小丽同学将图像绘在黑板上,并将方法分享给其他同学。

(1)最终瓶内气压相同,原因是_______ 。
(2)写出计算过程(最后结果精确到0.01)。

(1)最终瓶内气压相同,原因是
(2)写出计算过程(最后结果精确到0.01)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】100g某硫酸恰好与13g锌完全起反应,试计算:
(1)生成氢气的质量;
(2)该硫酸中溶质的质量分数;
(3)反应后所得溶液中溶质的质量分数(保留到0.1%).
(1)生成氢气的质量;
(2)该硫酸中溶质的质量分数;
(3)反应后所得溶液中溶质的质量分数(保留到0.1%).
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】向133.4克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示。

求:
(1)此过程产生气体的最大质量是______ g;
(2)原稀盐酸中溶质的质量为多少?(请写出计算过程)

求:
(1)此过程产生气体的最大质量是
(2)原稀盐酸中溶质的质量为多少?(请写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐3】小明同学将13.9g含杂质的的纯碱样品(碳酸钠与氯化钠的混合物)与90.5g稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为_______ g
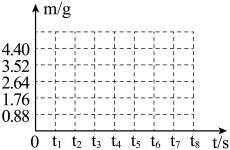
(2)请在下面的坐标图中,画出反应时生成气体的质量(m)随时间(t)变化的曲线。
(3)求完全反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl=2NaCl+CO2↑+H2O)。
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
(1)碳酸钠完全反应后,生成CO2的质量为
(2)请在下面的坐标图中,画出反应时生成气体的质量(m)随时间(t)变化的曲线。

(3)求完全反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl=2NaCl+CO2↑+H2O)。
您最近一年使用:0次