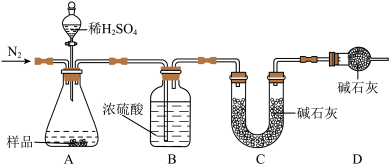
氯化镁,化学式MgCl2,可由海水中提取,氯化镁可用于融雪剂、控制灰尘、用于储藏、用于消防器材、储存氢气等。
(1)①氯化镁易潮解,易溶于水,在储藏的时候要注意存放在干燥阴凉的地方。
②海水中原本就有氯化镁,为什么要先加石灰乳生成氢氧化镁沉淀,再加盐酸得到氯化镁,原因是______ 。
③电解熔融状态氯化镁制取金属镁,是将电能转化为______ ,反应的化学方程式为______ 。
(2)测定某氯化镁溶液中 MgCl2的质量分数。小明同学取 100g 某氯化镁溶液于一只洁净的烧杯中,然后逐滴加入溶质质量分数为 10%的 NaOH 溶液至过量,烧杯内溶液的质量与加入 NaOH 溶液的质量关系如图所示。试回答:______ (填离子符号)。
② 当滴入10%的 NaOH 溶液 80g 时(即B 点)恰好完全反应,试通过计算,求该氯化镁溶液的溶质质量分数。______ (计算结果精确至 0.1%)。
(1)①氯化镁易潮解,易溶于水,在储藏的时候要注意存放在干燥阴凉的地方。
②海水中原本就有氯化镁,为什么要先加石灰乳生成氢氧化镁沉淀,再加盐酸得到氯化镁,原因是
③电解熔融状态氯化镁制取金属镁,是将电能转化为
(2)测定某氯化镁溶液中 MgCl2的质量分数。小明同学取 100g 某氯化镁溶液于一只洁净的烧杯中,然后逐滴加入溶质质量分数为 10%的 NaOH 溶液至过量,烧杯内溶液的质量与加入 NaOH 溶液的质量关系如图所示。试回答:
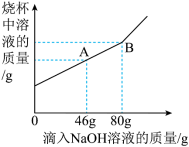
② 当滴入10%的 NaOH 溶液 80g 时(即B 点)恰好完全反应,试通过计算,求该氯化镁溶液的溶质质量分数。
2024·山东济南·一模 查看更多[3]
更新时间:2024-01-19 14:32:35
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某碳酸钠样品中含有杂质NaCl,化学兴趣小组的同学的进行了如下实验探究:称取25g样品放入烧杯中,加入稀盐酸至不再产生气泡为止,加入稀盐酸的质量与生成气体质量的关系如下图:_______ g。
(2)所用稀盐酸中溶质的质量分数是多少?
(3)计算当盐酸与碳酸钠恰好完全反应时,所得溶液中溶质的质量分数是多少?(结果保留到0.1%)
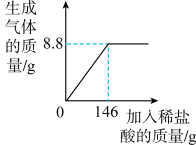
(2)所用稀盐酸中溶质的质量分数是多少?
(3)计算当盐酸与碳酸钠恰好完全反应时,所得溶液中溶质的质量分数是多少?(结果保留到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎放在烧杯中,然后向其中滴加某浓度的稀盐酸滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算:

(1)产生CO2的质量为 g。
(2)该鸡蛋壳中CaCO3的质量分数;
(3)所用稀盐酸溶质的质量分数。

(1)产生CO2的质量为 g。
(2)该鸡蛋壳中CaCO3的质量分数;
(3)所用稀盐酸溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】兴趣小组的同学对石灰石和稀盐酸制取二氧化碳后的废液(石灰石中的杂质不溶于水,也不与盐酸反应)开展了如下探究,向100g废液中逐渐加入碳酸钠溶液,加入碳酸钠溶液的质量与产生沉淀的质量如下表所示,请你回答:
(1)
______ 。
(2)计算原废液中氯化钙的质量。(写出计算过程,下同)
(3)计算碳酸钠溶液的溶质质量分数。(精确至0.1%)
| 加入碳酸钠溶液的质量/g | 100 | 200 | 250 | 280 |
| 产生沉淀的质量/g | 2.5 | 7.5 | n | 10 |

(2)计算原废液中氯化钙的质量。(写出计算过程,下同)
(3)计算碳酸钠溶液的溶质质量分数。(精确至0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某化学兴趣小组称取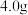 石灰石样品,把
石灰石样品,把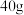 稀盐酸分
稀盐酸分 次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
请计算:
(1)石灰石样品中碳酸钙的质量分数是多少。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到 )。
)。
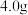 石灰石样品,把
石灰石样品,把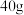 稀盐酸分
稀盐酸分 次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
次加入样品中(假设杂质不反应也不溶解),得实验数据如下:| 稀盐酸的用量 | 剩余固体的质量 |
第一次加入 | 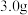 |
第二次加入 |  |
第三次加入 | 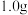 |
第四次加入 |  |
(1)石灰石样品中碳酸钙的质量分数是多少。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到
 )。
)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】BaCl2是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl2溶液可立即服用MgSO4溶液解毒。为测定某BaCl2溶液的溶质质量分数,现取100 g 该BaCl2溶液,不断加入MgSO4溶液至恰好完全反应,此时用去MgSO4溶液的质量为100 g,反应后所得溶液的质量为176.7g。请回答:
(1)反应后所得溶液中的溶质是______(填化学式);
(2)计算原BaCl2溶液的溶质质量分数(保留到0.1%)。
(1)反应后所得溶液中的溶质是______(填化学式);
(2)计算原BaCl2溶液的溶质质量分数(保留到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】电动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用。电瓶的正极材料是二氧化铅(PbO2),负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下: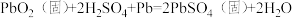 。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
(1)电瓶在放电时,____________能转化为电能。
(2)假如某个电瓶中铅的质量为1800g,请计算:当有621g铅参加反应时,理论上需消耗硫酸的质量(要求写出计算过程)。
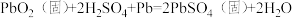 。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。(1)电瓶在放电时,____________能转化为电能。
(2)假如某个电瓶中铅的质量为1800g,请计算:当有621g铅参加反应时,理论上需消耗硫酸的质量(要求写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】2023年5月30日,神舟十六号载人飞船发射取得圆满成功,发射时火箭所用的液体燃料为偏二甲肼(C2H8N2)与四氧化二氮(N2O4)
(1)二者发生反应的化学方程式为:C2H8N2+2N2O4=3N2+2CO2+4H2O。计算12kg的C2H8N2与足量的N2O4反应生成CO2的质量。
(2)已知植物光合作用,每吸收44gCO2,需要吸收的能量约为470kJ,则吸收上述反应生成的CO2,需要吸收的能量约为______ kJ。
(1)二者发生反应的化学方程式为:C2H8N2+2N2O4=3N2+2CO2+4H2O。计算12kg的C2H8N2与足量的N2O4反应生成CO2的质量。
(2)已知植物光合作用,每吸收44gCO2,需要吸收的能量约为470kJ,则吸收上述反应生成的CO2,需要吸收的能量约为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】动自行车、小汽车等交通工具中都有为其提供电能的铅蓄电池(又称“电瓶”),它的优点是可以充电循环使用。电瓶的正极材料是二氧化铅(PbO2),负极材料是金属铅(Pb),电瓶内所加液体是溶质质量分数为36%的稀硫酸,放电(为外界供电)时发生反应的化学方程式如下:PbO2(固)+2H2SO4+Pb=2PbSO4(固)+2H2O。当放电时,反应物反应掉一定量后,就会导致电压下降,不能正常使用,这时就必须及时充电。
(1)电瓶在放电时,_________能转化为电能。
(2)假如某个电瓶中铅的质量为1800 g,内装36%的稀硫酸1200 g,当有310.5 g的铅参加反应时,需消耗稀硫酸中溶质_____克?此时电瓶中硫酸溶液溶质的质量分数是_____?(最后结果精确到0. 01%)
(1)电瓶在放电时,_________能转化为电能。
(2)假如某个电瓶中铅的质量为1800 g,内装36%的稀硫酸1200 g,当有310.5 g的铅参加反应时,需消耗稀硫酸中溶质_____克?此时电瓶中硫酸溶液溶质的质量分数是_____?(最后结果精确到0. 01%)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】海洋是巨大的资源宝库,人类在运用多种方法合理开发的同时,应保护好海洋环境。镁元素广泛应用于火箭、导弹和飞机制造业,被称为“国防元素”,它在海水中的质量分数约为0.13%,海水提镁的工艺流程如图所示:

上述转化过程中发生的化学反应主要有:
①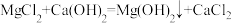
②
③
根据上述信息,试回答:
(1)海水或卤水中本来就含有氯化镁,工业生产需要过程①②的原因是______(填序号之一)。
(2)某化学小组欲测定某氯化镁样品中MgCl2的含量(杂质仅为NaCl),先称取该样品10.0g,将其置于洁净烧杯中,再加入适量水,使固体样品完全溶解,然后向所得溶液中逐滴加入溶质质量分数为8%的NaOH溶液,生成沉淀的质量与滴入NaOH溶液的质量关系如图所示:
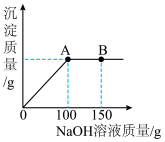
试回答下列问题:
①当滴入8%的NaOH溶液150g时(即图中B点),烧杯内溶液中的溶质为(写化学式)______ 。
②当滴入8%的NaOH溶液100g时(即图中A点),恰好完全反应,试通过计算,求该实验样品中所含MgCl2的质量。______ (根据化学方程式计算写出完整的计算步骤,结果精确至0.1g)

上述转化过程中发生的化学反应主要有:
①
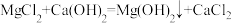
②

③

根据上述信息,试回答:
(1)海水或卤水中本来就含有氯化镁,工业生产需要过程①②的原因是______(填序号之一)。
| A.将氯化镁富集提纯 | B.生成更多氯化镁 | C.使石灰乳和稀盐酸反应 |
(2)某化学小组欲测定某氯化镁样品中MgCl2的含量(杂质仅为NaCl),先称取该样品10.0g,将其置于洁净烧杯中,再加入适量水,使固体样品完全溶解,然后向所得溶液中逐滴加入溶质质量分数为8%的NaOH溶液,生成沉淀的质量与滴入NaOH溶液的质量关系如图所示:

试回答下列问题:
①当滴入8%的NaOH溶液150g时(即图中B点),烧杯内溶液中的溶质为(写化学式)
②当滴入8%的NaOH溶液100g时(即图中A点),恰好完全反应,试通过计算,求该实验样品中所含MgCl2的质量。
您最近一年使用:0次