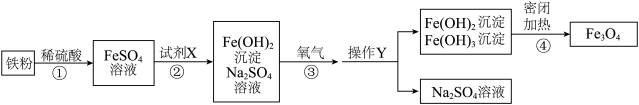
2023年5月30日,神舟十六号点火发射成功,3名航天员成功进驻中国空间站,再现6名航天员“太空会师”场面,全面实现了神舟飞船在“空间站时代”的再升级,为“神舟”踏上新征程打下坚实基础。请回答下列问题:
(1)偏二甲肼(C2H8N2)是运载火箭使用的燃料之一,该燃料与四氧化二氮(N2O4)反应的化学方程式为: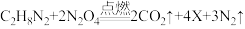 ,则X的化学式为
,则X的化学式为_____ ;
(2)镁合金、铝合金等材料以其低密度高使用寿命、优异的耐腐蚀及耐高温等综合性能,在飞行器及航天领域被广泛应用。
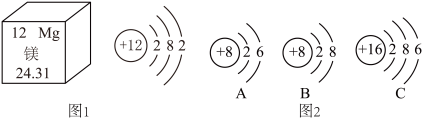
①图1是镁元素的部分信息,图2是另外三种微粒的结构示意图。镁原子在化学反应中易_____ (填“失去”或“得到”)电子。判断A与B属于同种元素的依据是_____ 。
②铝制品耐腐蚀,是因为常温下,铝能与空气中的氧气反应,在其表面形成一层致密的氧化铝薄膜,该反应的化学方程式为____ 。
(1)偏二甲肼(C2H8N2)是运载火箭使用的燃料之一,该燃料与四氧化二氮(N2O4)反应的化学方程式为:
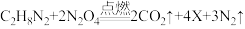 ,则X的化学式为
,则X的化学式为(2)镁合金、铝合金等材料以其低密度高使用寿命、优异的耐腐蚀及耐高温等综合性能,在飞行器及航天领域被广泛应用。

①图1是镁元素的部分信息,图2是另外三种微粒的结构示意图。镁原子在化学反应中易
②铝制品耐腐蚀,是因为常温下,铝能与空气中的氧气反应,在其表面形成一层致密的氧化铝薄膜,该反应的化学方程式为
更新时间:2024-02-05 17:52:06
|
相似题推荐
【推荐1】化学与我们的生活、生产、科技密切相关。
(1)Na2O2在日常生活中有着非常广泛的用途,可以用于消毒、杀菌和漂白等,Na2O2中氧元素的化合价为______ 价。
(2)防疫期间,人们常用84消毒液【主要成分为次氯酸钠(NaClO)】对生活场所进行杀菌、消毒,工业上制备NaClO的反应原理为2NaOH+Cl2═X+NaClO+H2O,则X的化学式为_______ 。
(3)三大化石燃料分别为煤、石油、天然气。写出天然气的主要成分燃烧的化学方程式_______ 。
(4)化学就在我们身边,写出下列常见物质的化学式。
①补钙剂的主要成分是_________ ;
②可用于金属表面除锈的酸(具有挥发性)是______________ ;
③纯碱______________ ;
④可用于改良酸性土壤的碱是_____________ 。
(1)Na2O2在日常生活中有着非常广泛的用途,可以用于消毒、杀菌和漂白等,Na2O2中氧元素的化合价为
(2)防疫期间,人们常用84消毒液【主要成分为次氯酸钠(NaClO)】对生活场所进行杀菌、消毒,工业上制备NaClO的反应原理为2NaOH+Cl2═X+NaClO+H2O,则X的化学式为
(3)三大化石燃料分别为煤、石油、天然气。写出天然气的主要成分燃烧的化学方程式
(4)化学就在我们身边,写出下列常见物质的化学式。
①补钙剂的主要成分是
②可用于金属表面除锈的酸(具有挥发性)是
③纯碱
④可用于改良酸性土壤的碱是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】燃煤电厂常采用脱硫技术以减少污染。其中某燃煤电厂脱硫后所产生的废水常含有CaCl2和MgCl2,下列是对脱硫废水进行软化并使其溶液转化成中性的一种工艺流程:
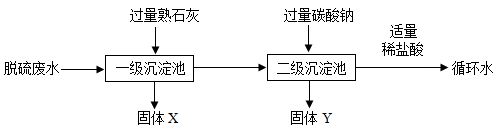
(1)目前,社会常用的能源还是以化石燃料为主,化石燃料中属于较清洁能源的是___________ (写化学式)。
(2)“脱硫”过程中发生反应的化学方程式为: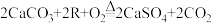 。R的化学式为
。R的化学式为___________ 。
(3)“二级沉淀”后加入适量稀盐酸目的是___________ 。
(4)脱硫废水在软化的过程中,熟石灰和碳酸钠的添加顺序___________ (填“可以”或“不可以”)颠倒。

(1)目前,社会常用的能源还是以化石燃料为主,化石燃料中属于较清洁能源的是
(2)“脱硫”过程中发生反应的化学方程式为:
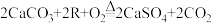 。R的化学式为
。R的化学式为(3)“二级沉淀”后加入适量稀盐酸目的是
(4)脱硫废水在软化的过程中,熟石灰和碳酸钠的添加顺序
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题:

(1)中国科学院等单位联合发布了115号元素,中文名为“镆”。该元素属于______ 元素(填“金属”或“非金属”),此元素原子的核电荷数为______ 。
(2)已知硫原子的中子数为16,则硫原子的相对原子质量为______ ,写出13号元素和16号元素形成化合物的化学式______ ,该物质的名称为______ 。
(3)最外层电子数是决定元素化学性质的重要依据,下列各组具有相似化学性质的元素是______(填字母)
(4)某粒子的结构示意图如图,当x﹣y=8时,该粒子的符号为______ 。


(1)中国科学院等单位联合发布了115号元素,中文名为“镆”。该元素属于
(2)已知硫原子的中子数为16,则硫原子的相对原子质量为
(3)最外层电子数是决定元素化学性质的重要依据,下列各组具有相似化学性质的元素是______(填字母)
| A.Na、Cl | B.O、S | C.F、Cl | D.Cl、Ar |

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】南昌大学研发的“硅衬底高光效GaN基蓝色发光二极管技术”获得2015年国家技术发明一等奖.请回答下列问题:

(1)图甲是镓在元素周期表中的信息以及原子结构示意图.镓的相对原子质量为_____ ;
(2)如图乙原子结构示意图所对应的元素与镓元素的化学性质相似的是____ (填序号),在化学反应中容易_________ (填“得到”或“失去”)电子。
(3)传统制备氮化镓的化学原理是:GaCl3+NH3 GaN+3X,其中X的化学式为
GaN+3X,其中X的化学式为____ .

(1)图甲是镓在元素周期表中的信息以及原子结构示意图.镓的相对原子质量为
(2)如图乙原子结构示意图所对应的元素与镓元素的化学性质相似的是
(3)传统制备氮化镓的化学原理是:GaCl3+NH3
 GaN+3X,其中X的化学式为
GaN+3X,其中X的化学式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
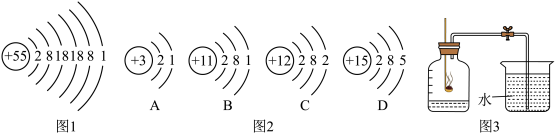
【推荐3】铯(Cs)原子钟是一种精密的计时工具。中国计量科学研究院研制的第二代铯原子钟是获得国际计量局认可的“世界上最好的基准原子钟”之一,其准确度达到2000万年不差一秒。饱原子结构示意图如图1所示。
回答下列问题:
(1)Cs属于______ (填“金属”或“非金属”)元素,在周期表中属于第______ 周期,
(2)图2表示的微粒中,与铯原子化学性质相似的是______ (填字母标号)。
(3)图2中由D所示原子构成的某种单质可用于测定空气中氧气的含量(如图3所示),该实验集气瓶底部的水作用为______ ,写出该单质发生反应的化学方______ 。

回答下列问题:
(1)Cs属于
(2)图2表示的微粒中,与铯原子化学性质相似的是
(3)图2中由D所示原子构成的某种单质可用于测定空气中氧气的含量(如图3所示),该实验集气瓶底部的水作用为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。请你回答:

(1)氟元素的相对原子质量为_____________ ;
(2)D中的X=_________ ;
(3)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似___________ (填序号);
(4)B和_______ 属于同种元素的粒子(用“A”、“C”、“D”填空);
(5)以上A、B、C、D粒子结构示意图中,表示稀有气体元素的原子的是________ 。

(1)氟元素的相对原子质量为
(2)D中的X=
(3)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似
(4)B和
(5)以上A、B、C、D粒子结构示意图中,表示稀有气体元素的原子的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下图为四种粒子的结构示意图,用对应的序号填空:

(1) 具有相对稳定结构的粒子是__________ ;
(2) 属于同种元素的粒子是______________ ;
(3) 某元素R形成的氧化物的化学式为R2O3,则R元素对应原子的原子结构示意图是_________ 。

(1) 具有相对稳定结构的粒子是
(2) 属于同种元素的粒子是
(3) 某元素R形成的氧化物的化学式为R2O3,则R元素对应原子的原子结构示意图是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】早在17世纪,质量守恒定律发现之前,英国化学家波义耳曾经做过一个实验:在密闭的容器中燃烧金属时,得到了金属灰,然后打开容器盖,称量金属灰的质量,发现比原来金属质量增加了。
(1)试解释金属灰质量比原金属质量增加的原因_____________ 。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律_______________________ 。
(1)试解释金属灰质量比原金属质量增加的原因
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量方法,以验证质量守恒定律
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】铝、铁、铜是生活中常见的三种金属,请根据金属及性质回答下列问题。
(1)生活中铝制品比铁制品更耐腐蚀,其原因是___________ 。
(2)某同学用未知金属M进行了以下实验,实验流程及现象如下图所示:(注:M在化合物中化合价为“+2”,题中M的化合物的溶液呈无色)

①写出步骤②中使溶液变蓝的化学反应方程式___________ 。
②蓝色滤液中一定含有溶质是___________ (填化学式)。以上实验可得出M、Cu、Ag三种金属活动性的强弱关系是___________ 。
(1)生活中铝制品比铁制品更耐腐蚀,其原因是
(2)某同学用未知金属M进行了以下实验,实验流程及现象如下图所示:(注:M在化合物中化合价为“+2”,题中M的化合物的溶液呈无色)

①写出步骤②中使溶液变蓝的化学反应方程式
②蓝色滤液中一定含有溶质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属材料被大量应用于工农业生产和其他领域。请回答:
(1)金属的物理性质的应用
下列金属的用途利用金属导热性的是___________ (填字母)。
a、铜制电线b、铁制铁锅c、金制项链d、铝制饮料罐
(2)金属的化学性质的应用
①铝制品耐腐蚀的原因是___________ 。
②实验室用锌与稀硫酸制取氢气的化学方程式是___________ ,所选用装置的连接顺序为___________ (填端口序号)。

(3)金属的获得
①湿法冶炼
“曾青(CuSO4)得铁则化为铜”所属的基本反应类型是___________
②电解法冶炼
工业上利用电解熔融的氧化铝得到铝和氧气,写出该反应的化学方程式。___________ 。
(1)金属的物理性质的应用
下列金属的用途利用金属导热性的是
a、铜制电线b、铁制铁锅c、金制项链d、铝制饮料罐
(2)金属的化学性质的应用
①铝制品耐腐蚀的原因是
②实验室用锌与稀硫酸制取氢气的化学方程式是

(3)金属的获得
①湿法冶炼
“曾青(CuSO4)得铁则化为铜”所属的基本反应类型是
②电解法冶炼
工业上利用电解熔融的氧化铝得到铝和氧气,写出该反应的化学方程式。
您最近一年使用:0次