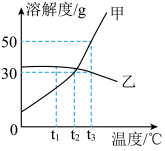
如图是硝酸钾、氯化钾固体的溶解度曲线。硝酸钾、氯化钾溶解度相等时的温度为_____ ℃:t1℃时,分别将等质量的硝酸钾、氯化钾的饱和溶液升温到t2℃,硝酸钾溶液中溶质的质量________ (填“大于”“等于”或“小于”)氯化钾溶液中溶质的质量;t2℃时,75g硝酸钾的饱和溶液稀释到25%,需加水________ g。

更新时间:2024-02-07 08:03:00
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
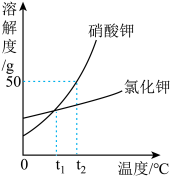
【推荐1】如图是物质A和B在不同温度时的溶解度及其溶解度曲线
回答下列问题:
(1)图中表示B物质溶解度曲线的是_____ (填“甲”或“乙”).
(2)曲线上M点的含义是_______________________________ .
(3)温度t1介于_________________ ℃之间.
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | A | 110 | 114 | 121 | 126 | 139 |
| B | 31.6 | 45.8 | 85.5 | 110 | 169 |
回答下列问题:
(1)图中表示B物质溶解度曲线的是
(2)曲线上M点的含义是
(3)温度t1介于

您最近一年使用:0次
【推荐2】在劳动中感悟化学原理。
(1)和家人一起包饺子。
①煮饺子:打开燃气灶阀门,燃气燃烧过程中将______ 能转化为热能。
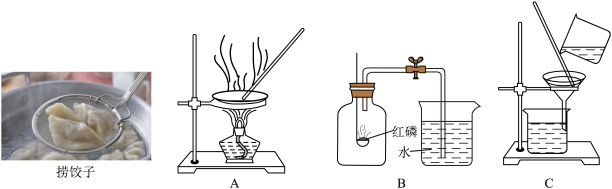
②捞饺子:用漏勺将饺子捞出,利用的原理与下图A、B、C所示相同的是______ (填字母序号)。______ 。
(2)为了防止学校花园里的铁制工艺品生锈,同学们为铁艺刷油漆,以隔绝______ 。
(3)同学们来到晒盐场开展实践活动。结合如图氯化钠的溶解度曲线,请回答下列问题:______ g。
②获得食盐晶体常用的结晶方法:______ 。
(1)和家人一起包饺子。
①煮饺子:打开燃气灶阀门,燃气燃烧过程中将
②捞饺子:用漏勺将饺子捞出,利用的原理与下图A、B、C所示相同的是
(2)为了防止学校花园里的铁制工艺品生锈,同学们为铁艺刷油漆,以隔绝
(3)同学们来到晒盐场开展实践活动。结合如图氯化钠的溶解度曲线,请回答下列问题:
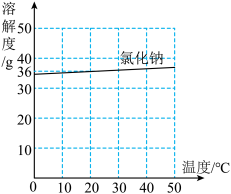
②获得食盐晶体常用的结晶方法:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】海洋是人类的母亲,是巨大的资源宝库。请回答下列问题:_____ (填写化学式)。
(2) 时,将
时,将 碳酸氢钠放入
碳酸氢钠放入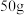 水中充分溶解,得到
水中充分溶解,得到__ g溶液。
(3)下列说法正确的是___。

(2)
 时,将
时,将 碳酸氢钠放入
碳酸氢钠放入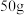 水中充分溶解,得到
水中充分溶解,得到(3)下列说法正确的是___。
| A.碳酸钠的溶解度大于碳酸氢钠的溶解度 |
B. 时,等质量的碳酸钠和碳酸氢钠配成饱和溶液,碳酸氢钠需要的水多 时,等质量的碳酸钠和碳酸氢钠配成饱和溶液,碳酸氢钠需要的水多 |
C.使B点的溶液转变为A点的溶液,只能通过加入 完成 完成 |
| D.碳酸氢钠不稳定,受热易分解 |
您最近一年使用:0次
【推荐1】请回答下列问题。
(1)党的二十大报告中对生态环境保护和绿色低碳发展做出了重大战略部属,深入学习、领会党的二十大精神中关于绿色低碳发展的要义,是我们做好生态环境保护工作的根本遵循。
①下列各项叙述中,不符合保护环境、绿色发展要求的是______ (填选项序号之一)。
A. 禁止使用化石燃料
B. 减少一次性餐具的使用
C. 使用催化净化装置,减少汽车尾气污染
D. 不用的电池,要放入有害垃圾桶
②天然气是一种家庭常用燃料,天然气的主要成分是甲烷( ),根据你所学的知识写出甲烷作为清洁燃料的优点:
),根据你所学的知识写出甲烷作为清洁燃料的优点:______ 。如果每个家庭每天平均消耗0.32kg甲烷,向大气中排放的碳元素的质量为______ kg。(结果保留0.01kg)
③自然界的水资源通过天然循环实现了水的自身净化和水资源的重新分配,水的天然循环是通过水的三态变化实现的,______ 提供了能量。
④煤的气化和液化可实现能源清洁化,改善空气质量。水煤气中的一氧化碳和氢气在高温、高压和催化剂条件下合成甲醇( ),该反应的化学方程式是
),该反应的化学方程式是______ 。
(2)海洋是人类的巨大资源宝库,从海水中可以得到重要化工原料NaCl和 。NaCl和
。NaCl和 的溶解度曲线如图所示,试回答下列问题:
的溶解度曲线如图所示,试回答下列问题:

①t2℃时, 的溶解度是
的溶解度是______ g,其饱和溶液的溶质量分数是______ (保留到0.1%)
②t2℃时,将不同质量的 饱和溶液和NaCl饱和溶液均降温至t1℃,此时,
饱和溶液和NaCl饱和溶液均降温至t1℃,此时, 溶液的溶质质量分数
溶液的溶质质量分数______ (填“大于”“等于”“小于”或“无法判断”)NaCl溶液的溶质质量分数。
③下列说法中,不正确的是___ (选填序号)。
A. 是一种常用的氮肥,在施用的时候不能与熟石灰混合使用。
是一种常用的氮肥,在施用的时候不能与熟石灰混合使用。
B. t2℃时,向100g20%NH4Cl的不饱和溶液中加入100g水,充分搅拌,溶液质量分数为10%
C. t2℃时,等质量的NH4Cl、NaCl分别制成饱和溶液,需要水的质量最多的是NH4Cl
D. 降低KNO3溶液的温度,一定有晶体析出
(1)党的二十大报告中对生态环境保护和绿色低碳发展做出了重大战略部属,深入学习、领会党的二十大精神中关于绿色低碳发展的要义,是我们做好生态环境保护工作的根本遵循。
①下列各项叙述中,不符合保护环境、绿色发展要求的是
A. 禁止使用化石燃料
B. 减少一次性餐具的使用
C. 使用催化净化装置,减少汽车尾气污染
D. 不用的电池,要放入有害垃圾桶
②天然气是一种家庭常用燃料,天然气的主要成分是甲烷(
 ),根据你所学的知识写出甲烷作为清洁燃料的优点:
),根据你所学的知识写出甲烷作为清洁燃料的优点:③自然界的水资源通过天然循环实现了水的自身净化和水资源的重新分配,水的天然循环是通过水的三态变化实现的,
④煤的气化和液化可实现能源清洁化,改善空气质量。水煤气中的一氧化碳和氢气在高温、高压和催化剂条件下合成甲醇(
 ),该反应的化学方程式是
),该反应的化学方程式是(2)海洋是人类的巨大资源宝库,从海水中可以得到重要化工原料NaCl和
 。NaCl和
。NaCl和 的溶解度曲线如图所示,试回答下列问题:
的溶解度曲线如图所示,试回答下列问题:
①t2℃时,
 的溶解度是
的溶解度是②t2℃时,将不同质量的
 饱和溶液和NaCl饱和溶液均降温至t1℃,此时,
饱和溶液和NaCl饱和溶液均降温至t1℃,此时, 溶液的溶质质量分数
溶液的溶质质量分数③下列说法中,不正确的是
A.
 是一种常用的氮肥,在施用的时候不能与熟石灰混合使用。
是一种常用的氮肥,在施用的时候不能与熟石灰混合使用。B. t2℃时,向100g20%NH4Cl的不饱和溶液中加入100g水,充分搅拌,溶液质量分数为10%
C. t2℃时,等质量的NH4Cl、NaCl分别制成饱和溶液,需要水的质量最多的是NH4Cl
D. 降低KNO3溶液的温度,一定有晶体析出
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
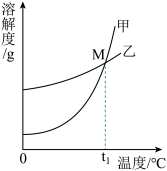
【推荐2】如图为甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)t1℃时,向30g甲物质中加入50g水,充分溶解后,所得溶液质量为_______ ,将其升高到t2℃时,所得溶液中溶质和溶液质量比为_______ 。

(2)在温度高于t2℃时,把等质量的甲、乙、丙分别配制成饱和溶液,所得溶液质量由大到小的顺序为_______ 。
(3)将t2℃时甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序为_______ 。
(1)t1℃时,向30g甲物质中加入50g水,充分溶解后,所得溶液质量为

(2)在温度高于t2℃时,把等质量的甲、乙、丙分别配制成饱和溶液,所得溶液质量由大到小的顺序为
(3)将t2℃时甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数由大到小的顺序为
您最近一年使用:0次
【推荐1】2021年“世界水日”的主题为“珍惜水、爱护水”。
(1)2021年5月开始,“南水北调东线北延应急供水工程”启动向京津等地供水,以缓解我国华北地区可利用淡水资源___________ 的现状。
(2)下列有关保护水资源的说法正确的是___________(填字母)。
(3)如图是利用海水提取粗盐的过程。

根据海水晒盐的原理,下列说法正确的是___________(填字母)。
(4)某同学配制50g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为___________ g。
②配制过程有以下步骤:a、称量及量取b、计算c、溶解d、装瓶贴标签,正确顺序是___________ (填字母)。
③将50g溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水___________ g。
(5)为研究水的组成,某同学进行了电解水实验。
①电解水的时候,明明没有漏气,但氢气和氧气的体积比总是略大于2∶1,可能的原因是:___________ ;
②电解水的实验证明水是由___________ 元素组成的。
(1)2021年5月开始,“南水北调东线北延应急供水工程”启动向京津等地供水,以缓解我国华北地区可利用淡水资源
(2)下列有关保护水资源的说法正确的是___________(填字母)。
| A.生活污水可直接排放 |
| B.工业上对污染的水体作处理使之符合排放标准后再排放 |
| C.农药、化肥的施用会造成水体污染,应该禁止施用 |
(3)如图是利用海水提取粗盐的过程。

根据海水晒盐的原理,下列说法正确的是___________(填字母)。
| A.进入贮水池中的海水,氯化钠的质量逐渐减少 |
| B.在蒸发池中,海水中氯化钠的质量逐渐增加 |
| C.析出晶体后,母液中的氯化钠溶液达到饱和 |
(4)某同学配制50g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为
②配制过程有以下步骤:a、称量及量取b、计算c、溶解d、装瓶贴标签,正确顺序是
③将50g溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水
(5)为研究水的组成,某同学进行了电解水实验。
①电解水的时候,明明没有漏气,但氢气和氧气的体积比总是略大于2∶1,可能的原因是:
②电解水的实验证明水是由
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】溶液在日常生活、工农业生产和科学研究中具有广泛用途。Ca(OH)2 、 KNO3 、 NaCl的溶解度如下表所示。
回答问题:
(1)Ca(OH)2 的溶解度随温度的升高而_____ (填“增大”或“减小”)。
(2)将接近饱和的KNO3溶液变为饱和溶液,可以采用的一种方法是_____ 。
(3)农业上常用质量分数为16%的 NaCl溶液选种。20℃时,将136g饱和 NaCl溶液稀释成质量分数为16%的 NaCl溶液,需加水的质量为_____ 。
(4)下列有关说法正确的是 (填标号)。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | 氢氧化钙 | 0.18 | 0.16 | 0.14 | 0.11 | 0.09 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
| 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | |
(1)Ca(OH)2 的溶解度随温度的升高而
(2)将接近饱和的KNO3溶液变为饱和溶液,可以采用的一种方法是
(3)农业上常用质量分数为16%的 NaCl溶液选种。20℃时,将136g饱和 NaCl溶液稀释成质量分数为16%的 NaCl溶液,需加水的质量为
(4)下列有关说法正确的是 (填标号)。
| A.40℃时,向氢氧化钙饱和溶液中加入少量硝酸钾,溶液质量不变 |
| B.60℃时,将100g硝酸钾饱和溶液恒温蒸发10g水,析出11g硝酸钾 |
| C.某物质的不饱和溶液,其溶质的质量分数可能比该物质的饱和溶液大 |
您最近一年使用:0次

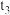 ℃时等质量的甲、乙的饱和溶液降温到
℃时等质量的甲、乙的饱和溶液降温到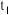 ℃,所得溶液中溶剂的质量为甲
℃,所得溶液中溶剂的质量为甲