如图是a、b、c三种物质的溶解度曲线。

(1)b溶液在点P时处于______ (填”饱和”或”不饱和”)状态;
(2)t2℃时,150克水中最多能溶解a物质______ ;
(3)除去a 固体中混有的少量b,提纯的步骤是:加水溶解、蒸发浓缩、______ ,然后过滤、洗涤、干燥;
(4)t2℃时,将a、b、c三种物质的饱和溶液降温至t1℃,下列说法正确的是______ 。
Ⅰ、溶剂的质量:a>b>c Ⅱ、析出固体的质量a>b,c无固体析出
Ⅲ、溶质质量分数:b>a>c Ⅳ、a、b是饱和溶液,c是不饱和溶液

(1)b溶液在点P时处于
(2)t2℃时,150克水中最多能溶解a物质
(3)除去a 固体中混有的少量b,提纯的步骤是:加水溶解、蒸发浓缩、
(4)t2℃时,将a、b、c三种物质的饱和溶液降温至t1℃,下列说法正确的是
Ⅰ、溶剂的质量:a>b>c Ⅱ、析出固体的质量a>b,c无固体析出
Ⅲ、溶质质量分数:b>a>c Ⅳ、a、b是饱和溶液,c是不饱和溶液
更新时间:2024-02-04 07:55:36
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】电缆生产过程中产生了一定量的含铜废料。化学兴趣小组利用过量稀硫酸和铁粉分离回收铜,并获得硫酸亚铁晶体。先将含铜废料粉碎,再按如下设计方案处理:
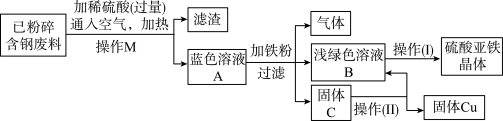
查阅资料得知:在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜。反应的化学方程式: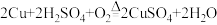 。
。
(1)步骤中分离得到蓝色溶液A的操作M名称是_______ ,粉碎的目的是_______ 。
(2)写出铁与硫酸铜溶液反应的化学方程式_______ 。
(3)蓝色溶液A中溶质的成分是_______ (填化学式)。
(4)该方案中加入过量的铁粉目的是_______ ;从浅绿色溶液B得到硫酸亚铁晶体常要经过蒸发浓缩、_______ 、洗涤、干燥等步骤。
(5)铜制品在空气中发生锈蚀生成铜锈【Cu2(OH)2CO3】。根据铜锈主要成分的元素组成,可以判断出铜生锈除了具备铁生锈应有的条件外,还需要空气中的CO2共同参与反应,写出铜在潮湿的空气中生成铜锈的化学方程式_______ 。

查阅资料得知:在通入空气并加热的条件下,铜可与稀硫酸反应转化为硫酸铜。反应的化学方程式:
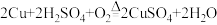 。
。(1)步骤中分离得到蓝色溶液A的操作M名称是
(2)写出铁与硫酸铜溶液反应的化学方程式
(3)蓝色溶液A中溶质的成分是
(4)该方案中加入过量的铁粉目的是
(5)铜制品在空气中发生锈蚀生成铜锈【Cu2(OH)2CO3】。根据铜锈主要成分的元素组成,可以判断出铜生锈除了具备铁生锈应有的条件外,还需要空气中的CO2共同参与反应,写出铜在潮湿的空气中生成铜锈的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图1是硝酸钾、氯化钠和图2氢氧化钙固体物质在水中的溶解度曲线,请回答下列问题。
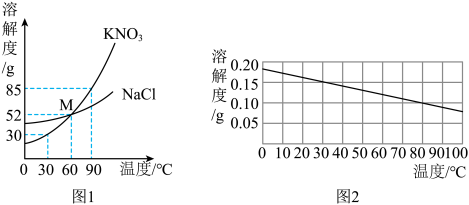
(1)交点M的含义是_______ 。
(2)硝酸钾中含有少量的氯化钠,为了得到纯净的硝酸钾常用的方法是_______ 。
(3)图2中,将接近饱和的氢氧化钙溶液变为饱和溶液,且质量分数不变的方法是_______ 。
(4)图1中,80℃时将45g的硝酸钾加入50g水中,充分溶解,所得溶液的溶质质量分数为_______ 。
(5)图1中,将80℃等质量的硝酸钾和氯化钠的饱和溶液降温至60℃,所得溶液的溶质质量分数关系为_______ 。

(1)交点M的含义是
(2)硝酸钾中含有少量的氯化钠,为了得到纯净的硝酸钾常用的方法是
(3)图2中,将接近饱和的氢氧化钙溶液变为饱和溶液,且质量分数不变的方法是
(4)图1中,80℃时将45g的硝酸钾加入50g水中,充分溶解,所得溶液的溶质质量分数为
(5)图1中,将80℃等质量的硝酸钾和氯化钠的饱和溶液降温至60℃,所得溶液的溶质质量分数关系为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】 时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:
时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:
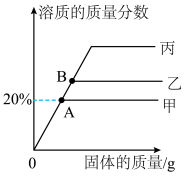
(1)该温度下,甲、乙、丙三种固体的溶解度由大到小的顺序是______ 。
(2)乙溶液在 点属于
点属于______ (填“饱和”或“不饱和”)溶液。
(3)将甲的不饱和溶液变为饱和溶液,可采取的方法是______ 。
(4)该温度下,甲的溶解度为______ 。
(5)已知乙和丙的溶解度均随温度的降低而减小,其中乙的溶解度受温度变化影响较小,丙的溶解度受温度变化影响较大,当丙中混有少量乙时,提纯丙的方法是______ 。
 时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:
时,等质量的甲、乙、丙三种固体分别加入等质量的水中,加入固体的质量与溶液溶质质量分数的关系如图所示,请回答下列问题:
(1)该温度下,甲、乙、丙三种固体的溶解度由大到小的顺序是
(2)乙溶液在
 点属于
点属于(3)将甲的不饱和溶液变为饱和溶液,可采取的方法是
(4)该温度下,甲的溶解度为
(5)已知乙和丙的溶解度均随温度的降低而减小,其中乙的溶解度受温度变化影响较小,丙的溶解度受温度变化影响较大,当丙中混有少量乙时,提纯丙的方法是
您最近一年使用:0次
【推荐1】向装有等量水的A、B、C烧杯中加入10g、20g、25g的NaNO3固体,充分溶解后,现象如图一所示:

(1)A、B、C烧杯中溶液一定属于饱和溶液的是_______ (填标号);
(2)图二中能表示NaNO3溶解度曲线的是______ (填“甲”或“乙”);
(3)要使B烧杯中剩余固体继续溶解,可采用的方法是_________________________ ;
(4)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的质量是______ (填标号)。
A.甲=乙 B.甲>乙 C.甲<乙 D.无法判断

(1)A、B、C烧杯中溶液一定属于饱和溶液的是
(2)图二中能表示NaNO3溶解度曲线的是
(3)要使B烧杯中剩余固体继续溶解,可采用的方法是
(4)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的质量是
A.甲=乙 B.甲>乙 C.甲<乙 D.无法判断
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
(1)10℃时,KNO3溶解度是______ g。
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为______ g。
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过______ 方法获得较纯净的KNO3晶体。
(4)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是______ 。
a.10℃~20℃ b.20℃~40℃ c.40℃~60℃ d.60℃~80℃
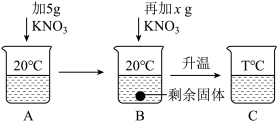
(5)向20mL水中溶解一定量KNO3固体的操作如图:请根据实验现象和溶解度数据回答:A、B、C中溶液一定是不饱和溶液的是______ 。当x=______ g时,B中恰好没有固体剩余。
| 温度/℃ | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
(1)10℃时,KNO3溶解度是
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过
(4)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是
a.10℃~20℃ b.20℃~40℃ c.40℃~60℃ d.60℃~80℃
(5)向20mL水中溶解一定量KNO3固体的操作如图:请根据实验现象和溶解度数据回答:A、B、C中溶液一定是不饱和溶液的是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】A、B、C三种固体物质在水中的溶解度曲线如图所示。
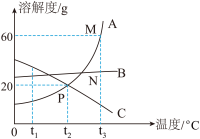
(1)交点P的含义是_______ 。
(2)t1℃时,A、B、C三种物质的溶解度大小关系为_______ 。
(3)将A物质的溶液状态由N点转变为M点,可以采取的方法是_______ (填一种即可)。
(4)下列有关叙述正确的是 (填序号)。

(1)交点P的含义是
(2)t1℃时,A、B、C三种物质的溶解度大小关系为
(3)将A物质的溶液状态由N点转变为M点,可以采取的方法是
(4)下列有关叙述正确的是 (填序号)。
| A.当A中混有少量B时,可用降温结晶的方法提纯A |
| B.分别将t2℃的A、B的饱和溶液降到t1℃,析出固体的质量大小关系为B>A |
| C.将接近饱和的A溶液中析出一定质量的A晶体后,溶液的溶质质量分数一定变小 |
| D.分别将t1℃的A、B、C的饱和溶液升温到t3℃,所得溶液的溶质质量分数大小关系为A>B>C |
| E.t3℃时分别用50gA、B、C固体溶于水配成饱和溶液,需要水的质量大小关系为C>B>A |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】下表是NaCl和KNO3的溶解度表,如图所示是NaCl和KNO3的溶解度曲线。请回答:

(1)t1℃时NaCl的溶解度________ KNO3的溶解度(填“>”、“<”或“=”)。
(2)t2℃时分别将等质量的A、B的饱和溶液降温至t1℃,所得溶液中溶质的质量A________ B(填“>”、“<”或“=”)。
(3)某一温度时,向75 g KNO3的饱和溶液中加入50 g水,可以得到质量分数为20%的溶液,则该温度下KNO3的溶解度为________ 。
温度/℃ | 0 | 20 | 30 | 40 | 50 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.3 | 36.6 | 37.0 |
KNO3 | 13.3 | 31.6 | 45.8 | 63.9 | 85.5 | |

(1)t1℃时NaCl的溶解度
(2)t2℃时分别将等质量的A、B的饱和溶液降温至t1℃,所得溶液中溶质的质量A
(3)某一温度时,向75 g KNO3的饱和溶液中加入50 g水,可以得到质量分数为20%的溶液,则该温度下KNO3的溶解度为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】下表是氯化钾和硝酸钾在不同温度时的溶解度,这两种固体物质在水中的溶解度曲线如图所示,回答问题:
(1)乙曲线表示的是_____ (填化学式)的溶解度曲线。
(2)图中t°C所对应的温度范围是_____ (填字母)。

A 20~30°C
B 30 ~40°C
C 40~50°C
(3)某化学兴趣小组的同学在老师的指导下用固体甲做了如下实验:
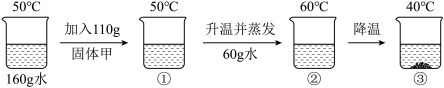
①、②、③中的溶液属于饱和溶液的是___ (填序号),③中析出晶体的质量为___ g。
| 温度/°C | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | |
(2)图中t°C所对应的温度范围是

A 20~30°C
B 30 ~40°C
C 40~50°C
(3)某化学兴趣小组的同学在老师的指导下用固体甲做了如下实验:

①、②、③中的溶液属于饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙三种物质的溶解度曲线如图所示,据图回答:
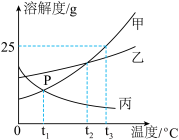
(1)p点的含义是_____ 。
(2)t3℃时,将25g甲物质放入50g水中,充分溶解后,该溶液的质量为_____ 。
(3)甲物质中含有少量的乙物质,要提纯甲物质,通常采用的方法是_____ 。
(4)三种物质的溶解度满足 甲 > 乙 >丙的温度范围是________ 。
(5)t3℃时,将A、B、C的饱和溶液蒸发相同质量的水,再回到t3℃时,析出晶体最多的是________ 。

(1)p点的含义是
(2)t3℃时,将25g甲物质放入50g水中,充分溶解后,该溶液的质量为
(3)甲物质中含有少量的乙物质,要提纯甲物质,通常采用的方法是
(4)三种物质的溶解度满足 甲 > 乙 >丙的温度范围是
(5)t3℃时,将A、B、C的饱和溶液蒸发相同质量的水,再回到t3℃时,析出晶体最多的是
您最近一年使用:0次
【推荐2】氯化钠是一种重要的化工原料,利用海水可制得氯化钠进而可以制得氢氧化钠、氢气和氯气。其主要工艺流程如图1所示。图2为甲、氯化钠和丙三种物质的溶解度曲线
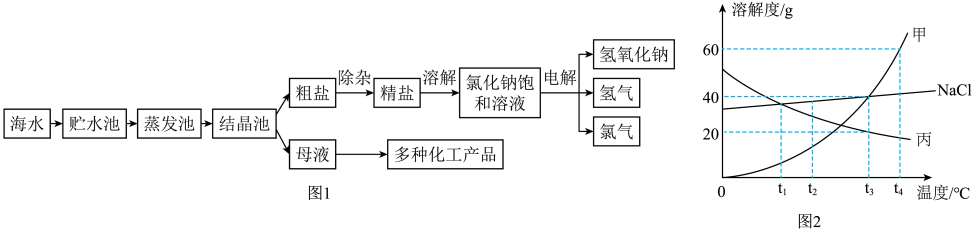
(1)结晶池析出晶体后得到的母液是氯化钠的______ (填“饱和”或“不饱和”)溶液
(2)海水制盐选用蒸发结晶法而不用降温结晶法的理由是______ 。
(3)工业上电解氯化钠饱和溶液的化学方程式是______ 。
(4)①t4℃时,80g甲饱和溶液稀释为20%需加水______ g。
②将t4℃时甲、NaCl、丙三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数从大到小的顺序为______ (分别用甲、NaCl、丙代表各自所得溶液溶质质量分数)。

(1)结晶池析出晶体后得到的母液是氯化钠的
(2)海水制盐选用蒸发结晶法而不用降温结晶法的理由是
(3)工业上电解氯化钠饱和溶液的化学方程式是
(4)①t4℃时,80g甲饱和溶液稀释为20%需加水
②将t4℃时甲、NaCl、丙三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数从大到小的顺序为
您最近一年使用:0次




