下图是A、B两种固体物质的溶解度曲线。据图回答:
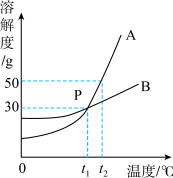
(1)P点表示的意义是_____ 。
(2)把t2℃时等质量A、B两物质的饱和溶液降低到t1℃,析出晶体较多的是_____ 。
(3)当A中含有少量B物质时,可采用_____ 的方法提纯A物质。
(4)t2℃时,将90gA物质投入到100g水中,得到A物质的_____ (填“饱和”或“不饱和”)溶液,此时溶液的质量是 _____ g。
(5)t2℃时,将30gA物质投入到100g水中,可再采取哪些具体措施,使之变为饱和溶液?_____ 。

(1)P点表示的意义是
(2)把t2℃时等质量A、B两物质的饱和溶液降低到t1℃,析出晶体较多的是
(3)当A中含有少量B物质时,可采用
(4)t2℃时,将90gA物质投入到100g水中,得到A物质的
(5)t2℃时,将30gA物质投入到100g水中,可再采取哪些具体措施,使之变为饱和溶液?
2014·山东日照·中考模拟 查看更多[6]
更新时间:2016-11-28 12:14:40
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】同学们对NaCl、KNO3两种物质的分离与提纯展开探究。下表是NaCl、KNO3在不同温度时的溶解度。
(1)20℃时,硝酸钾的溶解度是______ 。
(2)t℃时若要配制溶质质量分数相同的KNO3、NaCl的饱和溶液,t的最小范围是______ 。
(3)其NaCl样品中混有少量KNO3,可利用溶解度差异进行提纯。称取42g样品进行如下实验:______ g。
②对整个实验过程分析不正确的是______ (填字母)。
A.该实验采用的分离混合物的方法是结晶和过滤
B.步骤Ⅱ中氯化钠溶液的质量分数在不断变大
C.若步骤Ⅲ中温度降低到40℃时才过滤,将不能得到纯净的氯化钠晶体
D.对滤液进行降温结晶,就能回收到纯净的硝酸钾晶体
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
(1)20℃时,硝酸钾的溶解度是
(2)t℃时若要配制溶质质量分数相同的KNO3、NaCl的饱和溶液,t的最小范围是
(3)其NaCl样品中混有少量KNO3,可利用溶解度差异进行提纯。称取42g样品进行如下实验:
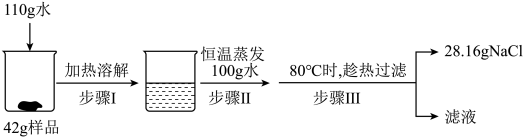
②对整个实验过程分析不正确的是
A.该实验采用的分离混合物的方法是结晶和过滤
B.步骤Ⅱ中氯化钠溶液的质量分数在不断变大
C.若步骤Ⅲ中温度降低到40℃时才过滤,将不能得到纯净的氯化钠晶体
D.对滤液进行降温结晶,就能回收到纯净的硝酸钾晶体
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】工业上以硫铁矿烧渣(主要成分为FeO、Fe2O3及少量Al2O3、SiO2)为原料制备硫酸亚铁晶体(FeSO4·7H2O)的流程如下:

【查阅资料】Al2O3、SiO2能与浓氢氧化钠溶液反应,而FeO、Fe2O3不反应。
(1)粉碎烧渣这一过程属于______________ (选填“物理”或“化学”)变化。
(2)已知SOi2与CO2的化学性质相似,都能和氢氧化钠溶液反应。“碱浸”步骤中SiO2与浓氢氧化钠溶液反应的生成物是水和______________ (填化学式)。
(3)“酸溶”步骤中反应的基本反应类型是______________ 。
(4)经过铁粉还原步骤以后,溶液中的金属阳离子只有Fe2+,则还原步骤中Fe将Fe3+还原的反应的化学方程式是__________ 。
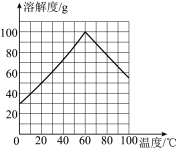
(5)FeSO4·7H2O的溶解度曲线如图所示,由FeSO4溶液获得FeSO4·7H2O晶体的实验步骤是蒸发浓缩、_________ 、过滤、少量冰水洗涤、低温干燥。

【查阅资料】Al2O3、SiO2能与浓氢氧化钠溶液反应,而FeO、Fe2O3不反应。
(1)粉碎烧渣这一过程属于
(2)已知SOi2与CO2的化学性质相似,都能和氢氧化钠溶液反应。“碱浸”步骤中SiO2与浓氢氧化钠溶液反应的生成物是水和
(3)“酸溶”步骤中反应的基本反应类型是
(4)经过铁粉还原步骤以后,溶液中的金属阳离子只有Fe2+,则还原步骤中Fe将Fe3+还原的反应的化学方程式是
(5)FeSO4·7H2O的溶解度曲线如图所示,由FeSO4溶液获得FeSO4·7H2O晶体的实验步骤是蒸发浓缩、

您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
【推荐3】如图是甲、乙、丙三种固体的溶解度曲线。请回答下列问题:
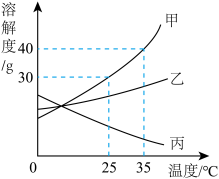
(1)35℃时,将50g甲固体加入到75g水中,充分溶解并恢复到原温度后,得到溶液的质量是___ g。
(2)要使25℃时接近饱和的丙溶液变成该温度下的饱和溶液,可采用的一种方法是_________ 。
(3)若将35℃时甲的饱和溶液降温到25℃,则其溶液的溶质质量分数会______ (填“变大”、“变小”或不变)。
(4)现有以下操作步骤:A 溶解;B 过滤;C 降温结晶;D 加热浓缩
若甲固体中含有少量乙,则提纯甲的操作步骤是__________ 。

(1)35℃时,将50g甲固体加入到75g水中,充分溶解并恢复到原温度后,得到溶液的质量是
(2)要使25℃时接近饱和的丙溶液变成该温度下的饱和溶液,可采用的一种方法是
(3)若将35℃时甲的饱和溶液降温到25℃,则其溶液的溶质质量分数会
(4)现有以下操作步骤:A 溶解;B 过滤;C 降温结晶;D 加热浓缩
若甲固体中含有少量乙,则提纯甲的操作步骤是
您最近一年使用:0次
填空与简答-科普阅读题
|
较难
(0.4)
解题方法
【推荐1】根据以下材料回答问题。
【材料一】据报道,在普通口罩上添加氯化钠涂层,就能将其转化为“特效口罩”。使用过程中,氯化钠会溶解于病毒自身携带的水中,杀死病毒,后水分蒸发,氯化钠再次析出。
【材料二】氯化钠的溶解度如下:
【材料三】某实验小组在室温(20℃)下,进行粗盐提纯的实验流程如下图所示:

(1)根据材料一:口罩使用过程中,氯化钠溶液中溶质质量分数______ (填“改变”或“不变”)。 构成氯化钠的阴离子符号为______ 。钠原子转化为钠离子,其核外电子数 ______ (填“增加”、 “减少”或“不变”)。
(2)根据材料二:20℃时,100.0g水中溶解________ g 氯化钠恰好饱和,若要把该饱和溶液转化成不饱和溶液,可以采用 _______ (填“搅拌”或“加水”)的方法。
(3)根据材料二和三:
①溶液A是_________ (选填“饱和”或“不饱和”)溶液。
②操作Ⅱ是____ ,用到的玻璃仪器有_______ 、烧杯、玻璃棒,其中玻璃棒的作用是_______ 。
③操作Ⅲ过程中溶液质量与时间变化关系如右图所示,相关分析正确的是_______ (填字母)。
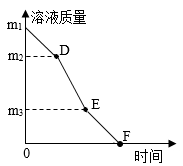
a.m1< 20g
b.(m2-m3)是减少的水的质量
c.D、E 点表示的溶液溶质质量分数相同
d.F 点时,停止加热
④该实验得到精盐的产率为_______ 。
【材料一】据报道,在普通口罩上添加氯化钠涂层,就能将其转化为“特效口罩”。使用过程中,氯化钠会溶解于病毒自身携带的水中,杀死病毒,后水分蒸发,氯化钠再次析出。
【材料二】氯化钠的溶解度如下:
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| 溶解度(g) | 35.8 | 36.0 | 36.1 | 36.4 | 37.1 | 38.0 | 39.2 |

(1)根据材料一:口罩使用过程中,氯化钠溶液中溶质质量分数
(2)根据材料二:20℃时,100.0g水中溶解
(3)根据材料二和三:
①溶液A是
②操作Ⅱ是
③操作Ⅲ过程中溶液质量与时间变化关系如右图所示,相关分析正确的是

a.m1< 20g
b.(m2-m3)是减少的水的质量
c.D、E 点表示的溶液溶质质量分数相同
d.F 点时,停止加热
④该实验得到精盐的产率为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】研究溶液对生产、生活有重要的意义。下表是NaCl和KNO3在不同温度下的溶解度。
______ g。
(2)NaCl的饱和溶液中含有少量KNO3,提纯NaCl,采用的方法是______ (选填“蒸发结晶”或“降温结晶”);
(3)根据图示实验和溶解度表,下列说法不正确的是______。
| 温度℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |

(2)NaCl的饱和溶液中含有少量KNO3,提纯NaCl,采用的方法是
(3)根据图示实验和溶解度表,下列说法不正确的是______。
| A.若a是NaCl,则③中的溶液是不饱和溶液 |
| B.若a是NaC1,则④中溶质的质量分数约为27.2% |
| C.若a是KNO3,则③到④溶液由不饱和转化为饱和 |
| D.实验证明溶液是否饱和与温度、溶质的量和溶剂种类有关 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】如图是a、b、c三种物质的溶解度曲线,据图回答下列问题。
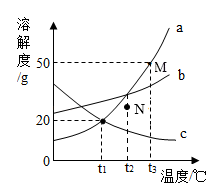
(1)t1℃时,把30g物质a加入到100g水中充分搅拌、静置,形成的是_________ 溶液(填“饱和”或“不饱和”)。
(2)t3℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是_________ 。
(3)将a物质N点状态下的溶液转化到M点的溶液可采取的措施是____________ 。
(4)下列说法中正确的是_____________ 。
a.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
b.配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高
c.将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减小
d.将t3℃时a、b、c三种物质的饱和溶液降温到t1℃,三种溶液溶质质量分数的大小关系为:b>a=c

(1)t1℃时,把30g物质a加入到100g水中充分搅拌、静置,形成的是
(2)t3℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
(3)将a物质N点状态下的溶液转化到M点的溶液可采取的措施是
(4)下列说法中正确的是
a.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
b.配制一定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高
c.将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量一定减小
d.将t3℃时a、b、c三种物质的饱和溶液降温到t1℃,三种溶液溶质质量分数的大小关系为:b>a=c
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】(1)用化学用语填空:
①氯气分子____ ;②电解水过程中不变的微粒____ ;
(2)写出下列反应的化学方程式:①工业上用磁铁矿来炼铁:____ ;②2017年5月18我国首次试采可燃冰(CH4·nH2O)宣告成功,可燃冰分解后,可释放出水和天然气,请写出天然气完全燃烧的化学方程式:____ ;
(3)如图是A、B两种固体物质的溶解度曲线.回答:
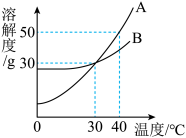
①要使接近饱和的A溶液变为饱和溶液,可采取的方法是__ ;
②在40℃时,等质量的A、B物质的饱和溶液降温到30℃时溶液质量的关系A____ B(选填“大于”、“小于”或“等于”);
③30℃时,130gA的饱和溶液,升温到40℃时,至少需加入A物质的质量为____ g才能变成饱和溶液;
④当A中混有少量B时,用____ 方法可以得到固体A.
①氯气分子
(2)写出下列反应的化学方程式:①工业上用磁铁矿来炼铁:
(3)如图是A、B两种固体物质的溶解度曲线.回答:

①要使接近饱和的A溶液变为饱和溶液,可采取的方法是
②在40℃时,等质量的A、B物质的饱和溶液降温到30℃时溶液质量的关系A
③30℃时,130gA的饱和溶液,升温到40℃时,至少需加入A物质的质量为
④当A中混有少量B时,用
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】盐是百味之首,也是咸味的来源。某市有一盐矿深埋地下千米左右,储量百亿吨以上,除NaCl外还含有少量 等。NaCl、
等。NaCl、 的溶解度曲线如图1所示。
的溶解度曲线如图1所示。

(1)利用天然气
(2)抽出的卤水检验合格后通过管道送往厂区。为防止冬季管道堵塞,检验时合格的卤水必须是该温度下的
(3)如图2所示是该盐厂采用的NaCl、
 联产工艺流程。析盐罐内真空减压蒸发水,温度宜控制为
联产工艺流程。析盐罐内真空减压蒸发水,温度宜控制为
(4)请你设计由二氧化硫生产
 的转化路径,
的转化路径, 化合为+6价硫的化合物)
化合为+6价硫的化合物)
您最近一年使用:0次
【推荐3】已知溶解度和溶解性有关系,20℃时a、b、c三种物质的溶解度曲线如图所示,求:______ 溶液。
(2)c在水中的溶解度随温度的变化趋势与_______相似(填序号)。
(3)某温度时,将b的饱和溶液升温______ (填“一定”或“不一定”)能形成不饱和溶液。
(4)关于a、b溶液说法正确的是_______(填序号)。
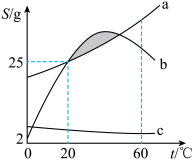
(2)c在水中的溶解度随温度的变化趋势与_______相似(填序号)。
| A.KNO3 | B.NaCl | C.Ca(OH)2 |
(3)某温度时,将b的饱和溶液升温
(4)关于a、b溶液说法正确的是_______(填序号)。
| A.20℃时,可配制质量分数为25%的a溶液 |
| B.使60℃的a饱和溶液析出晶体的方法不止一种 |
| C.阴影区域(不包括b曲线上的点)对应的b溶液为饱和溶液 |
| D.将20℃时a、b、c三种物质的饱和溶液升温至60℃,则60℃时a、b、c的溶质质量分数的关系为:Wa=Wb>Wc |
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
名校
【推荐1】Ⅰ.知物质甲乙丙及CuSO4的溶解度曲线如图所示:
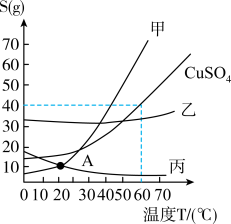
(1)对于处于 A 点的甲丙两物质的溶液,有关说法不正确的是(填编号)___________ 。
①都是饱和溶液; ②甲丙溶解度相等;
③溶液质量分数相等; ④溶液总质量相等;
⑤升温甲变为不饱和溶液,丙中析出固体
(2)若甲中混有少量的杂质乙,则除去乙的正确方法是(填编号)________ 。
①蒸发结晶 ②降温结晶 ③溶解过滤
(3)60℃时,CuSO4饱和溶液中溶质的质量百分数为(保留一位小数)__________ 。
(4)若将 16g 无水CuSO4加入足量CuSO4饱和溶液中,则析出CuSO45H2O 晶体的质量为(填编号)_____________ 。
①等于 16g ②大于 16 g 小于 25 g ③大于 25 g ④等于 25 g ⑤小于 25 g
Ⅱ.已知Cu2H2SO4 (浓) CuSO4SO22H2O 若将 36g Cu 和CuO 的混合物完全溶于过量热的浓 H2SO4中,冷却后加入水中稀释后再加入过量铁屑充分反应,放出气体质量为 1g,过滤洗涤干燥称重固体质量比加入的铁屑质量减少 24g,则原混合物中Cu 的质量为
CuSO4SO22H2O 若将 36g Cu 和CuO 的混合物完全溶于过量热的浓 H2SO4中,冷却后加入水中稀释后再加入过量铁屑充分反应,放出气体质量为 1g,过滤洗涤干燥称重固体质量比加入的铁屑质量减少 24g,则原混合物中Cu 的质量为________________ g。

(1)对于处于 A 点的甲丙两物质的溶液,有关说法不正确的是(填编号)
①都是饱和溶液; ②甲丙溶解度相等;
③溶液质量分数相等; ④溶液总质量相等;
⑤升温甲变为不饱和溶液,丙中析出固体
(2)若甲中混有少量的杂质乙,则除去乙的正确方法是(填编号)
①蒸发结晶 ②降温结晶 ③溶解过滤
(3)60℃时,CuSO4饱和溶液中溶质的质量百分数为(保留一位小数)
(4)若将 16g 无水CuSO4加入足量CuSO4饱和溶液中,则析出CuSO45H2O 晶体的质量为(填编号)
①等于 16g ②大于 16 g 小于 25 g ③大于 25 g ④等于 25 g ⑤小于 25 g
Ⅱ.已知Cu2H2SO4 (浓)
 CuSO4SO22H2O 若将 36g Cu 和CuO 的混合物完全溶于过量热的浓 H2SO4中,冷却后加入水中稀释后再加入过量铁屑充分反应,放出气体质量为 1g,过滤洗涤干燥称重固体质量比加入的铁屑质量减少 24g,则原混合物中Cu 的质量为
CuSO4SO22H2O 若将 36g Cu 和CuO 的混合物完全溶于过量热的浓 H2SO4中,冷却后加入水中稀释后再加入过量铁屑充分反应,放出气体质量为 1g,过滤洗涤干燥称重固体质量比加入的铁屑质量减少 24g,则原混合物中Cu 的质量为
您最近一年使用:0次
【推荐2】下图1为甲、乙两种固体物质的溶解度曲线。

(1)溶解度随温度升高而增大的物质是___________ (填“甲”或“乙”)。
(2)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是___________ (填字母)。向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量分数为___________ (结果精确到0.1%)。
(3)将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲___________ 乙(填“<”、“=”或“>”)。
(4)若固体甲中含少量固体乙,可采用___________ 结晶的方法提纯甲。
(5)若甲为KNO3,如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向烧杯中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的___________(填字母序号)。
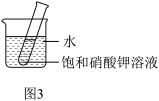

(1)溶解度随温度升高而增大的物质是
(2)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是
(3)将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲
(4)若固体甲中含少量固体乙,可采用
(5)若甲为KNO3,如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向烧杯中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的___________(填字母序号)。

| A.氢氧化钠固体 | B.生石灰固体 | C.冰块 | D.酒精 | E.浓硫酸 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐3】下图是A、B、C三种固体物质的溶解度曲线,据图回答下列问题:
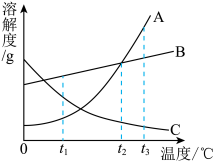
(1)t1°C时,A、B、 C三种物质的溶解度由小到大的顺序是___________ ;
(2)t1°C时,将C的不饱和溶液转化为该温度下的饱和溶液的一种方法是___________ ;
(3)在t3°C时,将等质量的A、B、C三种固体物质完全溶于水,分别配制成该温度下的饱和溶液,所得溶液质量最多的是___________ ;
(4)分别将t1°C时等质量的A、B、C三种物质的饱 和溶液升温至t2°C (忽略水分的蒸发),对所得溶液的叙述不正确的是___________ (填序号)。
①溶剂质量: A>C>B ②溶质质量: A<B
③溶质质量分数: A=B>C ④都是饱和溶液

(1)t1°C时,A、B、 C三种物质的溶解度由小到大的顺序是
(2)t1°C时,将C的不饱和溶液转化为该温度下的饱和溶液的一种方法是
(3)在t3°C时,将等质量的A、B、C三种固体物质完全溶于水,分别配制成该温度下的饱和溶液,所得溶液质量最多的是
(4)分别将t1°C时等质量的A、B、C三种物质的饱 和溶液升温至t2°C (忽略水分的蒸发),对所得溶液的叙述不正确的是
①溶剂质量: A>C>B ②溶质质量: A<B
③溶质质量分数: A=B>C ④都是饱和溶液
您最近一年使用:0次



