氯化钠是一种重要的资源,在海水中储量很丰富.

(1)晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程:
已知B溶液恰好是氯化钠的饱和溶液,与B溶液中溶质质量相等的溶液是_________ (填编号);与B溶液中溶质质量分数相等的溶液是 _________ (填编号).
(2)氯化钠、硝酸钾、硒酸镉的溶解度曲线如图2所示.据图回答:
溶解度变化受温度影响最大的是_________ .t℃时,将25g硒酸镉加入 _______ g水中,完全溶解后,恰好得到饱和溶液.要进一步提高该溶液的溶质质量分数,可进行的操作是 ____________________ .
(3)硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是___________ .

(1)晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程:
已知B溶液恰好是氯化钠的饱和溶液,与B溶液中溶质质量相等的溶液是
(2)氯化钠、硝酸钾、硒酸镉的溶解度曲线如图2所示.据图回答:
溶解度变化受温度影响最大的是
(3)硝酸钾溶液中含有少量氯化钠杂质,提纯的方法是
2014·上海·中考真题 查看更多[5]
更新时间:2016-11-28 12:16:37
|
相似题推荐
【推荐1】下图是氯化钠和硝酸钾两种固体的溶解度曲线。

(1) 时,两种物质的饱和溶液中溶质的质量分数
时,两种物质的饱和溶液中溶质的质量分数______ (填“相等”或“不相等”)。
(2)若硝酸钾中混有少量氯化钠,提纯方法为______ 。
(3)60℃时,将50g质量分数为20%的硝酸钾溶液稀释为10%,需加水______ g。

(1)
 时,两种物质的饱和溶液中溶质的质量分数
时,两种物质的饱和溶液中溶质的质量分数(2)若硝酸钾中混有少量氯化钠,提纯方法为
(3)60℃时,将50g质量分数为20%的硝酸钾溶液稀释为10%,需加水
您最近一年使用:0次
【推荐2】溶液在日常生产、工农业生产和科学研究中具有广泛的用途。
(1)碘酒用于杀菌消毒,其溶剂是___ (填化学式)。
(2)如图为硝酸钾和氯化钠的溶解度曲线示意图。

①P点表示的含义是_____ 。
②t2℃时,将55g硝酸钾加入到60g水中,充分搅拌后所得溶液的质量是___ g。
③若硝酸钾中混有少量氯化钠,可用___ 的方法提纯。
(1)碘酒用于杀菌消毒,其溶剂是
(2)如图为硝酸钾和氯化钠的溶解度曲线示意图。

①P点表示的含义是
②t2℃时,将55g硝酸钾加入到60g水中,充分搅拌后所得溶液的质量是
③若硝酸钾中混有少量氯化钠,可用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲和乙两种物质的溶解度曲线如图所示。
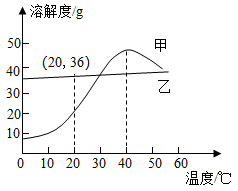
(1)请写出图像中(20,36)表达的含义______ 。
(2)在40℃时,若把甲的不饱和溶液变成饱和溶液,在保持溶质质量分数不变的情况下可采取的方法为______ 、______ 。(两种方法)
(3)在生产生活中,我们常常采取______ 获得乙物质晶体。

(1)请写出图像中(20,36)表达的含义
(2)在40℃时,若把甲的不饱和溶液变成饱和溶液,在保持溶质质量分数不变的情况下可采取的方法为
(3)在生产生活中,我们常常采取
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】如图为A、B、C三种物质的溶解度曲线。请根据图回答:

(1)N点的意义:______
(2)t1℃时,在25g水中放入20g A 物质,形成的A溶液溶质质量分数是_________ ,要使该溶液变为不饱和溶液可采用的方法 ________ (填一种即可)
(3)t2℃时,将等质量的A、B、C三种物质的饱和溶液,降温至t1℃,析出晶体最多的是______ ,没有晶体析出的是______ 。
(4)t2℃时,将等质量的A、B、C三种物质的饱和溶液,均恒温蒸发等质量的水,析出晶体由多到少的顺序为________________ ;
(5)欲将混有少量B的A物质提纯,可以采取的措施是____________________ 。
(6)t2℃时,将A、B、C的饱和溶液降温至t1℃,A、B、C的溶液溶质质量分数大小关系是_______________ 。
(7)上图中可能是气态物质的溶解度曲线是________ 。

(1)N点的意义:
(2)t1℃时,在25g水中放入20g A 物质,形成的A溶液溶质质量分数是
(3)t2℃时,将等质量的A、B、C三种物质的饱和溶液,降温至t1℃,析出晶体最多的是
(4)t2℃时,将等质量的A、B、C三种物质的饱和溶液,均恒温蒸发等质量的水,析出晶体由多到少的顺序为
(5)欲将混有少量B的A物质提纯,可以采取的措施是
(6)t2℃时,将A、B、C的饱和溶液降温至t1℃,A、B、C的溶液溶质质量分数大小关系是
(7)上图中可能是气态物质的溶解度曲线是
您最近一年使用:0次
【推荐3】下表是氯化钠和氯化铵在不同温度下的溶解度。
请回答下列问题:
(1)40℃时,NaCl的溶解度是______ ;
(2)使NH4Cl的饱和溶液变为不饱和溶液,可采用的一种方法是______ ;
(3)根据上表数据分析:NaCl和NH4Cl溶解度曲线相交的温度范围是______ 。(填序号)
①0℃-10℃ ②10℃-20℃ ③20℃-30℃ ④30℃-40℃
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
(1)40℃时,NaCl的溶解度是
(2)使NH4Cl的饱和溶液变为不饱和溶液,可采用的一种方法是
(3)根据上表数据分析:NaCl和NH4Cl溶解度曲线相交的温度范围是
①0℃-10℃ ②10℃-20℃ ③20℃-30℃ ④30℃-40℃
您最近一年使用:0次
【推荐1】化学与人类生活、生产活动息息相关,根据所学化学知识回答下列问题:
(1)碘酒是一种常见的消毒剂,碘酒中的溶剂是_______ 。(填化学式)
(2)打开汽水瓶盖时,汽水会自动喷出来,这说明气体在水中的溶解度与_______ 有关。
(3)如图是M、N两种固体物质的溶解度曲线。

①c点的意义_______
②对于M溶液,可通过_______ 方法实现从d点到c点的转化。
③t2℃时,等质量的M、N两种物质的饱和溶液中,溶剂质量关系是M_______ N(填写“ ”“
”“ ”或“
”或“ ”)
”)
④将t2℃时,将等质量的M、N两种物质的饱和溶液都降温到t1℃,两种溶液中溶质的质量分数关系是M_______ N(填写“ ”“
”“ ”或“
”或“ ”)
”)
⑤N中含有少量M,要提纯N可采用的方法是_______ 。
(1)碘酒是一种常见的消毒剂,碘酒中的溶剂是
(2)打开汽水瓶盖时,汽水会自动喷出来,这说明气体在水中的溶解度与
(3)如图是M、N两种固体物质的溶解度曲线。

①c点的意义
②对于M溶液,可通过
③t2℃时,等质量的M、N两种物质的饱和溶液中,溶剂质量关系是M
 ”“
”“ ”或“
”或“ ”)
”)④将t2℃时,将等质量的M、N两种物质的饱和溶液都降温到t1℃,两种溶液中溶质的质量分数关系是M
 ”“
”“ ”或“
”或“ ”)
”)⑤N中含有少量M,要提纯N可采用的方法是
您最近一年使用:0次
【推荐2】如图所示是甲、乙两种固体物质的溶解度曲线。将0℃时甲、乙的饱和溶液升温至10℃,两种溶液的溶质质量分数的大小关系为甲______ (填“>”“<”或“=”)乙;30℃时,将80g甲的饱和溶液稀释为溶质质量分数为10%的溶液,需加水的质量为_____ g;若量取水时仰视量筒读数,会导致所配溶液的溶质质量分数______ (填“偏大”“偏小”成“不变”)。


您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐3】如图是A、B两种固体(不含结晶水)物质的溶解度曲线,依图回答:
①____ ℃时,A、B两物质的溶解度相等;
②t1℃时,将A、B各m g分别加到均盛有50g水的两只小烧杯中,充分搅拌后,若其中有一个烧杯中有固体剩余,则该物质是____ (填“A”或“B”);
③t3℃时,A物质饱和溶液的溶质的质量分数为____ ;在不改变溶质质量分数的情况下,将该A的饱和溶液变为不饱和溶液的方法是____ ;
④烧杯中盛有一定质量、温度为80℃、溶质为A的溶液,将其置于室温环境中,测定不同温度时析出固体A的质量.测定结果记录如下表.
不考虑水蒸发,则65℃时,该溶液是否为饱和溶液?____ (填“是”、“否”或“无法判断”).
⑤根据如图A、B两种固体物质的溶解度曲线,下列说法错误的是____ .

A t2℃时,A、B两物质的溶液中所含的溶质相同
B t2℃时,A、B饱和溶液的溶质质量分数相同
C t3℃时,A、B的饱和溶液降温至t2℃,A 析出的固体比B多
D t3℃时,A、B的饱和溶液降温至t2℃,A、B所含的溶剂质量不变.
①
②t1℃时,将A、B各m g分别加到均盛有50g水的两只小烧杯中,充分搅拌后,若其中有一个烧杯中有固体剩余,则该物质是
③t3℃时,A物质饱和溶液的溶质的质量分数为
④烧杯中盛有一定质量、温度为80℃、溶质为A的溶液,将其置于室温环境中,测定不同温度时析出固体A的质量.测定结果记录如下表.
| 溶液的温度/℃ | 75 | 65 | 50 | 35 | 20 |
| 析出固体A的质量/g | 0 | 0 | 2.0 | 4.5 | 8.4 |
⑤根据如图A、B两种固体物质的溶解度曲线,下列说法错误的是

A t2℃时,A、B两物质的溶液中所含的溶质相同
B t2℃时,A、B饱和溶液的溶质质量分数相同
C t3℃时,A、B的饱和溶液降温至t2℃,A 析出的固体比B多
D t3℃时,A、B的饱和溶液降温至t2℃,A、B所含的溶剂质量不变.
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】从海水中提取食盐的方法主要为盐田法,这是一种古老而至今仍广泛沿用的方法。海水晒盐的流程如下:


(1)海水晒盐后得到的母液是当时温度下氯化钠的______ 溶液(填“饱和”或“不饱和”)。
(2)如图是A、B两种物质的溶解度曲线,回答下列问题:
①t2℃时,A的饱和溶液中溶质的质量分数为______ 。
②若A物质中含有少量B物质,可用______ 的方法提纯A。
③将t2℃时B的饱和溶液降低温度,溶液中溶质的质量分数______ (填“变大”、“变小”或“不变”)。


(1)海水晒盐后得到的母液是当时温度下氯化钠的
(2)如图是A、B两种物质的溶解度曲线,回答下列问题:
①t2℃时,A的饱和溶液中溶质的质量分数为
②若A物质中含有少量B物质,可用
③将t2℃时B的饱和溶液降低温度,溶液中溶质的质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】下图是甲、乙两种物质的溶解度曲线,请结合下图回答问题:
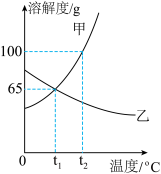
(1)溶解度随温度升高而降低的物质是_____ ;
(2)可使甲物质从其饱和溶液中结晶析出的方法是_____ ;
(3)t2℃时,将60克甲物质放入50克水中,形成溶液的质量为_____ 克,溶质质量分数为_____ ;
(4)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数_____ (填“大于”“等于”或“小于”)乙溶液的溶质质量分数。

(1)溶解度随温度升高而降低的物质是
(2)可使甲物质从其饱和溶液中结晶析出的方法是
(3)t2℃时,将60克甲物质放入50克水中,形成溶液的质量为
(4)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是a、b、c三种物质的溶解度曲线,请结合图示回答问题:

(1)P点的含义为___________ 。
(2)t3℃时,50g物质a放入50g水中形成的溶液中溶质和溶剂的质量比为___________ 。
(3)下列说法正确的是___________。
(4)保持温度不变,将c的不饱和溶液转化成c的饱和溶液的一种方法是___________ 。

(1)P点的含义为
(2)t3℃时,50g物质a放入50g水中形成的溶液中溶质和溶剂的质量比为
(3)下列说法正确的是___________。
| A.在t1℃时,等质量的a、b、c三种物质的饱和溶液中,所含溶剂质量由大到小的顺序为a>b>c |
| B.t2℃时,b的饱和溶液溶质的质量分数一定比a、c的溶液溶质的质量分数大 |
| C.将t3℃时,a、c的饱和溶液分别降温至t2℃,此时两溶液中溶质的质量分数相等 |
| D.当a中混有少量b时,可用降温结晶的方法提纯a |
(4)保持温度不变,将c的不饱和溶液转化成c的饱和溶液的一种方法是
您最近一年使用:0次




