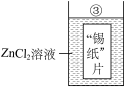
“锡纸烤鸡蛋”是一种特色小吃,它的一种做法是用“锡纸”包裹住鸡蛋,在炭火上烘烤。学习金属的相关知识后,化学小组对使用的“锡纸”产生了兴趣,查阅资料发现,“锡纸”实际上是金属铝箔。他们产生了疑惑:是铝还是锡呢?于是进行如下实验探究。
【提出问题】“锡纸”中的金属是铝还是锡?
【查阅资料】锡(Sn)与酸或金属的化合物溶液反应生成+2价的锡的化合物。
【做出假设】猜想I:“锡纸”中的金属是锡 猜想Ⅱ:“锡纸”中的金属是铝
【进行实验】
(1)实验过程中使用的金属均已打磨过,其目的是______ 。
【反思评价】
(2)下列物质的溶液可以替代实验二中的氯化锌溶液完成上述实验的是_____(填序号)。
(3)有的同学提出:“锡纸”中的金属为什么不是镁呢?我们根据已有的知识和经验可以直接判断不是镁,因为_____ 。
【实验拓展】
(4)对实验事实进行归纳概括是提炼物质性质的基本方法之一。
【提出问题】“锡纸”中的金属是铝还是锡?
【查阅资料】锡(Sn)与酸或金属的化合物溶液反应生成+2价的锡的化合物。
【做出假设】猜想I:“锡纸”中的金属是锡 猜想Ⅱ:“锡纸”中的金属是铝
【进行实验】
(1)实验过程中使用的金属均已打磨过,其目的是
| 实验序号 | 实验操作 | 实验现象 | 实验分析与结论 |
| 实验一 |
| 猜想 | |
| 实验二 |
| ③中有固体析出 |
【反思评价】
(2)下列物质的溶液可以替代实验二中的氯化锌溶液完成上述实验的是_____(填序号)。
| A.硫酸钠 | B.硫酸亚铁 | C.氯化铜 | D.硝酸银 |
【实验拓展】
(4)对实验事实进行归纳概括是提炼物质性质的基本方法之一。
| 归纳项目 | 适用方法 | 比较金属 |
| 金属活动性比较 | 与同一种物质发生反应的剧烈程度 | 镁、铁 |
| 与稀硫酸或稀盐酸是否反应 | 铁、铜 | |
| 与 | 铝、锌 |
更新时间:2024-03-15 09:09:37
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】小明同学为了探究铜、铁、银三种金属的活动性强弱,做了如下实验。他找来一块铜片,用砂纸打磨干净,然后分别在a、b、c三处滴上不同的溶液:

①在a处滴上稀HCl ;②在b处滴上FeSO4溶液 ;③在c处滴上AgNO3溶液.一段时间后观察a、b、c三处,无明显变化的地方是_____ ;写出有明显现象的地方所涉及的化学反应方程式:___________ ;以上实验中,你认为小明不必要进行的是____ (选填“①”“②”或“③”);据此实验,你认为小明得出的金属活动性正确结论的是_________ .

①在a处滴上稀HCl ;②在b处滴上FeSO4溶液 ;③在c处滴上AgNO3溶液.一段时间后观察a、b、c三处,无明显变化的地方是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】学习了金属的性质之后,同学们决定用实验对铁、铝、铜三种金属的活动性顺序进行验证.
 实验一
实验一 将粗细相同的铁丝、铝丝、铜丝分别插入相同的稀盐酸中:
将粗细相同的铁丝、铝丝、铜丝分别插入相同的稀盐酸中:
 讨论交流
讨论交流 铝丝在稀盐酸中短时间内无气泡,而一段时间后反应剧烈,是因为
铝丝在稀盐酸中短时间内无气泡,而一段时间后反应剧烈,是因为 ______  做金属性质实验前需先将金属进行打磨,目的是
做金属性质实验前需先将金属进行打磨,目的是 ______  实验中用到的“相同”盐酸指的是
实验中用到的“相同”盐酸指的是 ______ 相同.
 反思评价
反思评价 若不认真分析现象可能导致错误的结论.
若不认真分析现象可能导致错误的结论.
 实验二
实验二 为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中,欲通过实验现象得出金属活动性顺序.
为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中,欲通过实验现象得出金属活动性顺序.
实验过程中能看到:硫酸铝溶液中的铁丝表面______ ,硫酸铜溶液中的铁丝表面 ______ ,反应的化学方程式 ______ .
 实验一
实验一 将粗细相同的铁丝、铝丝、铜丝分别插入相同的稀盐酸中:
将粗细相同的铁丝、铝丝、铜丝分别插入相同的稀盐酸中:| 操作 |  |  |  |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
 讨论交流
讨论交流 铝丝在稀盐酸中短时间内无气泡,而一段时间后反应剧烈,是因为
铝丝在稀盐酸中短时间内无气泡,而一段时间后反应剧烈,是因为  做金属性质实验前需先将金属进行打磨,目的是
做金属性质实验前需先将金属进行打磨,目的是  实验中用到的“相同”盐酸指的是
实验中用到的“相同”盐酸指的是  反思评价
反思评价 若不认真分析现象可能导致错误的结论.
若不认真分析现象可能导致错误的结论. 实验二
实验二 为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中,欲通过实验现象得出金属活动性顺序.
为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中,欲通过实验现象得出金属活动性顺序.实验过程中能看到:硫酸铝溶液中的铁丝表面
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】化学兴趣小组为了探究金属与盐溶液发生置换反应的规律,进行了下列实验活动:
【提出问题】一种金属跟多种盐的混合溶液发生置换反应的规律是什么?
【实验探究】小组同学设计实验进行探究。
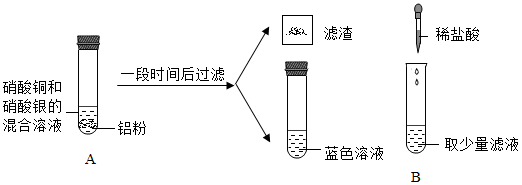
【实验分析】石建认真观察了滤渣和滤液,并取少量蓝色滤液于B试管中,滴加适量稀盐酸,没有观察到明显现象,确定滤液中一定没有的溶质是__ ,据此推断A中一定发生反应的化学方程式为__ ,因而确定了反应顺序。秦思另取少量蓝色滤液,重新加入过量的铝粉,充分反应,观察到的现象为__ 。加入铝粉过程中,滤液中Cu2+数目的变化趋势曲线应该是___ (如图,填序号)。
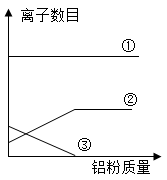
【实验结论】通过上述实验,同学们初步得出金属与盐溶液反应的规律。
【拓展延伸】通过查阅资料,小组同学了解到金属与盐在溶液中发生置换反应的实质是:金属原子与溶液中的金属离子之间发生了电子得失(转移),溶液中金属离子得电子能力越强,其对应金属的活动性越弱。据此可推断上述实验中涉及的三种金属离子得电子能力由强到弱依次是______ 。
【探究感悟】在此次探究活动中同学们再次认识到:证明物质发生化学反应,可根据明显的实验现象证明有其他物质生成或______ 。
【提出问题】一种金属跟多种盐的混合溶液发生置换反应的规律是什么?
【实验探究】小组同学设计实验进行探究。

【实验分析】石建认真观察了滤渣和滤液,并取少量蓝色滤液于B试管中,滴加适量稀盐酸,没有观察到明显现象,确定滤液中一定没有的溶质是

【实验结论】通过上述实验,同学们初步得出金属与盐溶液反应的规律。
【拓展延伸】通过查阅资料,小组同学了解到金属与盐在溶液中发生置换反应的实质是:金属原子与溶液中的金属离子之间发生了电子得失(转移),溶液中金属离子得电子能力越强,其对应金属的活动性越弱。据此可推断上述实验中涉及的三种金属离子得电子能力由强到弱依次是
【探究感悟】在此次探究活动中同学们再次认识到:证明物质发生化学反应,可根据明显的实验现象证明有其他物质生成或
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某化学实验小组用一块表面镀锌的铁样品进行实验探究活动。
【实验探究】将表面镀锌的铁进行如图A实验,加入稀盐酸与产生氢气的质量关系如图B。

【提出问题】反应后所得的无色滤液a的溶质与固体b的成分是什么?
【猜想假设】秦思认为无色滤液a的溶质是_________ 、氯化亚铁和氯化氢。
【反思评价】请你评价秦思的猜想_________ 。
【推理判断】由无色滤液a 的成分可推知,固体b中一定含有_______ 。
【实验与结论】为验证固体b的成分,单杰向b的样品中加入一种有色物质_______ (填化学式)溶液,产生的现象是 ______________ ,据此现象,证明出固体b中的两种成分,同时得出这两种金属的活动性顺序。
【表达交流】石建向固体b中继续滴加少量稀盐酸也确定出固体b的成分,他观察到的现象是_______________________ 。
【拓展延伸】通过比较锌、铁的活动性,结合图像B在开始加入稀盐酸的过程中并没有产生氢气的现象,你认为在铁的表面镀锌的原因是_________ ,可阻止进一步氧化。
【实验探究】将表面镀锌的铁进行如图A实验,加入稀盐酸与产生氢气的质量关系如图B。

【提出问题】反应后所得的无色滤液a的溶质与固体b的成分是什么?
【猜想假设】秦思认为无色滤液a的溶质是
【反思评价】请你评价秦思的猜想
【推理判断】由无色滤液a 的成分可推知,固体b中一定含有
【实验与结论】为验证固体b的成分,单杰向b的样品中加入一种有色物质
【表达交流】石建向固体b中继续滴加少量稀盐酸也确定出固体b的成分,他观察到的现象是
【拓展延伸】通过比较锌、铁的活动性,结合图像B在开始加入稀盐酸的过程中并没有产生氢气的现象,你认为在铁的表面镀锌的原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】为研究铝和铜的金属活动性,某研究小组进行了如下探究。
(1)小明设计的实验方案是:先用砂纸打磨铝片和铜片,“打磨”的目的是______ ,然后再将打磨干净的铝片和铜片分别放入稀盐酸中,观察反应的现象。写出铝与稀盐酸反应的化学方程式:______ 。
(2)小芳将打磨干净的铝片放入浓氯化铜溶液中,看到有大量气泡逸出,且在一段时间内气泡越来越快,经点燃能发出爆鸣声,说明生成的气体是______ 。
(3)小芳在(2)实验中,还观察到铝片与浓氯化铜溶液反应时还有“白色沉淀”这一异常现象出现。
【提出问题】铝片与浓氯化铜溶液反应出现的白色沉淀的组成是什么?
【查阅资料】①AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。
②CuCl为白色固体,不溶于水、乙醇:溶于浓盐酸且溶液变褐色;溶于浓氨水且溶液变蓝色。
【提出假设】。假设a:该白色沉淀可能含有CuCl:
假设b:该白色沉淀可能含有AlCl3:
假设c:该白色沉淀可能含有Al。
【设计实验】取白色沉淀分别进行如下实验。
【得出结论】由实验①可判断假设c不成立,再结合实验②和③可得出该白色沉淀的成分是______ 。
【反思评价】为探究铝与氯化铜溶液反应生成CuCl的条件,小组同学查阅相关资料发现:铝和氯化铜溶液反应分两步: 。
。
请对生成CuCl的条件提出猜想______ ;设计实验证明猜想(写出实验方案、可能现象)______ 。
(1)小明设计的实验方案是:先用砂纸打磨铝片和铜片,“打磨”的目的是
(2)小芳将打磨干净的铝片放入浓氯化铜溶液中,看到有大量气泡逸出,且在一段时间内气泡越来越快,经点燃能发出爆鸣声,说明生成的气体是
(3)小芳在(2)实验中,还观察到铝片与浓氯化铜溶液反应时还有“白色沉淀”这一异常现象出现。
【提出问题】铝片与浓氯化铜溶液反应出现的白色沉淀的组成是什么?
【查阅资料】①AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。
②CuCl为白色固体,不溶于水、乙醇:溶于浓盐酸且溶液变褐色;溶于浓氨水且溶液变蓝色。
【提出假设】。假设a:该白色沉淀可能含有CuCl:
假设b:该白色沉淀可能含有AlCl3:
假设c:该白色沉淀可能含有Al。
【设计实验】取白色沉淀分别进行如下实验。
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量浓盐酸 | |
| ② | 加入适量无水乙醇 | 固体部分溶解 |
| ③ | 加入适量 | 固体溶解,得到蓝色溶液 |
【反思评价】为探究铝与氯化铜溶液反应生成CuCl的条件,小组同学查阅相关资料发现:铝和氯化铜溶液反应分两步:
 。
。请对生成CuCl的条件提出猜想
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
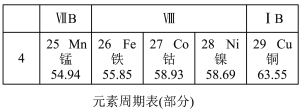
【推荐3】小倩同学了解到:外国人把中国称为“China”,在英文中与瓷器是同一个单词。“青花瓷”又是在中国瓷器中最具代表性的。绘制青花瓷纹饰的原料中主要含有氧化钴(CoO)。
她查阅元素周期表发现钴【读音: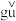 】元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
】元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
【提出问题】小倩同学产生疑问:为什么钴和铁都在第Ⅷ族呢?
【寻求帮助】
(1)咨询老师得知:因为铁与钴两种元素原子的结构具有相同点(见如图),使得二者的化学性质相似。因此把这两种元素放在一起。请你帮助小倩完成下列问题:
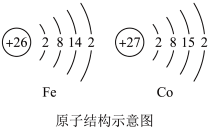
①钴元素在元素周期表中的原子序数为______
②铁原子与钴原子具有相同的______ (填序号,下同)。元素的化学性质主要与原子的______ 有关,因此二者的化学性质相似。
a.核电荷数 b.核外电子数
c.电子层数 d.最外层电子数
③在化学反应中,金属钴和铁一样,也能与稀盐酸发生反应放出氢气,反应的化学方程式为______ ;钴在氧气中燃烧生成Co3O4,化学方程式为______ 。
【深入探讨】
(2)查阅资料,钴及其化合物的相关性质如下:
根据你所学知识,预测金属钴化学性质,说明预测的依据,并设计实验验证。
限选试剂是:金属钴片各几片(用砂纸打磨光亮)、硫酸铝溶液、硫酸镁溶液、氯化铜溶液、稀硫酸溶液。
【产生问题】既然钴与铁的单质具有相似的性质,那么两种元素的化合物是否也有相似的化学性质?
【设计并实验验】
根据所学知识,同学们已知下列反应可以进行,并进行实验: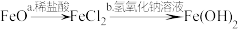
观察记录实验现象:氧化亚铁为黑色固体;实验a中,随着稀盐酸的加入,黑色固体逐渐溶解,溶液呈现浅绿色;实验b中,加入氢氧化钠溶液后出现白色沉淀,静置在空气中,沉淀物颜色发生变化,最后变为红褐色。【查阅资料得知:原因是溶液中的Fe(OH)2遇空气中的氧气生成Fe(OH)3】
(3)同学们欲探究钴元素化合物的性质,设计并进行了如下实验:
请你依据实验现象,完成下列问题:
I、实验①中,取少量灰黑色的氧化钴放入试管中,加入稀盐酸,固体被溶解,溶液呈红色,写出反应的化学方程式______ 。另取一支试管加入少量氧化钴,滴入浓盐酸,固体被溶解、溶液呈绿色。说明反应后钴离子在溶液中呈现的颜色与加入酸的______ 有关。
Ⅱ、实验②中,加入氢氧化钠溶液,出现青蓝色沉淀。将试管静置在空气中,沉淀物颜色发生变化,最终变为棕色,试推测沉淀物颜色变化可能与空气中的______ 有关。通过实验探究,同学们得出结论:铁和钴两种元素的化合物化学性质相似。
她查阅元素周期表发现钴【读音:
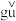 】元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
】元素符号为Co,在周期表中与铁元素同位于第4周期、第Ⅷ族。
【提出问题】小倩同学产生疑问:为什么钴和铁都在第Ⅷ族呢?
【寻求帮助】
(1)咨询老师得知:因为铁与钴两种元素原子的结构具有相同点(见如图),使得二者的化学性质相似。因此把这两种元素放在一起。请你帮助小倩完成下列问题:

①钴元素在元素周期表中的原子序数为
②铁原子与钴原子具有相同的
a.核电荷数 b.核外电子数
c.电子层数 d.最外层电子数
③在化学反应中,金属钴和铁一样,也能与稀盐酸发生反应放出氢气,反应的化学方程式为
【深入探讨】
(2)查阅资料,钴及其化合物的相关性质如下:
| 物质 | Co | Co2CO3 | Co3O4 | CoCl2 | CoSO4 |
| 在水中的溶解性 | 难溶于水的银白色固体 | 难溶于水的灰黑色粉末 | 难溶于水的黑色固体 | 易溶于水形成粉红色溶液 | 易溶于水成粉红色溶液 |
限选试剂是:金属钴片各几片(用砂纸打磨光亮)、硫酸铝溶液、硫酸镁溶液、氯化铜溶液、稀硫酸溶液。
| 预测 | 预测的依据 | 验证预测的实验操作与预期现象 |
| ①金属钴能够与A的溶液反应。 | 金属活动性顺序中:Fe>H,钴的金属活动性与铁相似。 | 取一片钴片于试管中,加入适量的 |
| ②金属钴能够与B的溶液反应。 | 取一片钴片于试管中,加入适量的 |
【产生问题】既然钴与铁的单质具有相似的性质,那么两种元素的化合物是否也有相似的化学性质?
【设计并实验验】
根据所学知识,同学们已知下列反应可以进行,并进行实验:
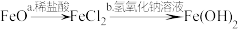
观察记录实验现象:氧化亚铁为黑色固体;实验a中,随着稀盐酸的加入,黑色固体逐渐溶解,溶液呈现浅绿色;实验b中,加入氢氧化钠溶液后出现白色沉淀,静置在空气中,沉淀物颜色发生变化,最后变为红褐色。【查阅资料得知:原因是溶液中的Fe(OH)2遇空气中的氧气生成Fe(OH)3】
(3)同学们欲探究钴元素化合物的性质,设计并进行了如下实验:

请你依据实验现象,完成下列问题:
I、实验①中,取少量灰黑色的氧化钴放入试管中,加入稀盐酸,固体被溶解,溶液呈红色,写出反应的化学方程式
Ⅱ、实验②中,加入氢氧化钠溶液,出现青蓝色沉淀。将试管静置在空气中,沉淀物颜色发生变化,最终变为棕色,试推测沉淀物颜色变化可能与空气中的
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】铜陵被誉为我国的“铜都”。下图是铜陵铜工艺品中著名的四喜娃娃,小明找到了分别用纯铜、青铜(CuSn合金)两种材料制作的四喜娃娃及用于实验的纯铜片和青铜片

(1)怎样用化学方法区分这两种四喜娃娃___________ ?区分纯铜和青铜的实验方法是___________ (2)四喜娃娃为什么生锈了?
通过查阅资料得知,金属铜长时间放置在空气中,能够和空气中氧气等物质发生化学反应,生成铜绿〔Cu2(OH)CO3〕。请你根据铜绿的组成推断,铜变成铜绿时,空气中的O2、
___________ 、______ 参加了反应。(填化学式)
(3)哪种四喜娃娃更容易生锈?
(4)由于有的青铜中含杂质较多,尤其是含铁,故在铜绿间还会有斑驳的、呈褐色的氧化铁。现有一些这种含褐色的锈斑粉末,请你设计实验证明锈斑粉末中含有铁元素___________ 。

(1)怎样用化学方法区分这两种四喜娃娃
通过查阅资料得知,金属铜长时间放置在空气中,能够和空气中氧气等物质发生化学反应,生成铜绿〔Cu2(OH)CO3〕。请你根据铜绿的组成推断,铜变成铜绿时,空气中的O2、

(3)哪种四喜娃娃更容易生锈?
小明发现从不同地 点收集到的两个四喜娃娃中,青铜娃娃身上的锈斑比纯铜的多,他据此得出结论:青铜比纯铜更容
点收集到的两个四喜娃娃中,青铜娃娃身上的锈斑比纯铜的多,他据此得出结论:青铜比纯铜更容 易生锈。
易生锈。
他的这种推理方法是否科学
(4)由于有的青铜中含杂质较多,尤其是含铁,故在铜绿间还会有斑驳的、呈褐色的氧化铁。现有一些这种含褐色的锈斑粉末,请你设计实验证明锈斑粉末中含有铁元素
您最近一年使用:0次
【推荐2】同学们通过实验来验证Cu、Fe、Ag三种金属的活动性。
实验室提供的药品有:Cu(NO3)2溶液、AgNO3溶液、Fe(NO3)2溶液、稀硫酸、铜丝、铁丝、银丝、铝丝。
I、小华同学设计并完成了如下实验:
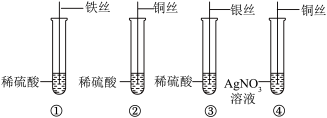
(1)你认为小华所做的实验______ (填序号)是多余的,实验①反应现象为______ ,实验④反应的化学反应方程式为______ 。
Ⅱ、小贝只选用了上述药品中的三种,通过两步实验,也达到了实验目的。
(2)他选用的三种药品是______ (写出一种药品组合即可)。
Ⅲ、取一定量的铝丝放入盛有Cù(NO3)2和AgNO3混合溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。
【提出问题】滤液中所含金属化合物是什么?
【猜想假设】同学们对滤液中所含的成分作出多种猜想:
猜想一:只有A1(NO3)3
猜想二:Cu(NO3)2、A1(NO3)3
猜想三:AgNO3、Al(NO3)3
猜想四:Cu(NO3)2、AgNO3、Al(NO3)3
(3)经过讨论,同学们一致认为猜想______ 一定不正确。
【实验验证】
(4)将实验方案补充完整:
实验室提供的药品有:Cu(NO3)2溶液、AgNO3溶液、Fe(NO3)2溶液、稀硫酸、铜丝、铁丝、银丝、铝丝。
I、小华同学设计并完成了如下实验:

(1)你认为小华所做的实验
Ⅱ、小贝只选用了上述药品中的三种,通过两步实验,也达到了实验目的。
(2)他选用的三种药品是
Ⅲ、取一定量的铝丝放入盛有Cù(NO3)2和AgNO3混合溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。
【提出问题】滤液中所含金属化合物是什么?
【猜想假设】同学们对滤液中所含的成分作出多种猜想:
猜想一:只有A1(NO3)3
猜想二:Cu(NO3)2、A1(NO3)3
猜想三:AgNO3、Al(NO3)3
猜想四:Cu(NO3)2、AgNO3、Al(NO3)3
(3)经过讨论,同学们一致认为猜想
【实验验证】
(4)将实验方案补充完整:
| 实验操作 | 现象 | 结论 |
| 小贝向所得滤渣中滴加稀盐酸 | 若观察到有气泡产生 | 猜想 |
| 小华将铜丝插入所得滤液 | 若观察到 | 猜想四成立 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】为探究铝、铁、铜三种金属的活动性,请完善下表的探究方案,并回答有关问题:
【实验探究】
【实验结论】金属活动性:铝>铁>铜
【实验拓展】
(1)在上述设计的方案中,只要补充一个实验,还可得出铝>铁>氢>铜的结论。要补充的实验操作是______ ;
(2)经过讨论,同学们认为将上述【实验探究】中实验步骤(1)、(2)、(3)中插入金属丝的顺序进行调整(其它操作相同),也可得到铝>铁>氢>铜的结论,你认为调整后插入金属的顺序是______ (填字母)。
A 铝、铁、铜 B 铜、铝、铁 C 铜、铁、铝
【实验探究】
| 实验步骤 | 观察到的现象或化学反应方程式 |
| (1)在试管中取少量盐酸,插入足量铁丝,充分反应。 | 现象为:铁丝表面有气泡生成,溶液由无色变为 |
| (2)在(1)所得的溶液中,插入足量 | 无明显现象 |
| (3)在(2)所得的溶液中插入足量 | 有明显现象,该反应的化学方程式为 |
【实验结论】金属活动性:铝>铁>铜
【实验拓展】
(1)在上述设计的方案中,只要补充一个实验,还可得出铝>铁>氢>铜的结论。要补充的实验操作是
(2)经过讨论,同学们认为将上述【实验探究】中实验步骤(1)、(2)、(3)中插入金属丝的顺序进行调整(其它操作相同),也可得到铝>铁>氢>铜的结论,你认为调整后插入金属的顺序是
A 铝、铁、铜 B 铜、铝、铁 C 铜、铁、铝
您最近一年使用:0次
【推荐1】为研究锌和铝的金属活动性,某研究小组进行了如下探究。
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸。写出锌与盐酸反应的化学方程式:_____ 。
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是_____ 。
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现。
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。
【提出合理假设】假设a:该灰黑色沉淀可能含有_____ ;
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质。
【设计并完成实验】取灰黑色沉淀分别进行如下实验。
【得出结论】由实验①可判断假设c_____ (填“成立”或“不成立”),再结合②和③可得出该灰黑色沉淀的成分是_____ 。
(4)你认为(1)中小明的实验能否比较锌和铝的金属活动性强弱?_____ (填“能”或“不能”),分别从设计方法和操作可行性的角度,具体说明理由:_____ 。
(1)小明设计的实验方案:向表面积相同的铝片和锌粒中分别加入盐酸。写出锌与盐酸反应的化学方程式:
(2)小芳将去膜和未去膜的铝片分别放入盐酸中,发现前者比后者反应快,原因是
(3)小芳在(2)实验中,还观察到有“灰黑色沉淀”这一异常现象出现。
【提出问题】铝与盐酸反应出现的灰黑色沉淀的组成是什么?
【查阅文献】铝在颗粒较小时为灰黑色;AlCl3为无色透明晶体或白色而微带浅黄色的固体,易溶于水和乙醇。
【提出合理假设】假设a:该灰黑色沉淀可能含有
假设b:该灰黑色沉淀可能含有AlCl3;
假设c:该灰黑色沉淀可能含有难溶于酸的物质。
【设计并完成实验】取灰黑色沉淀分别进行如下实验。
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀盐酸 | 有微量气泡,固体全部溶解,得到澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
【得出结论】由实验①可判断假设c
(4)你认为(1)中小明的实验能否比较锌和铝的金属活动性强弱?
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】探究金属性质:金属原子容易失去最外层电子,化学性质活泼。下图为探究金属化学性质的实验。

(1)图甲中反应的化学方程式为________ 。
(2)图1只有乙中不反应,能得出三种金属活动性及它们和氢元素的位置关系,由强到弱的顺序是_________ (填元素符号)。
(3)写出丁中的现象________ ,丙中的方程式_______ 。

(1)图甲中反应的化学方程式为
(2)图1只有乙中不反应,能得出三种金属活动性及它们和氢元素的位置关系,由强到弱的顺序是
(3)写出丁中的现象
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。人类经历了新石器时代、青铜器时代、铁器时代,后来陆续使用了锌、铝、钠、镁等金属。金属材料在生产生活中有不同的用途,发挥着重大的作用。某化学兴趣小组对金属的活动性强弱产生了浓厚的兴趣,在老师的指导下,他们开启了铝、铁、铜三种金属的活动性强弱的探究之旅。请你和他们一起完善下表的探究方案并回答有关问题。
任务一:小明同学设计了用铜丝、铁丝、铝丝和稀硫酸,只用一只试管,取一次硫酸的探究方案
(1)步骤①中发生反应的化学方程式为_______ ;
(2)将铝丝插入前应进行的操作是_________ ,目的是_______ 。
任务二:
小亮同学认为在小明设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论。
小亮要补充的实验是________ 。
任务三:
小强同学认为要得到Al>Fe>H>Cu的结论,不必做补充实验,只需将小明同学的方案中插入金属的顺序调整即可,你认为调整后插入金属丝的顺序是_______ 。
任务一:小明同学设计了用铜丝、铁丝、铝丝和稀硫酸,只用一只试管,取一次硫酸的探究方案
实验步骤 | 实验现象 | 实验结论 |
| 步骤①:在试管中取少量稀硫酸,插入铁丝,充分反应 | 三种金属活动性由强到弱的顺序是: | |
| 步骤②:在①所得的溶液中,插入铜丝,充分反应 | ||
| 步骤③:在②所得的溶液中插入铝丝,充分反应 | 溶液由浅绿色变为无色 |
(2)将铝丝插入前应进行的操作是
任务二:
小亮同学认为在小明设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论。
小亮要补充的实验是
任务三:
小强同学认为要得到Al>Fe>H>Cu的结论,不必做补充实验,只需将小明同学的方案中插入金属的顺序调整即可,你认为调整后插入金属丝的顺序是
您最近一年使用:0次