下图是甲、乙、丙三种固体物质的溶解度曲线,请根据该曲线回答下列问题。
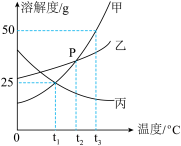
(1) ℃时,
℃时,______ 的溶解度是25g。
(2) ℃时,取甲、乙、丙各25g分别加入盛有100g水的3个烧杯中,充分搅拌后,能够形成饱和溶液的是
℃时,取甲、乙、丙各25g分别加入盛有100g水的3个烧杯中,充分搅拌后,能够形成饱和溶液的是______ 。
(3)将以上甲的溶液升温到 ℃,该溶液中溶质质量分数是
℃,该溶液中溶质质量分数是______ 。若将以上三个烧杯中的溶液都降温到 ℃以下时,溶液浓度相同的两种物质是
℃以下时,溶液浓度相同的两种物质是______ 。

(1)
 ℃时,
℃时,(2)
 ℃时,取甲、乙、丙各25g分别加入盛有100g水的3个烧杯中,充分搅拌后,能够形成饱和溶液的是
℃时,取甲、乙、丙各25g分别加入盛有100g水的3个烧杯中,充分搅拌后,能够形成饱和溶液的是(3)将以上甲的溶液升温到
 ℃,该溶液中溶质质量分数是
℃,该溶液中溶质质量分数是 ℃以下时,溶液浓度相同的两种物质是
℃以下时,溶液浓度相同的两种物质是
更新时间:2024-04-03 16:00:49
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】碳酸锂是生产锂电池的基础材料。以β-锂辉石为原料,其中锂元素(Li)以氧化物的形式存在,含有的主要杂质是氧化镁。用硫酸焙烧法制取碳酸锂的工艺流程(部分试剂和步骤等已略去)如图所示。

(1)下图摘自元素周期表,据此说明锂和钠元素化学性质相似的原因是________ 。

(2)步骤“浸出→滤渣”、“沉锂→母液”这两个过程都要进行的操作是_______ 。
(3)“沉锂”发生反应的化学方程式为_______ 。所得的母液为碳酸锂的______ (填“不饱和"或“饱和”)溶液。
(4)下表为Li2CO3在不同温度下的溶解度(g) 数据,据此判断在“沉锂”后洗涤得到的Li2CO3晶体的方法为:________ 。
(5)Li-SO2电池工作时的反应原理是锂与二氧化硫反应生成Li2S2O4。该电池工作过程中如有28g金属锂参加了反应,则同时消耗二氧化硫的质量________ (写出计算过程)

(1)下图摘自元素周期表,据此说明锂和钠元素化学性质相似的原因是

(2)步骤“浸出→滤渣”、“沉锂→母液”这两个过程都要进行的操作是
(3)“沉锂”发生反应的化学方程式为
(4)下表为Li2CO3在不同温度下的溶解度(g) 数据,据此判断在“沉锂”后洗涤得到的Li2CO3晶体的方法为:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(5)Li-SO2电池工作时的反应原理是锂与二氧化硫反应生成Li2S2O4。该电池工作过程中如有28g金属锂参加了反应,则同时消耗二氧化硫的质量
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】KNO3和KCl在不同温度时的溶解度如表所示。请回答下列问题:
(1)依据上表数据,绘制KNO3 和KCl的溶解度曲线,下图中能表示KNO3溶解度曲线的是_______ (填m 或n )。

(2)小王同学想将80 ℃时的KCl饱和溶液变为不饱和溶液,可以采取的方法是____ (写出其中一种)。
(3)20 ℃时,向10 g 水中加入2.5 g KNO3充分搅拌得到X,再加入2.5 g KNO3充分搅拌得到Y,继续升温至50 ℃得到Z,则X、Y、Z中为饱和溶液的是____ 。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |

(2)小王同学想将80 ℃时的KCl饱和溶液变为不饱和溶液,可以采取的方法是
(3)20 ℃时,向10 g 水中加入2.5 g KNO3充分搅拌得到X,再加入2.5 g KNO3充分搅拌得到Y,继续升温至50 ℃得到Z,则X、Y、Z中为饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
Ⅰ.每年的3月22日是“世界水日”,水与人类的生产、生活密切相关。
(1)水_______ (填“属于”或“不属于”)六大基本营养素之一。
(2)为区分软水和硬水,将等量的_______ 分别滴加到盛有等量软水、硬水的试管中,振荡,试管中产生_________ 的为硬水。生活上常用_______ 的方法来降低水的硬度。
(3)洗涤剂可以清洗掉盘子上的油污,洗涤剂起到_______ 作用。
Ⅱ.如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据如图回答下列问题。

(4)P点的含义是______ 。
(5)大量的b中混有少量的a,提纯b的方法为_______ 。
(6)t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是 。
Ⅰ.每年的3月22日是“世界水日”,水与人类的生产、生活密切相关。
(1)水
(2)为区分软水和硬水,将等量的
(3)洗涤剂可以清洗掉盘子上的油污,洗涤剂起到
Ⅱ.如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据如图回答下列问题。

(4)P点的含义是
(5)大量的b中混有少量的a,提纯b的方法为
(6)t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是 。
| A.都是饱和溶液 |
| B.溶质质量分数大小关系是:b>a>c |
| C.析出晶体质量最多的是a |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】甲、乙、丙三种物质的溶解度曲线如图所示(不含结晶水),请回答:
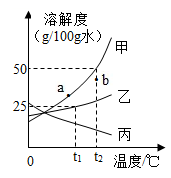
(1)0℃时,甲、乙、丙的溶解度最大的是_______ 。
(2)t2℃时,将30g甲固体加入到50g水中,充分搅拌后的所得溶液是_______ (填“饱和”“不饱和”)。
(3)若甲中含有少量乙,应用__________ 法提纯甲。
(4)等质量的甲、乙、丙三种饱和溶液从t2℃降温至0℃后,溶液的质量分数由大到小的顺序是______________ 。
(5)若使甲溶液的状态从a点转化为b点,可采取的措施是__________

(1)0℃时,甲、乙、丙的溶解度最大的是
(2)t2℃时,将30g甲固体加入到50g水中,充分搅拌后的所得溶液是
(3)若甲中含有少量乙,应用
(4)等质量的甲、乙、丙三种饱和溶液从t2℃降温至0℃后,溶液的质量分数由大到小的顺序是
(5)若使甲溶液的状态从a点转化为b点,可采取的措施是
您最近一年使用:0次
【推荐3】如图是A、B、C三种固体物质的溶解度曲线。

(1)P点表示的含义是___________ 。
(2)B中混有少量的A,提纯B的方法是___________ 。
(3)t1℃时把50gA物质与100g水混合,充分溶解形成___________ (填“饱和”或“不饱和”)溶液。
(4)将等质量的A、B、C三种固体物质分别配成t3℃时的饱和溶液,所得溶液的质量最多的是___________ 。
(5)将t1℃时A、B、C三种物质的饱和溶液升温到t3℃时,所得溶液的溶质质量分数由大到小的关系是___________ 。

(1)P点表示的含义是
(2)B中混有少量的A,提纯B的方法是
(3)t1℃时把50gA物质与100g水混合,充分溶解形成
(4)将等质量的A、B、C三种固体物质分别配成t3℃时的饱和溶液,所得溶液的质量最多的是
(5)将t1℃时A、B、C三种物质的饱和溶液升温到t3℃时,所得溶液的溶质质量分数由大到小的关系是
您最近一年使用:0次
【推荐1】t℃时分别将甲、乙两种固体的水溶液恒温蒸发,溶液的质量随蒸发水的质量变化关系如图所示。(甲、乙均不和水反应)

(1)蒸发溶剂前,____ (填“甲”或“乙”)是饱和溶液。
(2)t℃时乙的溶解度是____ g。
(3)b点对应溶液的溶质质量分数为________ 。
(4)依据上述实验,你认为乙的溶解度随温度变化的趋势是 (填字母)的。

(1)蒸发溶剂前,
(2)t℃时乙的溶解度是
(3)b点对应溶液的溶质质量分数为
(4)依据上述实验,你认为乙的溶解度随温度变化的趋势是 (填字母)的。
| A.随温度升高而增大 |
| B.随温度升高而减小 |
| C.无法判断 |
您最近一年使用:0次
【推荐2】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶度曲线的是_____ (填“A”或“B”);

(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙 ②升高温度 ③降低温度 ④加入水 ⑤蒸发水后再恢复到原温度 ⑥加入生石灰。
其中措施正确的是____
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体的质量为____
(4)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO后得到溶液乙,此时溶液中溶质的质量
乙_______ 甲(填“>”、“<”或“=”);
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH固体,应采取的物理方法是_______
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH____ (填“偏大”、“偏小”或“不受影响”)。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |

(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙 ②升高温度 ③降低温度 ④加入水 ⑤蒸发水后再恢复到原温度 ⑥加入生石灰。
其中措施正确的是
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体的质量为
(4)现有20℃时Ca(OH)2的饱和溶液甲,向其中加入一定量CaO后得到溶液乙,此时溶液中溶质的质量
乙
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH固体,应采取的物理方法是
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH
您最近一年使用:0次
【推荐3】甲、乙两种固体的溶解度曲线如图一所示,t2℃时,100克水中加入60克硝酸钾,充分搅拌,直到固体完全消失,然后按图二进行实验,分别采用不同方法(每种方法只改变一个量),得到三个恰好饱和的溶液,且溶液质量依次减小。

(1)t2°C时,溶解度大小关系为:甲______ 乙(填“>”或“<”或“=”)。
(2)由图二推测硝酸钾是图一中的__________ 物质(填“甲”或“乙”)。
(3)图二中“某一步操作”得到E杯中溶液的操作是__________ 。
(4)图二中得到的C、D、E杯溶液中溶质质量分数的大小关系是_______ (用“C、D、E和>或<或=”表示)。
(5)图二中“某一步操作”得到D杯溶液前后的溶液状态变化过程可以在图一中表示为________ (填字母序号)。
a.b点→a点 b.c点→a点 c.b点→c点 d.c点→d点

(1)t2°C时,溶解度大小关系为:甲
(2)由图二推测硝酸钾是图一中的
(3)图二中“某一步操作”得到E杯中溶液的操作是
(4)图二中得到的C、D、E杯溶液中溶质质量分数的大小关系是
(5)图二中“某一步操作”得到D杯溶液前后的溶液状态变化过程可以在图一中表示为
a.b点→a点 b.c点→a点 c.b点→c点 d.c点→d点
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐1】如图为a、b、c三种不含结晶水的固体物质在水中的溶解度曲线,请回答下列问题:_____ 。
(2)当b中混有少量a时,提纯b的方法是_____ 。
(3)t4℃时,将等质量的a、b、c三种饱和溶液降温到t3℃时,所得溶液中,溶剂质量由大到小的顺序为_____ 。
(4)t4℃时,在三个装有50g水的烧杯中分别加入a、b、c三种物质各20g,能形成不饱和溶液的是_____ ,再降温到t2℃时,所得三种溶液的溶质质量分数大小关系为_____ 。
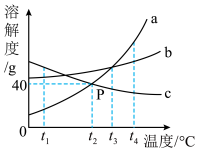
(2)当b中混有少量a时,提纯b的方法是
(3)t4℃时,将等质量的a、b、c三种饱和溶液降温到t3℃时,所得溶液中,溶剂质量由大到小的顺序为
(4)t4℃时,在三个装有50g水的烧杯中分别加入a、b、c三种物质各20g,能形成不饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答溶液的相关问题。
【研究一】:小刚做静脉点滴时发现,医用葡萄糖溶液的溶质质量分数为5%,他应用化学课学到的知识,配置了一份200g溶质质量分数为5%的葡萄糖溶液,步骤如下:
(1)计算:实验中需要称量葡萄糖的质量为___________ g。
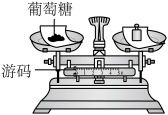
(2)称量:实验中选用与需要称量葡萄糖质量相等的砝码,游码未归零,位置如图所示。若其他操作正确,则配置溶液中葡萄糖的质量分数___________ 5%(选填“>”“=”或“<”)。
(3)量取:量取所需体积的水,应选择___________ mL(选填“100”“250”或“500”)量筒。
(4)溶解:需要用到玻璃棒和烧杯,玻璃棒的作用是___________ 。
(5)装瓶:把配好的溶液倒入细口瓶中,贴上标签。
【研究二】:小刚从家中冰箱中取出一杯含有葡萄糖晶体的溶液,常温放置一段时间,现象如图11所示(假设水不蒸发)。
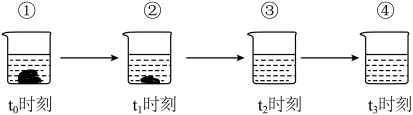
(1)由如图的现象,推测葡萄糖的溶解度受温度影响的变化规律___________ 。
(2)上述四个烧杯,一定为饱和溶液的是___________ (选填“①”、“②”,“③”或“④”,下同)。溶液质量最小的是___________ 。
【研究一】:小刚做静脉点滴时发现,医用葡萄糖溶液的溶质质量分数为5%,他应用化学课学到的知识,配置了一份200g溶质质量分数为5%的葡萄糖溶液,步骤如下:

(1)计算:实验中需要称量葡萄糖的质量为
(2)称量:实验中选用与需要称量葡萄糖质量相等的砝码,游码未归零,位置如图所示。若其他操作正确,则配置溶液中葡萄糖的质量分数
(3)量取:量取所需体积的水,应选择
(4)溶解:需要用到玻璃棒和烧杯,玻璃棒的作用是
(5)装瓶:把配好的溶液倒入细口瓶中,贴上标签。
【研究二】:小刚从家中冰箱中取出一杯含有葡萄糖晶体的溶液,常温放置一段时间,现象如图11所示(假设水不蒸发)。

(1)由如图的现象,推测葡萄糖的溶解度受温度影响的变化规律
(2)上述四个烧杯,一定为饱和溶液的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
(1)依据表中数据,溶解度曲线随温度的升高而降低的是________ 。
(2)20 ℃时,NaOH的溶解度为________ 。
(3)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体的措施有:①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。其中正确的是________ 。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(4)现将20 ℃时Ca(OH)2的饱和溶液甲溶液降温至0 ℃得到乙溶液,则两种溶液中溶质的质量分数相比,乙________ (填“>”“<”或“=”)甲。
(5)现有60 ℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是________________ 。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解 度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)20 ℃时,NaOH的溶解度为
(3)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体的措施有:①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。其中正确的是
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(4)现将20 ℃时Ca(OH)2的饱和溶液甲溶液降温至0 ℃得到乙溶液,则两种溶液中溶质的质量分数相比,乙
(5)现有60 ℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是
您最近一年使用:0次




