阅读下列短文,回答问题。
积极探索新型清洁能源有助于促进我国加快产业结构的优化。氢能是一种热值高、能量大、来源多样的绿色能源。现阶段使用天然气等化石能源重整制氢,以及电解水制氢。
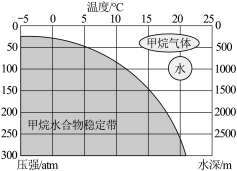
可燃冰外观类似冰,主要含甲烷水合物(由甲烷分子和水分子组成),还含有少量二氧化碳等气体。温度不高、压力足够大、有甲烷气源时,甲烷可与水生成甲烷水合物,分散在海底岩层的空隙中、甲烷水合物能稳定存在的压强和温度范围如图所示。甲烷还是重要的化工原料,可制造氢气、炭黑、已炔、氰化氢等。______ (填“纯净物”或“混合物”)。
(2)可燃冰中主要成分甲烷具有可燃性,写出其完全燃烧的化学反应方程式:______ 。
(3)下列有关说法正确的是______。
(4)请写出甲烷水合物能稳定存在的压强和温度规律______ 。
积极探索新型清洁能源有助于促进我国加快产业结构的优化。氢能是一种热值高、能量大、来源多样的绿色能源。现阶段使用天然气等化石能源重整制氢,以及电解水制氢。
可燃冰外观类似冰,主要含甲烷水合物(由甲烷分子和水分子组成),还含有少量二氧化碳等气体。温度不高、压力足够大、有甲烷气源时,甲烷可与水生成甲烷水合物,分散在海底岩层的空隙中、甲烷水合物能稳定存在的压强和温度范围如图所示。甲烷还是重要的化工原料,可制造氢气、炭黑、已炔、氰化氢等。
(2)可燃冰中主要成分甲烷具有可燃性,写出其完全燃烧的化学反应方程式:
(3)下列有关说法正确的是______。
| A.海底温度低,压强大,有利于甲烷的溶解 |
| B.在 300atm 下,任何温度下都可以形成可燃冰 |
| C.可燃冰开采不合理,会造成温室效应或者海底塌方等 |
| D.可燃冰作为燃料优点是燃烧热值大,对环境不会造成污染 |
(4)请写出甲烷水合物能稳定存在的压强和温度规律
2024·安徽马鞍山·一模 查看更多[2]
更新时间:2024-05-01 00:53:06
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】“5G”改变生活,中国芯彰显中国“智”造。芯片的基材主要是高纯硅,如图是一种制备高纯硅的工艺流程图:
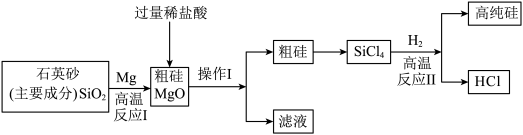
(1)反应I的基本类型是_______ 。
(2)操作I中用到的的玻璃仪器除了烧杯、漏斗还需要_______ ,其作用是_______ 。
(3)反应Ⅱ的化学方程式为_______ 。
(4)上述已知生产流程中,可以循环利用的物质是_______ 。

(1)反应I的基本类型是
(2)操作I中用到的的玻璃仪器除了烧杯、漏斗还需要
(3)反应Ⅱ的化学方程式为
(4)上述已知生产流程中,可以循环利用的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】水是人类宝贵的自然资源之一。
(1)生活中常讲“烧开水”是指利用_____ 的方法来获得饮用水,即可以杀菌又可以降低水的_____ 。
(2)用下列方法得到的水,纯度最高的是_____ 。
A 吸附 B 蒸馏 C 过滤 D 沉淀
(3)为了确定水的组成,某小组进行了电解水的实验。则正极和负极产生的气体的体积比是_____ ,电解水的化学方程式为_____ 。
(1)生活中常讲“烧开水”是指利用
(2)用下列方法得到的水,纯度最高的是
A 吸附 B 蒸馏 C 过滤 D 沉淀
(3)为了确定水的组成,某小组进行了电解水的实验。则正极和负极产生的气体的体积比是
您最近一年使用:0次
【推荐1】水是宝贵的自然资源,是人类生命之源。
(1)下列各种水中,属于纯净物的是 (填字母)。
(2)蒸馏水、矿泉水、白醋、酒精都是常见的无色液体,其中白醋具有酸味,酒精具有特殊气味,常被称为绿色能源。另外两种无色液体可用多种方法区分,例如:加入____________ ,根据产生泡沫的多少来区分。
(3)小刚为了净化收集到的雨水,自制了简易净水器,其中小卵石、石英沙和膨松棉的作用是____________ 。
(1)下列各种水中,属于纯净物的是 (填字母)。
| A.汽水 | B.矿泉水 | C.蒸馏水 | D.经过净化处理的自来水 |
(3)小刚为了净化收集到的雨水,自制了简易净水器,其中小卵石、石英沙和膨松棉的作用是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】分类、类比和总结是初中常用的学习方法。
(1)下列化学反应过程中放出热量的是 。
(2)根据______ ,可以把物质分为纯净物和混合物。下列物质中,属于纯净物的是______ (填字母)。
A.雨水 B.氮气 C.氢氧化钠 D.冰水共存物
(3)已知S和Se具有相似的化学性质,请类比H2SO4写出硒酸(H2SeO4)和氢氧化钠溶液发生中和反应的化学方程式______ 。
(1)下列化学反应过程中放出热量的是 。
| A.镁与盐酸反应 | B.氧化钙与水反应 |
| C.氢氧化钠溶液与稀硫酸反应 | D.碳与二氧化碳反应 |
A.雨水 B.氮气 C.氢氧化钠 D.冰水共存物
(3)已知S和Se具有相似的化学性质,请类比H2SO4写出硒酸(H2SeO4)和氢氧化钠溶液发生中和反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】空气中氧气约占21%,利用分离液态空气的方法得到氧气是工业上制取氧气的重要途径,下面是工业上制氧气的流程图:
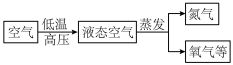
(1)工业上分离液态空气制氧气的变化属于______ (填“物理变化”或“化学变化”)。
(2)氮气的沸点为-196℃,氧气的沸点为-183℃,在蒸发的过程中先被蒸发出来是______ (填化学符号)。
(3)这样制得的氧气是______ (填“纯净物”或“混合物”)。
(4)任何物质我们都要辩证地看待,氧气既有有利的一面,也有有害的一面,请各写出一点。
有利的一面:______ ,有害的一面:______ 。

(1)工业上分离液态空气制氧气的变化属于
(2)氮气的沸点为-196℃,氧气的沸点为-183℃,在蒸发的过程中先被蒸发出来是
(3)这样制得的氧气是
(4)任何物质我们都要辩证地看待,氧气既有有利的一面,也有有害的一面,请各写出一点。
有利的一面:
您最近一年使用:0次
【推荐1】溶液在生产和科研中具有广泛的用途,与人们的生活密不可分。
(1)衣服上沾有的油污,可用汽油洗去,是因为汽油能______ (填“溶解”或“乳化”)油污。
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与______ 有关。
(3)甲、乙、丙三种物质的溶解度曲线如图所示,根据图中信息回答下列问题:

①50℃时,乙物质的溶解度是______ g。
②20℃时,甲、乙、丙三种物质溶解度由大到小的顺序______ 。
③温度为______ ℃时,甲、乙两物质溶解度相同。
④50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数由小到大的顺序为______ 。
(1)衣服上沾有的油污,可用汽油洗去,是因为汽油能
(2)喝了冰镇汽水以后,常常会打嗝。这种现象说明气体的溶解度与
(3)甲、乙、丙三种物质的溶解度曲线如图所示,根据图中信息回答下列问题:

①50℃时,乙物质的溶解度是
②20℃时,甲、乙、丙三种物质溶解度由大到小的顺序
③温度为
④50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数由小到大的顺序为
您最近一年使用:0次
【推荐2】阅读下列科普短文,回答相关问题。
二氧化碳,一种碳氧化合物,常温常压下是一种无色无味的气体,也是一种常见的温室气体,还是空气的组分之一(占大气总体积的0.03%-0.04%)。在物理性质方面,二氧化碳的熔点为-56.6℃,沸点为-78.5℃,密度比空气密度大(标准条件下),溶于水。在化学性质方面,二氧化碳的化学性质不活泼,热稳定性很高(2000℃时仅有1.8%分解),不能燃烧,通常也不支持燃烧,能与水反应生成的是碳酸。
二氧化碳一般可由高温煅烧石灰石或由石灰石和稀盐酸反应制得,主要应用于冷藏易腐败的食品(固态)、作制冷剂(液态)、制造碳化软饮料(气态)和作均相反应的溶剂(超临界状态)等。高温煅烧生成的氧化钙疏松多孔,可用于吸收捕捉二氧化碳。
(1)实验室制备并收集二氧化碳。
①选用药品。按左下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如下图所示:
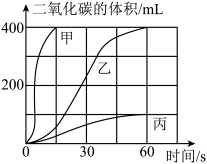
图中丙对应实验_____ (选填“I”“Ⅱ”或“Ⅲ”)。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是_____ ;不用甲对应的药品,理由是_____ 。
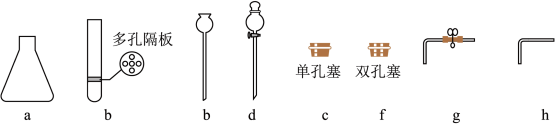
②搭建装置。组装简易启普发生器,应选用_____ (选填编号)。
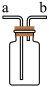
③收集二氧化碳。用图装置收集时,空气从_____ (选填“a”或“b”)端排出。
(2)CO2的捕集与资源化利用是化学研究的热点。
①控制CO2的排放,是为了减缓_____ 效应,加压水洗法可捕集CO2,是因为压强增大时CO2在水中的溶解度_____ (填“增大”“不变”或“减小”)。
②CaO可在较高温度下捕集CO2,在更高温度下将捕集的CO2释放利用。CaC2O4·H2O受热分解可制备CaO,CaC2O4·H2O加热升温过程中固体的质量变化见图。
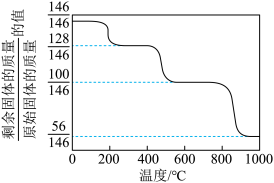
Ⅰ、400~600℃范围内分解反应是:CaC2O4 CaCO3+CO↑,请写出800℃以后发生的反应化学方程式:
CaCO3+CO↑,请写出800℃以后发生的反应化学方程式:_____ 。
Ⅱ、与CaCO3热分解制备的CaO相比,CaC2O4·H2O热分解制备的CaO具有更好的CO2捕集性能,其原因是_____ 。
(3)对CO2气体加压,降温,可获得干冰,从构成物质的微粒视角分析,该过程主要改变的是_____ 。
(4)绿色植物是地球的肺,多植树造林,增加绿地面积,可以有效吸收二氧化碳,减缓温室效应,请写出相应的化学方程式_____ 。
二氧化碳,一种碳氧化合物,常温常压下是一种无色无味的气体,也是一种常见的温室气体,还是空气的组分之一(占大气总体积的0.03%-0.04%)。在物理性质方面,二氧化碳的熔点为-56.6℃,沸点为-78.5℃,密度比空气密度大(标准条件下),溶于水。在化学性质方面,二氧化碳的化学性质不活泼,热稳定性很高(2000℃时仅有1.8%分解),不能燃烧,通常也不支持燃烧,能与水反应生成的是碳酸。
二氧化碳一般可由高温煅烧石灰石或由石灰石和稀盐酸反应制得,主要应用于冷藏易腐败的食品(固态)、作制冷剂(液态)、制造碳化软饮料(气态)和作均相反应的溶剂(超临界状态)等。高温煅烧生成的氧化钙疏松多孔,可用于吸收捕捉二氧化碳。
(1)实验室制备并收集二氧化碳。
①选用药品。按左下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如下图所示:
| 实验编号 | 药品 |
| Ⅰ | 块状大理石、10%H2SO4溶液 |
| Ⅱ | 块状大理石、7%HCl溶液 |
| Ⅲ | 大理石粉末、7%HCl溶液 |

图中丙对应实验
②搭建装置。组装简易启普发生器,应选用

③收集二氧化碳。用图装置收集时,空气从

(2)CO2的捕集与资源化利用是化学研究的热点。
①控制CO2的排放,是为了减缓
②CaO可在较高温度下捕集CO2,在更高温度下将捕集的CO2释放利用。CaC2O4·H2O受热分解可制备CaO,CaC2O4·H2O加热升温过程中固体的质量变化见图。

Ⅰ、400~600℃范围内分解反应是:CaC2O4
 CaCO3+CO↑,请写出800℃以后发生的反应化学方程式:
CaCO3+CO↑,请写出800℃以后发生的反应化学方程式:Ⅱ、与CaCO3热分解制备的CaO相比,CaC2O4·H2O热分解制备的CaO具有更好的CO2捕集性能,其原因是
(3)对CO2气体加压,降温,可获得干冰,从构成物质的微粒视角分析,该过程主要改变的是
(4)绿色植物是地球的肺,多植树造林,增加绿地面积,可以有效吸收二氧化碳,减缓温室效应,请写出相应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】2018年我市大部分居民用上了燃气公司提供的天然气,代替原来使用的煤或液化石油气,对我市的环境起了一定的改善作用。回答下列问题:
(1)天然气的主要成分是甲烷(CH4),写出甲烷燃烧的化学方程式为_________ 。
(2)某小区原来使用的管道燃气是液化石油气(主要成分C3H8),煤气公司给小区的炉灶进行了改装,如果改装进空气口,应将进口直径_______ (变大或变小)。
(3)列举一条天然气取代煤作为燃料的优点________ 。
(1)天然气的主要成分是甲烷(CH4),写出甲烷燃烧的化学方程式为
(2)某小区原来使用的管道燃气是液化石油气(主要成分C3H8),煤气公司给小区的炉灶进行了改装,如果改装进空气口,应将进口直径
(3)列举一条天然气取代煤作为燃料的优点
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
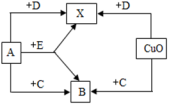
【推荐2】教材中常见四种物质之间的转化关系(部分物质和反应条件已经略去)如图所示。甲是天然气最主要的成分,乙、丙组成元素完全相同。
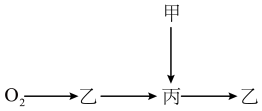
(1)写出甲→丙的化学方程式________ 。
(2)简述丙在生活中的一种用途________ 。
(3)请你设计一种鉴别乙和丙的方法。(用化学方程式表示)________

(1)写出甲→丙的化学方程式
(2)简述丙在生活中的一种用途
(3)请你设计一种鉴别乙和丙的方法。(用化学方程式表示)
您最近一年使用:0次

 三种固体物质的溶解度曲线,请回答下列问题:
三种固体物质的溶解度曲线,请回答下列问题: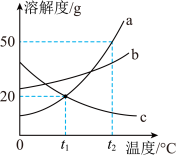
 的饱和溶液同时析出晶体,方法是
的饱和溶液同时析出晶体,方法是 或“
或“ ”)相似。
”)相似。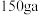 的饱和溶液稀释成质量分数为
的饱和溶液稀释成质量分数为 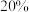 的溶液需加水
的溶液需加水 。
。