从海水中获取的食盐是一种里要的工业原料。
(1)组成。
构成NaCl晶体的微粒为_________ (填离子符号)。
(2)提取。
①1000g海水含有27.2 gNaCl,则海水中NaCl的质量分数为__________ 。海水晒盐的基本原理是_________ 。
②海水晒制的粗盐中含有MgCl2、CaCl2和Na2SO4等少量可溶性杂质和泥沙。为除去可溶性杂质,将粗盐样品溶于水,可依次加入过量_________ (填一种试剂)和Na2CO3溶液,充分反应后过滤,向滤液中加入过量的稀盐酸,搅拌,煮沸得NaCl溶液。加入稀盐酸的目的是_________ 。
(3)应用。
①通过电解饱和NaCl溶液制备NaOH,反应的化学方程式: ,则X的化学式为
,则X的化学式为_________ 。
②电解熔融NaCl可得到金属Na和另一种单质,该反应的化学方程式为________ 。
(4)拓展。
I.“侯氏制碱法”生产纯碱的过程中,碳酸氢钠的生成是至关重要的一环,其原理是:
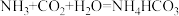 ,
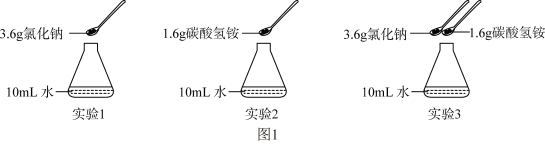
, 。兴趣小组在常温(20℃)下设计并完成了如图1所示实验。
。兴趣小组在常温(20℃)下设计并完成了如图1所示实验。
【已知20℃时NaCl、NH4HCO3、NaHCO3、NH4Cl的溶解度为36.0g、21.0g、9.6g、37.2g。】________ 。(填序号)
②实验3的锥形瓶中出现白色浑浊,经检验为NaHCO3,写出用稀盐酸检验NaHCO3的化学方程式:_______ 。
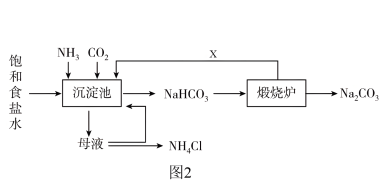
Ⅱ.侯氏制碱法的生产流程如图2所示:_________ 。
②请结合如图的信息,写出NaHCO3晶体能析出的原因_________ 。
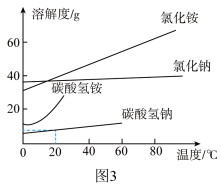
③图3是四种物质的溶解度曲线。母液中含有较高浓度的NH4Cl和少量NaCl,利用降温结晶的方法可提纯NH4Cl,理由是_________ 。
④上述流程中可循环利用的物质有:NaCl和_________ 。
Ⅲ.测定纯碱样品中碳酸钠的质量分数。
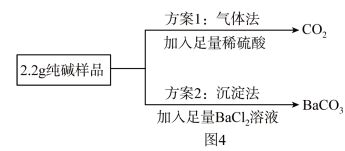
纯碱产品中常混有少量氯化钠,兴趣小组设计图4所示两种方案测定某纯碱样品中碳酸钠的质量分数:根据方案1,实验测得CO2的质量为0.88g。根据方案2,实验测得BaCO3的质量为3.94g请任选其中一种方案与相关数据,计算该纯碱样品中碳酸钠的质量分数_______ (写出计算过程,结果精确到0.1%)。
(1)组成。
构成NaCl晶体的微粒为
(2)提取。
①1000g海水含有27.2 gNaCl,则海水中NaCl的质量分数为
②海水晒制的粗盐中含有MgCl2、CaCl2和Na2SO4等少量可溶性杂质和泥沙。为除去可溶性杂质,将粗盐样品溶于水,可依次加入过量
(3)应用。
①通过电解饱和NaCl溶液制备NaOH,反应的化学方程式:
 ,则X的化学式为
,则X的化学式为②电解熔融NaCl可得到金属Na和另一种单质,该反应的化学方程式为
(4)拓展。
I.“侯氏制碱法”生产纯碱的过程中,碳酸氢钠的生成是至关重要的一环,其原理是:
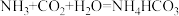 ,
, 。兴趣小组在常温(20℃)下设计并完成了如图1所示实验。
。兴趣小组在常温(20℃)下设计并完成了如图1所示实验。【已知20℃时NaCl、NH4HCO3、NaHCO3、NH4Cl的溶解度为36.0g、21.0g、9.6g、37.2g。】
②实验3的锥形瓶中出现白色浑浊,经检验为NaHCO3,写出用稀盐酸检验NaHCO3的化学方程式:
Ⅱ.侯氏制碱法的生产流程如图2所示:
②请结合如图的信息,写出NaHCO3晶体能析出的原因
③图3是四种物质的溶解度曲线。母液中含有较高浓度的NH4Cl和少量NaCl,利用降温结晶的方法可提纯NH4Cl,理由是
④上述流程中可循环利用的物质有:NaCl和
Ⅲ.测定纯碱样品中碳酸钠的质量分数。
纯碱产品中常混有少量氯化钠,兴趣小组设计图4所示两种方案测定某纯碱样品中碳酸钠的质量分数:根据方案1,实验测得CO2的质量为0.88g。根据方案2,实验测得BaCO3的质量为3.94g请任选其中一种方案与相关数据,计算该纯碱样品中碳酸钠的质量分数
2024·江苏苏州·模拟预测 查看更多[2]
更新时间:2024-04-28 14:50:40
|
相似题推荐
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐1】请利用化学知识分析,回答下列问题。
(1)测量体温时,水银温度计的汞柱会升高。请从微观角度解释汞柱升高的原因:温度升高,___________ 。
(2)“84”消毒液的消毒原理是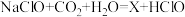 ,生成的HClO具有杀菌作用。化学方程式中X的化学式为
,生成的HClO具有杀菌作用。化学方程式中X的化学式为___________ ,HClO中氯元素的化合价为___________ 。
(3)科学家最新研制出5个氮原子构成的带一个单位正电荷的原子团___________ (填符号)。
(4)从微观上看,化学反应是微观粒子按一定的数目关系进行的。已知2gH2、36.5gHCl中所含分子数均为α。一定条件下,某反应中所有物质的分子数随反应过程的变化如图所示(H2和物质X的变化曲线重合),下列说法正确的是___________。

(1)测量体温时,水银温度计的汞柱会升高。请从微观角度解释汞柱升高的原因:温度升高,
(2)“84”消毒液的消毒原理是
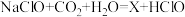 ,生成的HClO具有杀菌作用。化学方程式中X的化学式为
,生成的HClO具有杀菌作用。化学方程式中X的化学式为(3)科学家最新研制出5个氮原子构成的带一个单位正电荷的原子团
(4)从微观上看,化学反应是微观粒子按一定的数目关系进行的。已知2gH2、36.5gHCl中所含分子数均为α。一定条件下,某反应中所有物质的分子数随反应过程的变化如图所示(H2和物质X的变化曲线重合),下列说法正确的是___________。

| A.物质X的化学式是Cl | B.一个Cl原子的质量为 |
| C.t时刻,H2和HCl的质量相等 | D.反应开始时,物质X的质量为34.5g |
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】2018年5月13日,我国首艘001A型国产航母开始海试,标志着我国在航海及军事领域取得重大突破。
(1)建造航母用到了钛合金,构成金属钛的粒子是___ (填“原子”“分子”或“离子”),工业制钛有一种反应为: ,X的化学式为
,X的化学式为___ 。
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与___ 接触而锈蚀。
(3)请你用化学方程式表示出探究航母材料中铝、铜两种金属活动性强弱的方法___ 。
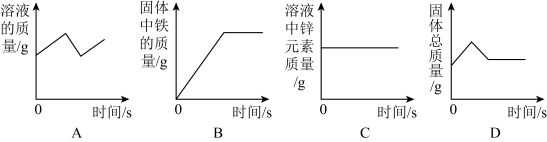
(4)康康为了探究航母中金属锌的化学性质,将一定量的锌粉加入到硝酸亚铁、硝酸银的混合溶液中,溶液最终变为无色。下列图像能表示对应变化关系的是___ (填字母序号)。
(5)如图是工业炼铁示意图。

①炼铁的固体原料需经过粉碎,其目的是什么?_____ 。
②冶炼过程中焦炭的作用是什么?______ 。
③若要炼制含铁96%的生铁70t,则理论上需要含杂质20%的赤铁矿的质量是多少?_____ 。
(1)建造航母用到了钛合金,构成金属钛的粒子是
 ,X的化学式为
,X的化学式为(2)航母外壳用涂料覆盖,是为了防止钢铁材料与
(3)请你用化学方程式表示出探究航母材料中铝、铜两种金属活动性强弱的方法
(4)康康为了探究航母中金属锌的化学性质,将一定量的锌粉加入到硝酸亚铁、硝酸银的混合溶液中,溶液最终变为无色。下列图像能表示对应变化关系的是

(5)如图是工业炼铁示意图。

①炼铁的固体原料需经过粉碎,其目的是什么?
②冶炼过程中焦炭的作用是什么?
③若要炼制含铁96%的生铁70t,则理论上需要含杂质20%的赤铁矿的质量是多少?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】金属材料在生产生活中有广泛的用途。回答下列问题。
(1)我国古代典籍中有“银针验毒”记载,其反应原理之一是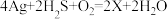 ,则X的化学式为
,则X的化学式为______ 。
(2)铁和铝都可以用来制作炊具,这是利用了铁和铝的______ 性。对因生锈而废弃的铁制品,你认为比较妥当的处理方法是______ (写出一条)。
(3)我国西汉时期,在《淮南万毕术》一书中写到“曾青得铁则化为铜”,请用化学方程式表示该原理:______ 。
(4)“暖宝宝”是人们冬天用于局部取暖的简易工具,某兴趣小组同学对“暖宝宝”发热原理进行了探究。
下表是六组实验分别选用的物品,蛭石是保温性能极好的材料,吸水树脂能不断从空气中吸收水分。(每组实验所用同种药品质量相等,忽略其它因素的影响。)
同学们按照如图1装置进行实验。密闭的集气瓶中有干燥的空气,用温度传感器测定集气瓶中温度的变化,得到图2所示时间——温度曲线。

根据实验,回答下列问题。
①对比分析六组实验,你认为最适合做“暖宝宝”袋内物质的是______ (填实验编号)。
②“暖宝宝”放热是由于铁在______ 的作用下发生了缓慢氧化。
③分析上面图表,能说明氯化钠加快反应速度的两组实验是______ 。
(1)我国古代典籍中有“银针验毒”记载,其反应原理之一是
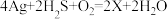 ,则X的化学式为
,则X的化学式为(2)铁和铝都可以用来制作炊具,这是利用了铁和铝的
(3)我国西汉时期,在《淮南万毕术》一书中写到“曾青得铁则化为铜”,请用化学方程式表示该原理:
(4)“暖宝宝”是人们冬天用于局部取暖的简易工具,某兴趣小组同学对“暖宝宝”发热原理进行了探究。
下表是六组实验分别选用的物品,蛭石是保温性能极好的材料,吸水树脂能不断从空气中吸收水分。(每组实验所用同种药品质量相等,忽略其它因素的影响。)
编号 | 选用的物品 |
实验一 | 铁粉 |
实验二 | 铁粉、水 |
实验三 | 铁粉、氯化钠 |
实验四 | 铁粉、氯化钠、水 |
实验五 | 铁粉、氯化钠,水,活性炭 |
实验六 | 铁粉、水、活性炭、吸水树脂、食盐、蛭石等 |

根据实验,回答下列问题。
①对比分析六组实验,你认为最适合做“暖宝宝”袋内物质的是
②“暖宝宝”放热是由于铁在
③分析上面图表,能说明氯化钠加快反应速度的两组实验是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】火力发电厂(燃烧煤发电)会排放较多的二氧化硫,造成严重的环境问题是_____ ,该厂技术人员设计三种除硫环保方案:(已知亚硫酸钙不溶于水)
①用烧碱溶液吸收SO2,反应方程式是_____ 。
②用石灰浆(氢氧化钙的悬浊液)反应方程式是_____ 。
③用石灰石浆吸收,反应方程式是2CaCO3+2SO2+O2=2CaSO4+2CO2,
(1)从降低成本的角度考虑,你认为最佳方案是_____ (填方案序号)
(2)若该发电厂排放的1000kg废气中含1.8kg的二氧化硫气体,计算除去4000kg废气中的二氧化硫至少需要含碳酸钙80%的石灰石多少kg?_____
①用烧碱溶液吸收SO2,反应方程式是
②用石灰浆(氢氧化钙的悬浊液)反应方程式是
③用石灰石浆吸收,反应方程式是2CaCO3+2SO2+O2=2CaSO4+2CO2,
(1)从降低成本的角度考虑,你认为最佳方案是
(2)若该发电厂排放的1000kg废气中含1.8kg的二氧化硫气体,计算除去4000kg废气中的二氧化硫至少需要含碳酸钙80%的石灰石多少kg?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。还可以用于牙膏,对牙齿有漂白和防过敏的作用。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为____ )是一种白色的粉末,其外观与物理性质与氧化镁相似。化学性质不够稳定,不溶于水,但逐渐的被分解放出氧气。
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式________ 。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量__________ (填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁【Mg2(OH)2CO3】和30%的过氧化氢溶液来制取过氧化镁。
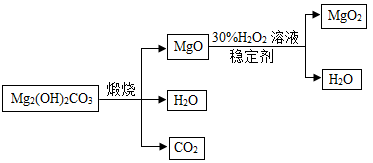
【资料】①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是_________ (写出具体的操作和现象);上述生产过程加入稳定的剂的作用是 ________ 。
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在________ ℃,煅烧的时间适宜控制在 ______ h。
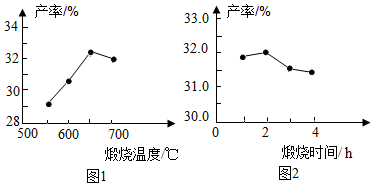
(5)结果分析:在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因____ 。
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。
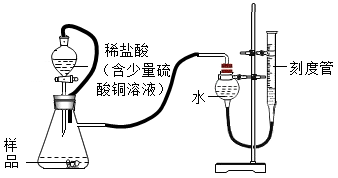
①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是__________ 。
(7)根据上面实验数据计算样品中过氧化镁的质量分数__________ (写出具体的计算过程,实验条件下O2密度为1.429g/L)。
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是( )
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量
二.过氧化镁的制备
下图是利用碱式碳酸镁【Mg2(OH)2CO3】和30%的过氧化氢溶液来制取过氧化镁。

【资料】①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在

(5)结果分析:在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。

①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是
(7)根据上面实验数据计算样品中过氧化镁的质量分数
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】为测定MgCl2和稀盐酸的混合溶液的组成情况,某研究小组进行如下实验。

请回答下列问题:
(1)写出实验中有沉淀生成的反应的化学方程式______ 。
(2)根据已知条件列出求解参加反应氯化镁质量(x)的比例式______ 。
(3)在滴加氢氧化钠溶液的整个过程中烧杯内各溶质的质量变化情况为______ 。
(4)原混合溶液中 MgCl2和HCl质量的最简整数比为______ 。
(5)请计算所加氢氧化钠溶液溶质的质量分数______ 。

请回答下列问题:
(1)写出实验中有沉淀生成的反应的化学方程式
(2)根据已知条件列出求解参加反应氯化镁质量(x)的比例式
(3)在滴加氢氧化钠溶液的整个过程中烧杯内各溶质的质量变化情况为
(4)原混合溶液中 MgCl2和HCl质量的最简整数比为
(5)请计算所加氢氧化钠溶液溶质的质量分数
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】某过碳酸钠样品中含有少量的碳酸钠等杂质,为测定其纯度,某化学小组同学利用如图装置展开如下探究:

[资料在线]
①过碳酸钠(Na2CO4)和稀硫酸反应的原理为:
2 Na2CO4+2H2SO4=2Na2SO4+2CO2↑+O2↑+2H2O
②碳酸钠与稀硫酸反应后生成硫酸钠、二氧化碳和水。
③浓硫酸具有强吸水性。氢氧化钠溶液能吸收二氧化碳。
④含钠的化合物可溶于水,样品中其它杂质不溶于水且不参与反应。
⑤该实验条件下,氧气的密度为l.43g/L、二氧化碳的密度l.97g/L。
[实验步骤]
a.连接仪器并检查装置气密性。
b.向装置Ⅰ中的锥形瓶加入1.0g样品,由注射器缓缓注入稀硫酸,待到完全反应后,利用装置Ⅳ测得反应生成的气体体积为82.6 mL;装置I中的溶液经处理,称得硫酸钠固体质量为1.1g。
c.根据测得数据,计算样品中过碳酸钠的质量分数。
[回答问题]
(1)判断样品与稀硫酸完全反应的现象是___________ 。
写出碳酸钠与稀硫酸反应的化学方程式:___________ 。
(2)装置Ⅱ和Ⅲ的广口瓶中盛有足量的药品是___________ (填标号)。
A.Ⅱ—浓硫酸、Ⅲ—氢氧化钠溶液B.Ⅱ—氢氧化钠溶液、Ⅲ—浓硫酸
(3)甲同学通过称量装置I中实验前后固体的质量、乙同学通过读取装置IV中气体的体积,分别计算出样品中过碳酸钠质量分数。
①乙同学计算过程中,需要选用___________ (填“氧气”或“二氧化碳”)的密度。
②两位同学的实验结果不同,经分析乙同学实验方案正确。甲同学的实验方案不准确的原因是___________ 。

[资料在线]
①过碳酸钠(Na2CO4)和稀硫酸反应的原理为:
2 Na2CO4+2H2SO4=2Na2SO4+2CO2↑+O2↑+2H2O
②碳酸钠与稀硫酸反应后生成硫酸钠、二氧化碳和水。
③浓硫酸具有强吸水性。氢氧化钠溶液能吸收二氧化碳。
④含钠的化合物可溶于水,样品中其它杂质不溶于水且不参与反应。
⑤该实验条件下,氧气的密度为l.43g/L、二氧化碳的密度l.97g/L。
[实验步骤]
a.连接仪器并检查装置气密性。
b.向装置Ⅰ中的锥形瓶加入1.0g样品,由注射器缓缓注入稀硫酸,待到完全反应后,利用装置Ⅳ测得反应生成的气体体积为82.6 mL;装置I中的溶液经处理,称得硫酸钠固体质量为1.1g。
c.根据测得数据,计算样品中过碳酸钠的质量分数。
[回答问题]
(1)判断样品与稀硫酸完全反应的现象是
写出碳酸钠与稀硫酸反应的化学方程式:
(2)装置Ⅱ和Ⅲ的广口瓶中盛有足量的药品是
A.Ⅱ—浓硫酸、Ⅲ—氢氧化钠溶液B.Ⅱ—氢氧化钠溶液、Ⅲ—浓硫酸
(3)甲同学通过称量装置I中实验前后固体的质量、乙同学通过读取装置IV中气体的体积,分别计算出样品中过碳酸钠质量分数。
①乙同学计算过程中,需要选用
②两位同学的实验结果不同,经分析乙同学实验方案正确。甲同学的实验方案不准确的原因是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
真题
【推荐2】据统计全球每年消耗大约1500亿个易拉罐,其使用后的处理已成为研究热点。
Ⅰ、辨识材质
(1)易拉罐置于冰箱能迅速降温,这体现了金属的______ 性。
(2)易拉罐以铝或铁作为罐体材料。为区分常见装可乐和椰汁的罐体主材,对其进行如下探究:
①物理方法:分别将磁铁置于两个罐体样品上,可乐罐不能被磁铁吸引,椰汁罐可以被磁铁吸引,则说明可乐罐和椰汁罐的材质分别是______ 。
②化学方法:______ (填写一种操作、现象和结论)。
Ⅱ、铁罐回收
兴趣小组的同学们尝试用回收的铁罐来制备补铁剂硫酸亚铁。除去铁罐表层的涂层后将其剪碎,称取5份5.6g的铁屑,分别向其中加入一定体积14%的硫酸溶液(密度为1.1g•mL﹣1),测得硫酸亚铁的产率如表:
(3)至少加入______ mL(精确到0.1)14%的硫酸溶液能使5.6g铁屑完全反应。
(4)m(Fe):m(H2SO4)=______ 时进行反应最佳(从表中选择一组数据填写)。
Ⅲ、铝罐回收
科研人员将碱液捕集二氧化碳后的产物与铝罐在一定条件下制备高效储氢物质甲酸钠(HCOONa)和牙科材料勃姆石[AlO(OH)],工艺流程如图1:

为探究反应①进行的实验条件,科研人员将相同比例和质量的NaHCO3和Al在不同温度、碱度、反应时长进行对比实验,收集实验数据如图2所示:

(5)从捕集到的二氧化碳到产品甲酸钠,其中碳元素的化合价______ (选填“不变”、“升高”或“降低”)。
(6)由图2可知反应①的最佳实验条件为______ ,此时反应的化学方程式为______ 。
(7)若一定条件下甲酸钠产率为60%,1500亿(1.5×1011)个330mL铝制易拉罐(含铝约20克/个)可以制取约______ 万吨甲酸钠。
Ⅰ、辨识材质
(1)易拉罐置于冰箱能迅速降温,这体现了金属的
(2)易拉罐以铝或铁作为罐体材料。为区分常见装可乐和椰汁的罐体主材,对其进行如下探究:
①物理方法:分别将磁铁置于两个罐体样品上,可乐罐不能被磁铁吸引,椰汁罐可以被磁铁吸引,则说明可乐罐和椰汁罐的材质分别是
②化学方法:
Ⅱ、铁罐回收
兴趣小组的同学们尝试用回收的铁罐来制备补铁剂硫酸亚铁。除去铁罐表层的涂层后将其剪碎,称取5份5.6g的铁屑,分别向其中加入一定体积14%的硫酸溶液(密度为1.1g•mL﹣1),测得硫酸亚铁的产率如表:
| 序号 | m(Fe):m(H2SO4) | 产率/% |
| 1 | 5.6:8.82 | 74.63 |
| 2 | 5.6:9.80 | 76.74 |
| 3 | 5.610.78 | 87.85 |
| 4 | 5.6:11.16 | 95.14 |
| 5 | 5.6:12.74 | 92.36 |
(3)至少加入
(4)m(Fe):m(H2SO4)=
Ⅲ、铝罐回收
科研人员将碱液捕集二氧化碳后的产物与铝罐在一定条件下制备高效储氢物质甲酸钠(HCOONa)和牙科材料勃姆石[AlO(OH)],工艺流程如图1:

为探究反应①进行的实验条件,科研人员将相同比例和质量的NaHCO3和Al在不同温度、碱度、反应时长进行对比实验,收集实验数据如图2所示:

(5)从捕集到的二氧化碳到产品甲酸钠,其中碳元素的化合价
(6)由图2可知反应①的最佳实验条件为
(7)若一定条件下甲酸钠产率为60%,1500亿(1.5×1011)个330mL铝制易拉罐(含铝约20克/个)可以制取约
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】海洋是巨大的资源宝库,人类提取海水中的化学元素,来制备有多种用途的物质。广泛应用于火箭、导弹和飞机制造业;金属镁,就是利用从海水中提取的镁盐制取的。工业上从海水中提取单质镁的过程如图所示:________ 。
(2)海水中本身就含有氯化镁,请分析①、②两步的目的是________ 。
(3)小明同学在实验室中用 NaOH 溶液替代石灰乳模拟生产过程中的第①步.他取 NaCl 和 MgCl2的固体混合物 25g,加入适量水完全溶解后,与溶质质量分数为 20%的 NaOH 溶液混合充分反应,记录生成的沉淀与加入的 NaOH 溶液质量关系如图所示:________ (写化学式);当滴入上述 NaOH 溶液至图中 B 点时,烧杯中溶液里含有的溶质为________ (写化学式)。
②当滴入上述 NaOH 溶液 100g 时,试通过计算,求此时烧杯中所得不饱和溶液中 NaCl 溶质的质量。________ (计算结果精确至 0.1g)

(2)海水中本身就含有氯化镁,请分析①、②两步的目的是
(3)小明同学在实验室中用 NaOH 溶液替代石灰乳模拟生产过程中的第①步.他取 NaCl 和 MgCl2的固体混合物 25g,加入适量水完全溶解后,与溶质质量分数为 20%的 NaOH 溶液混合充分反应,记录生成的沉淀与加入的 NaOH 溶液质量关系如图所示:

②当滴入上述 NaOH 溶液 100g 时,试通过计算,求此时烧杯中所得不饱和溶液中 NaCl 溶质的质量。
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】连云港市是著名的海滨城市,拥有丰富的海洋资源,开发利用这些宝贵的资源可以有力地促进经济的发展。
(1)从海水中提取出的粗盐中除了含有泥沙等不溶性杂质,还含有 、
、 、
、 等可溶性杂质。如图为我校化学兴趣小组在实验室提纯粗盐的流程图:
等可溶性杂质。如图为我校化学兴趣小组在实验室提纯粗盐的流程图:

①加水溶解之前,将粗盐样品研碎的主要目的是_______ 。
②若沉淀剂分别使用:a. ;b.
;b. ;c.
;c. ,则依次加入沉淀剂的顺序不合理的是
,则依次加入沉淀剂的顺序不合理的是_______ 。(填字母序号)
A.a、b、c B.c、b、a C.b、c、a D.c、a、b
③若优化沉淀剂的种类,则可以使用_______ 溶液代替 和
和 。
。
④操作a和操作b中都使用了玻璃棒,其作用_______ (填“相同”或“不相同”)。操作b中当_______ 时结束实验。
(2)连云港碱厂年产纯碱120万吨,是我国三大纯碱生产企业之一。它的产品除了纯碱外,还有氯化钙和碳酸氢钠。该厂生产纯碱的工艺流程可简单表示如下:

其生产过程中涉及的主要化学反应有:①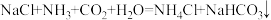 ;②
;②
请回答:
①“碳化”过程中需要的 ,可由石灰石高温煅烧得到,该反应的化学方程式为
,可由石灰石高温煅烧得到,该反应的化学方程式为_______ 。
②该厂“过滤”所得的 可作化肥中的
可作化肥中的_______ 肥,它也可与 在加热时发生反应生成产品
在加热时发生反应生成产品 ,同时还有
,同时还有 和
和 生成,写出该反应的化学方程式:
生成,写出该反应的化学方程式:_______ 。
③该流程中_______ (填化学式)可循环利用。
(3)认真阅读下列材料,回答有关问题。
材料一:融雪剂又称“化冰盐”,它以氯化钙和氯化钠为主要原料,并可根据需要调整配比,广泛应用于冬季道路、停车场、广场等场所的融雪和防冻,以保证人们出行安全。
材料二:节日燃放的烟花,是很多金属化合物在灼烧时呈现出的艳丽色彩。实验中用铂丝蘸取某些金属化合物灼烧时发现:含钠元素的火焰呈黄色,含钙元素的火焰呈砖红色。

I.研究“融雪剂”成分。
结合上述材料,某兴趣小组按如图步骤进行实验,并记录实验现象。
【解释与结论】
①上述实验验证了样品中含有氯化钙,所依据的实验现象是_______ 。该反应的化学方程式是_______ 。
②同学们认为仅通过上述实验,无法确定样品中是否含氯化钠,理由是_______ 。
II.拓展探究
【提出问题】反应后上层清液的溶质成分是什么?
【进行猜想】
猜想一:_______ ;猜想二:氯化钠和碳酸钠;猜想三:氯化钠和氯化钙。
【实验验证】为进一步确定该上层清液的溶质成分,兴趣小组继续设计实验并请你一起完成下面报告:
【交流讨论】用食盐融雪,造成土壤中含盐浓度偏高,使路旁树木死亡。融雪剂还可能会加速钢铁制品的锈蚀,请写出一种路边护栏(钢铁材质)的防锈方法_______ 。
(1)从海水中提取出的粗盐中除了含有泥沙等不溶性杂质,还含有
 、
、 、
、 等可溶性杂质。如图为我校化学兴趣小组在实验室提纯粗盐的流程图:
等可溶性杂质。如图为我校化学兴趣小组在实验室提纯粗盐的流程图:
①加水溶解之前,将粗盐样品研碎的主要目的是
②若沉淀剂分别使用:a.
 ;b.
;b. ;c.
;c. ,则依次加入沉淀剂的顺序不合理的是
,则依次加入沉淀剂的顺序不合理的是A.a、b、c B.c、b、a C.b、c、a D.c、a、b
③若优化沉淀剂的种类,则可以使用
 和
和 。
。④操作a和操作b中都使用了玻璃棒,其作用
(2)连云港碱厂年产纯碱120万吨,是我国三大纯碱生产企业之一。它的产品除了纯碱外,还有氯化钙和碳酸氢钠。该厂生产纯碱的工艺流程可简单表示如下:

其生产过程中涉及的主要化学反应有:①
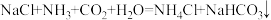 ;②
;②
请回答:
①“碳化”过程中需要的
 ,可由石灰石高温煅烧得到,该反应的化学方程式为
,可由石灰石高温煅烧得到,该反应的化学方程式为②该厂“过滤”所得的
 可作化肥中的
可作化肥中的 在加热时发生反应生成产品
在加热时发生反应生成产品 ,同时还有
,同时还有 和
和 生成,写出该反应的化学方程式:
生成,写出该反应的化学方程式:③该流程中
(3)认真阅读下列材料,回答有关问题。
材料一:融雪剂又称“化冰盐”,它以氯化钙和氯化钠为主要原料,并可根据需要调整配比,广泛应用于冬季道路、停车场、广场等场所的融雪和防冻,以保证人们出行安全。
材料二:节日燃放的烟花,是很多金属化合物在灼烧时呈现出的艳丽色彩。实验中用铂丝蘸取某些金属化合物灼烧时发现:含钠元素的火焰呈黄色,含钙元素的火焰呈砖红色。

I.研究“融雪剂”成分。
结合上述材料,某兴趣小组按如图步骤进行实验,并记录实验现象。
【解释与结论】
①上述实验验证了样品中含有氯化钙,所依据的实验现象是
②同学们认为仅通过上述实验,无法确定样品中是否含氯化钠,理由是
II.拓展探究
【提出问题】反应后上层清液的溶质成分是什么?
【进行猜想】
猜想一:
【实验验证】为进一步确定该上层清液的溶质成分,兴趣小组继续设计实验并请你一起完成下面报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量上层清液于试管中,滴加 | 猜想二成立 |
您最近一年使用:0次
【推荐2】酸、碱、盐为体现自己的应用价值,展开了一场旅行,途中完成了多项任务。
(1)任务一:进厨房除油污
炉具清洁剂去油污的原理是油污和_____ (填字母代号)发生反应。
a.生石灰b.熟石灰c.石灰石d.苛性钠
(2)任务二:进工厂除铁锈、防污染
①工厂用稀硫酸清洗金属器件上的铁锈,溶液变黄,原因是_____ (用化学方程式表示)。
②工人师傅欲向除锈后的废液中加入硝酸钡溶液证明硫酸有剩余,说明其做法不合理的原因_____ 。
③工厂用熟石灰处理废液中硫酸的过程中,反应微观过程如图。请从微粒的角度分析,反应后溶液中的溶质_____ (用化学符号表示)。
为了除去粗盐水中的CaCl2、MgCl2杂质,某化学小组设计了以下实验方案。_____ 。
②写出向粗盐水溶液中加入碳酸钠溶液时反应的化学方程式_____ 。
③有同学提出,可以将流程中加入的过量氢氧化钠溶液换成氢氧化钙溶液,请判断该方案是否可行,并说明理由_____ 。
(4)任务四:进医院降胃酸、促健康
经医院检查小甘爷爷的胃液超标,经计算超标HCl的质量约为0.73g,除去超标的HCl,爷爷需要服用碳酸氢钠片的质量是多少?(结果保留一位小数)
(1)任务一:进厨房除油污
炉具清洁剂去油污的原理是油污和
a.生石灰b.熟石灰c.石灰石d.苛性钠
(2)任务二:进工厂除铁锈、防污染
①工厂用稀硫酸清洗金属器件上的铁锈,溶液变黄,原因是
②工人师傅欲向除锈后的废液中加入硝酸钡溶液证明硫酸有剩余,说明其做法不合理的原因
③工厂用熟石灰处理废液中硫酸的过程中,反应微观过程如图。请从微粒的角度分析,反应后溶液中的溶质

为了除去粗盐水中的CaCl2、MgCl2杂质,某化学小组设计了以下实验方案。

②写出向粗盐水溶液中加入碳酸钠溶液时反应的化学方程式
③有同学提出,可以将流程中加入的过量氢氧化钠溶液换成氢氧化钙溶液,请判断该方案是否可行,并说明理由
(4)任务四:进医院降胃酸、促健康
经医院检查小甘爷爷的胃液超标,经计算超标HCl的质量约为0.73g,除去超标的HCl,爷爷需要服用碳酸氢钠片的质量是多少?(结果保留一位小数)
您最近一年使用:0次
【推荐3】山东省有漫长的海岸线,蕴藏着丰富的海洋资源:(已知:20℃氯化钠的溶解度为36g,水的密度可近似看作1g/mL)
(1)海水淡化。反渗透膜法与过滤法在原理上都是利用混合体系中各物质的_____ 不同进行分离的方法。
(2)海水晒盐。从化学视角看,海水晒盐是采用了_____ 的分离方法,从海水中获得NaCl不采用降温结晶的方法,原因是_____ 。
(3)粗盐提纯。

①操作Ⅰ、Ⅱ的名称依次为_____ 、_____ 。
②20℃时提纯9g粗盐,若已知粗盐中氯化钠含量约为80%,溶解时应选择哪一种规格的量筒量取所需要的水最为合适_____ (提供的量筒规格有“10mL”、“25mL”和“100mL”)。
(4)粗盐纯化。某氯化钠溶液中含有Mg2+、SO42-、Ca2+,若用化学沉淀法依次除去Mg2+、SO42-、Ca2+,需要的三种离子分别是_____ (写离子符号)。
(5)海水制镁。如果要充分利用海边贝壳〔主要成份碳酸钙)和苦卤进行海水制镁的流程图如下:

写出上述流程中,①、③、④、⑤的化学方程式:①_____ 、③_____ 、④_____ 、⑤_____ ;上述四个化学方程式中,其中属于分解反应的是_____ 。
(6)海水制碱。如图是工业上采用氨碱法生产纯碱的流程图:

请回答下列问题:
①写出步骤①的化学方程式_____ ;
②氨溶于水后会与水反应生成一水合氨(NH3﹒H2O),我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通入二氧化碳,其原因是_____ ;
③氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵,首先结晶析出的物质是_____ (填化学式),其原因是_____ 。
(1)海水淡化。反渗透膜法与过滤法在原理上都是利用混合体系中各物质的
(2)海水晒盐。从化学视角看,海水晒盐是采用了
(3)粗盐提纯。

①操作Ⅰ、Ⅱ的名称依次为
②20℃时提纯9g粗盐,若已知粗盐中氯化钠含量约为80%,溶解时应选择哪一种规格的量筒量取所需要的水最为合适
(4)粗盐纯化。某氯化钠溶液中含有Mg2+、SO42-、Ca2+,若用化学沉淀法依次除去Mg2+、SO42-、Ca2+,需要的三种离子分别是
(5)海水制镁。如果要充分利用海边贝壳〔主要成份碳酸钙)和苦卤进行海水制镁的流程图如下:

写出上述流程中,①、③、④、⑤的化学方程式:①
(6)海水制碱。如图是工业上采用氨碱法生产纯碱的流程图:

请回答下列问题:
①写出步骤①的化学方程式
②氨溶于水后会与水反应生成一水合氨(NH3﹒H2O),我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通入二氧化碳,其原因是
③氨盐水吸收二氧化碳后生成的碳酸氢钠和氯化铵,首先结晶析出的物质是
您最近一年使用:0次



