24. 从海水中获取的食盐是一种里要的工业原料。
(1)组成。
构成NaCl晶体的微粒为
_________(填离子符号)。
(2)提取。
①1000g海水含有27.2 gNaCl,则海水中NaCl的质量分数为
__________。海水晒盐的基本原理是
_________。
②海水晒制的粗盐中含有MgCl
2、CaCl
2和Na
2SO
4等少量可溶性杂质和泥沙。为除去可溶性杂质,将粗盐样品溶于水,可依次加入过量
_________(填一种试剂)和Na
2CO
3溶液,充分反应后过滤,向滤液中加入过量的稀盐酸,搅拌,煮沸得NaCl溶液。加入稀盐酸的目的是
_________。
(3)应用。
①通过电解饱和NaCl溶液制备NaOH,反应的化学方程式:

,则X的化学式为
_________。
②电解熔融NaCl可得到金属Na和另一种单质,该反应的化学方程式为
________。
(4)拓展。
I.“侯氏制碱法”生产纯碱的过程中,碳酸氢钠的生成是至关重要的一环,其原理是:
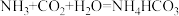
,

。兴趣小组在常温(20℃)下设计并完成了如图1所示实验。
【已知20℃时NaCl、NH
4HCO
3、NaHCO
3、NH
4Cl的溶解度为36.0g、21.0g、9.6g、37.2g。】
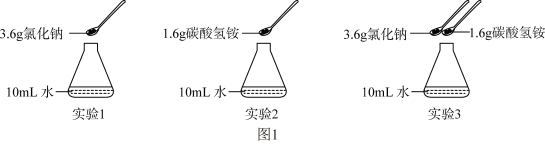
①实验1、2所得溶液处于饱和状态的是
________。(填序号)
②实验3的锥形瓶中出现白色浑浊,经检验为NaHCO
3,写出用稀盐酸检验NaHCO
3的化学方程式:
_______。
Ⅱ.侯氏制碱法的生产流程如图2所示:
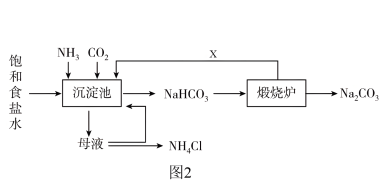
①实际生产中沉淀池内的温度不能太高,原因是
_________。
②请结合如图的信息,写出NaHCO
3晶体能析出的原因
_________。
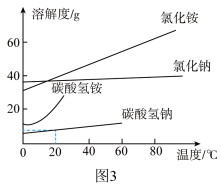
③图3是四种物质的溶解度曲线。母液中含有较高浓度的NH
4Cl和少量NaCl,利用降温结晶的方法可提纯NH
4Cl,理由是
_________。
④上述流程中可循环利用的物质有:NaCl和
_________。
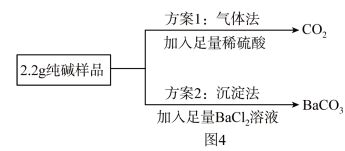
Ⅲ.测定纯碱样品中碳酸钠的质量分数。
纯碱产品中常混有少量氯化钠,兴趣小组设计图4所示两种方案测定某纯碱样品中碳酸钠的质量分数:根据方案1,实验测得CO
2的质量为0.88g。根据方案2,实验测得BaCO
3的质量为3.94g请任选其中一种方案与相关数据,计算该纯碱样品中碳酸钠的质量分数
_______(写出计算过程,结果精确到0.1%)。