市面上售卖的低钠盐通过添加一定量的 MgSO4,可以帮助改善体内钠、镁的平衡状态,预防高血压。小雪欲测定某低钠盐中 MgSO4 的质量分数,进行如下实验。
(1)称量 40.0g 低钠盐溶于适量的水配得溶液,滴加 10% 的氢氧化钠溶液,同时用 pH 传感器监测溶液酸碱度,并绘制了溶液 pH 随时间变化的图像。_______ 、洗涤、干燥后测得生成沉淀的质量为1.74g。
【数据分析】
(2)小雪认为该低钠盐溶液呈酸性,她的判断依据是_______ 。
(3)Mg(OH)2 沉淀生成对应着图像的 段(填大写字母序号)。
(4)请计算该低钠盐中硫酸镁的质量分数。(根据化学方程式计算,并写出计算过程)

(1)称量 40.0g 低钠盐溶于适量的水配得溶液,滴加 10% 的氢氧化钠溶液,同时用 pH 传感器监测溶液酸碱度,并绘制了溶液 pH 随时间变化的图像。
【数据分析】
(2)小雪认为该低钠盐溶液呈酸性,她的判断依据是
(3)Mg(OH)2 沉淀生成对应着图像的 段(填大写字母序号)。
| A.a—b | B.b—c | C.c—d | D.b—d |
(4)请计算该低钠盐中硫酸镁的质量分数。(根据化学方程式计算,并写出计算过程)
更新时间:2024-04-12 11:16:19
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】小红有一只银手镯(银锌合金),标签标识为925银(925银一般是指含银量为92.5%的银制品)。小红想用实验探究手国中银的含量,先用电子秤称得手的质量是25.00g再用稀盐酸分多次与此手镯充分反应,实验数据如下表:
根据上表中数据分析,完成下列问题:(写出计算过程)
(1)该手镯中银的质量分数。
(2)所用稀盐酸的溶质质量分数。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量(g) | 10.00 | 10.00 | 10.00 | 10.00 | 10.00 |
| 充分反应后剩余固体的质量(g) | 24.35 | 23.70 | 23.05 | 23.00 | 23.00 |
(1)该手镯中银的质量分数。
(2)所用稀盐酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取石灰石样品20g于烧杯中,加入50g稀盐酸,充分反应后,不再产生气体后的关系图如下:

(1)计算碳酸钙中Ca元素的百分含量___ 。
(2)Ca : C: O元素的质量比是____ 。
(3)X的值是__________ g。
(4)计算石灰石样品中碳酸钙的含量(要有计算过程)。

(1)计算碳酸钙中Ca元素的百分含量
(2)Ca : C: O元素的质量比是
(3)X的值是
(4)计算石灰石样品中碳酸钙的含量(要有计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】用海水吸收含硫烟气中的 并生产石膏(主要成分
并生产石膏(主要成分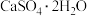 )的主要物质转化关系如下:
)的主要物质转化关系如下:
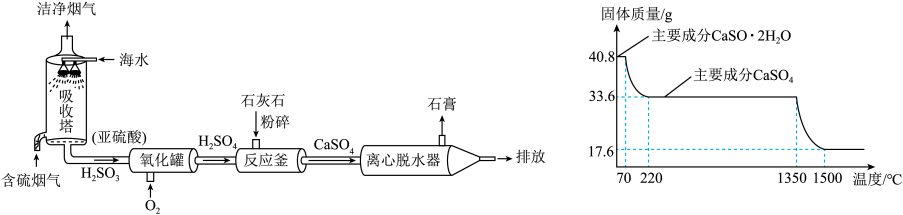
(1)吸收塔中,生成一种酸——亚硫酸(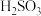 ),其溶液显酸性。若将二氧化硫气体通入紫色石蕊溶液中,可能出现的现象是
),其溶液显酸性。若将二氧化硫气体通入紫色石蕊溶液中,可能出现的现象是_____ 。
(2)现取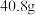 石膏药品进行加热,固体质量随温度的变化如图(杂质不参加反应且不含钙元素)。
石膏药品进行加热,固体质量随温度的变化如图(杂质不参加反应且不含钙元素)。
①石膏开始分解的温度是_______ 。
②计算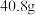 该石膏样品中含有
该石膏样品中含有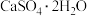 的质量。
的质量。_______ (写出计算过程)
③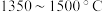 时,
时,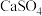 继续分解生成氧化钙、二氧化硫和氧气,最终剩余的
继续分解生成氧化钙、二氧化硫和氧气,最终剩余的 固体中含有
固体中含有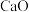 的质量为
的质量为_______ 。
 并生产石膏(主要成分
并生产石膏(主要成分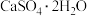 )的主要物质转化关系如下:
)的主要物质转化关系如下:
(1)吸收塔中,生成一种酸——亚硫酸(
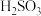 ),其溶液显酸性。若将二氧化硫气体通入紫色石蕊溶液中,可能出现的现象是
),其溶液显酸性。若将二氧化硫气体通入紫色石蕊溶液中,可能出现的现象是(2)现取
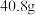 石膏药品进行加热,固体质量随温度的变化如图(杂质不参加反应且不含钙元素)。
石膏药品进行加热,固体质量随温度的变化如图(杂质不参加反应且不含钙元素)。①石膏开始分解的温度是
②计算
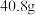 该石膏样品中含有
该石膏样品中含有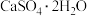 的质量。
的质量。③
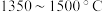 时,
时,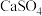 继续分解生成氧化钙、二氧化硫和氧气,最终剩余的
继续分解生成氧化钙、二氧化硫和氧气,最终剩余的 固体中含有
固体中含有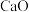 的质量为
的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】查阅资料可知:无水硫酸铜是白色晶体,在20℃时,100g水中最多溶解32gCuSO4。在20℃时,小明同学将40gCuSO4固体加入到盛有100g水的烧杯中,充分搅拌后。请填写下列空白:
(1)小明所得溶液是20℃时CuSO4的_________ 溶液(填“饱和”或“不饱和”);用pH试纸测得该溶液的pH<7,说明溶液显________ 性。
(2)经实验证明,取少量10%硫酸铜溶液加入到过氧化氢溶液也能达到与MnO2相同的效果。现将(1)中所得的硫酸铜溶液稀释为10%硫酸铜溶液,需加水_________ g。
(3)小明同学现取一定质量的过氧化氢溶液和硫酸铜溶液混合,过氧化氢完全分解后,实验数据如下表:请计算:
①反应生成氧气的质量为_________ g。
②反应后硫酸铜溶液中溶质质量是___________
③求参加反应的过氧化氢的质量___________
(1)小明所得溶液是20℃时CuSO4的
(2)经实验证明,取少量10%硫酸铜溶液加入到过氧化氢溶液也能达到与MnO2相同的效果。现将(1)中所得的硫酸铜溶液稀释为10%硫酸铜溶液,需加水
(3)小明同学现取一定质量的过氧化氢溶液和硫酸铜溶液混合,过氧化氢完全分解后,实验数据如下表:请计算:
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和过氧化氢溶液的质量/g | 硫酸铜溶液的质量/g | 烧杯和烧杯中溶液的质量/g |
| 60.0 | 6.6 | 65.0 | |
②反应后硫酸铜溶液中溶质质量是
③求参加反应的过氧化氢的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】学习小组同学通过下面实验测定某铜锌合金中铜的质量分数。

(1)反应过程生成氢气的质量为_____ g。
(2)计算黄铜中铜的质量分数。
(3)若硫酸锌溶液为中性,反应结束后所得溶液的
_____ (选填“>”“=”或“<”)7.

(1)反应过程生成氢气的质量为
(2)计算黄铜中铜的质量分数。
(3)若硫酸锌溶液为中性,反应结束后所得溶液的

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】学习酸碱中和反应时,很多同学对其产生了探究兴趣。
(1)甲同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,用手轻轻触摸试管外壁,感觉发烫,于是他得出“酸碱中和反应是放热反应”的结论,乙同学认为甲同学推理不合理,他的理由是 1 。
(2)乙同学为了验证甲同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀硫酸质量的变化
如图所示:

①由图知,稀硫酸与氢氧化钠溶液发生的反应是 2 (填“放热”或“吸热”)反应,B点表示的含义 3 。
②从A到B过程中,烧杯中溶液pH逐渐 4 。
③B到C的过程中,烧杯内溶液中含有的阳离子有(填离子符号) 5 。
(3)为了测定所用稀硫酸中溶质的质量分数,做了以下实验:取50g这种稀硫酸,加入40g、20%的氢氧化钠溶液,两者恰好完全反应。试计算:
①所用稀硫酸中溶质的质量分数。 6
②反应后所得溶液中溶质的质量分数。 7
(1)甲同学将固体氢氧化钠放入装有稀硫酸的试管中并振荡,用手轻轻触摸试管外壁,感觉发烫,于是他得出“酸碱中和反应是放热反应”的结论,乙同学认为甲同学推理不合理,他的理由是
(2)乙同学为了验证甲同学的结论,将实验加以改进:将稀硫酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出氢氧化钠溶液温度随加入稀硫酸质量的变化
如图所示:

①由图知,稀硫酸与氢氧化钠溶液发生的反应是
②从A到B过程中,烧杯中溶液pH逐渐
③B到C的过程中,烧杯内溶液中含有的阳离子有(填离子符号)
(3)为了测定所用稀硫酸中溶质的质量分数,做了以下实验:取50g这种稀硫酸,加入40g、20%的氢氧化钠溶液,两者恰好完全反应。试计算:
①所用稀硫酸中溶质的质量分数。
②反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】一定质量的石灰石与足量稀盐酸反应生成22gCO2,求该石灰石中碳酸钙的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】课外小组的同学研究的课题是测定贝壳中碳酸钙的质量分数,他们取25g贝壳粉碎后放入烧杯中,当向烧杯中加入稀盐酸至100g时发现不再产生气泡,并测得烧杯内固体和液体总质量为120.6g (杂质不与盐酸反应)。求:
(1)生成二氧化碳的质量___________
(2)贝壳中碳酸钙的质量分数为__________(要求写出必要的解题过程)
(1)生成二氧化碳的质量___________
(2)贝壳中碳酸钙的质量分数为__________(要求写出必要的解题过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】小慧称取20g某氯化铜样品放入烧杯中,加入50g水使氯化铜完全溶解,逐滴加入一定溶质质量分数的氢氧化钾溶液,反应生成沉淀的质量与所加氢氧化钾溶液质量的关系如图所示,(提示① ,氯化铜样品中所含杂质既不溶于水,也不参与反应。)
,氯化铜样品中所含杂质既不溶于水,也不参与反应。)

试计算:
(1)生成沉淀的质量为______ g;
(2)当恰好完全反应时,所得溶液的溶质质量分数是多少?
 ,氯化铜样品中所含杂质既不溶于水,也不参与反应。)
,氯化铜样品中所含杂质既不溶于水,也不参与反应。)
试计算:
(1)生成沉淀的质量为
(2)当恰好完全反应时,所得溶液的溶质质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】请结合下图实验回答有关问题:

(1)上图中操作a的名称是_______ ,该操作中所需的玻璃仪器有烧杯、玻璃棒和__________ 。
(2)上图中x的值为___________ 。
(3)检验上述实验中产生气体的方法是______ ,反应中共产生该气体的质量为_____ g。
(4)计算参加反应的过氧化氢质量是多少?(写出计算过程)。

(1)上图中操作a的名称是
(2)上图中x的值为
(3)检验上述实验中产生气体的方法是
(4)计算参加反应的过氧化氢质量是多少?(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室制取氧气时,某同学取氯酸钾和二氧化锰的混合固体16.25g,加热,根据图像及结合所学知识回答下列问题:

(1)加热固体时,试管口要略向下倾斜的目的是:_____ 。
(2)该同学制得氧气的质量为_____ g。
(3)计算混合固体中氯酸钾的质量。(写出计算过程)
(4)反应过程中,固体中钾元素的质量分数_____ 。(选填“增大”、“不变”或“减小”)。
(5)要从该同学制取氧气后的残余固体中分离出二氧化锰,正确的操作步骤是先溶解,再_____ (提示:任何含钾化合物都能溶于水,二氧化锰不溶于水)。

(1)加热固体时,试管口要略向下倾斜的目的是:
(2)该同学制得氧气的质量为
(3)计算混合固体中氯酸钾的质量。(写出计算过程)
(4)反应过程中,固体中钾元素的质量分数
(5)要从该同学制取氧气后的残余固体中分离出二氧化锰,正确的操作步骤是先溶解,再
您最近一年使用:0次

 ,将其慢慢通入盛有过量澄清石灰水的试管中,充分反应后得到
,将其慢慢通入盛有过量澄清石灰水的试管中,充分反应后得到 和澄清石灰水不反应)
和澄清石灰水不反应)

