为了使除铁锈的废液得到综合利用(其他杂质忽略,溶质成分为FeCl3),需测定废液中溶质的质量分数,进行如图实验。
(1)写出发生反应的化学方程式______ 。
(2)样品中FeCl3的质量为X,列出求解X的比例式______ 。
(3)废液样品中溶质的质量分数为_______ 。
(4)将反应后所得溶液加入_____ g水,可以得到溶质质量分数为10%的溶液。
(5)若工厂处理10t这样的废液,需要NaOH固体的质量为______ 。
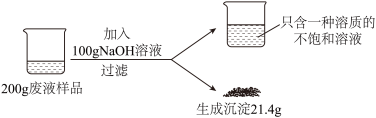
(1)写出发生反应的化学方程式
(2)样品中FeCl3的质量为X,列出求解X的比例式
(3)废液样品中溶质的质量分数为
(4)将反应后所得溶液加入
(5)若工厂处理10t这样的废液,需要NaOH固体的质量为
更新时间:2024-04-13 16:05:23
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】海鲜速运包装箱里常用过氧化钙(化学式为CaO2)与水反应生成氢氧化钙和氧气。求用72g过氧化钙和足量的水反应可以制取多少g氧气?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】碳酸氢钠(NaHCO3)受热易分解,生产碳酸钠、水和二氧化碳,反应的化学方程式为____。充分加热44.2g含碳酸钠的碳酸氢钠固体,反应前后固体中钠元素的质量分数之比为159:221,则生成水和二氧化碳的质量之和为____g。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐3】化学储氢材料研发是当下科技研究的热点之一。
(1)下列化学储氢材料中含氢量最高的是______(填字母)。
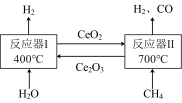
(2)我国科学家发明了一种将甲烷中的氢转化为氢气的工艺(原理如图所示)。 。
。
①反应器Ⅰ中的化学反应方程式为______ 。
②当甲烷的转化率(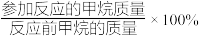 )为80%时,理论上1.0吨甲烷与足量水蒸气反应生成氢气的总质量是
)为80%时,理论上1.0吨甲烷与足量水蒸气反应生成氢气的总质量是______ 吨。(请将计算过程写到答题卡上)
(1)下列化学储氢材料中含氢量最高的是______(填字母)。
A. | B. | C. |
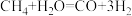 。
。①反应器Ⅰ中的化学反应方程式为
②当甲烷的转化率(
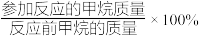 )为80%时,理论上1.0吨甲烷与足量水蒸气反应生成氢气的总质量是
)为80%时,理论上1.0吨甲烷与足量水蒸气反应生成氢气的总质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某同学在实验室发现一瓶标签残缺的硫酸铜溶液。为了测定此溶液的溶质质量分数,他取出100g该溶液,向其中逐滴加入溶质质量分数为10.4%的氯化钡溶液。反应过程中生成沉淀的质量与所用氯化钡溶液质量的关系如图所示。请你仔细分析此关系图,并进行计算。

(1)当滴入氯化钡溶液________ g时,硫酸铜与氯化钡溶液恰好完全反应,此时溶液中的溶质为________ (填化学式)。
(2)计算此硫酸铜溶液中溶质的质量分数(写出解题过程)。

(1)当滴入氯化钡溶液
(2)计算此硫酸铜溶液中溶质的质量分数(写出解题过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某中学化学兴趣小组的同学取22克工业纯碱样品(含少量氯化钠)放入烧杯中,将220g稀盐酸分五次加入,充分反应,五次测量所得数据如表所示,请计算:
(1)恰好完全反应时,生成二氧化碳的质量为_______ g。
(2)该稀盐酸的溶质质量分数是多少?______ (写出计算过程,计算结果保留到0.1%)
| 次数 | 一 | 二 | 三 | 四 | 五 |
| 累计加入稀盐酸的质量/g | 50 | 100 | 150 | 200 | 220 |
| 烧杯中溶液的总质量/g | 69.8 | 117.6 | 165.4 | 213.2 | 233.2 |
(1)恰好完全反应时,生成二氧化碳的质量为
(2)该稀盐酸的溶质质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验室有一份在空气中部分变质的氢氧化钠样品,质量为3.72g。某实验小组将这份样品完全溶解,配成50g溶液,然后缓慢滴入14.6%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液pH和溶液总质量,部分数据如表所示:
请分析计算:
(1)实验中生成二氧化碳的质量为_____ g。
(2)求样品中氢氧化钠的质量______ g。
(3)当恰好完全反应时,该溶液的溶质质量分数。(写出计算过程,结果保留一位小数)
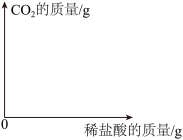
(4)请在如图中画出稀盐酸质量与二氧化碳质量关系的图像。(温馨提醒:不用写出计算过程,但要标出关键点的数据)
| 测量次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 滴加的盐酸总质量/g | 0 | 5 | 20 | 30 | 35 |
| 溶液总质量/g | 50 | 55 | 69.12 | 79.12 | 84.12 |
| 溶液pH | 12.4 | 12.1 | 7.0 | 2.2 | 2.1 |
(1)实验中生成二氧化碳的质量为
(2)求样品中氢氧化钠的质量
(3)当恰好完全反应时,该溶液的溶质质量分数。(写出计算过程,结果保留一位小数)
(4)请在如图中画出稀盐酸质量与二氧化碳质量关系的图像。(温馨提醒:不用写出计算过程,但要标出关键点的数据)

您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】我国化学家侯德榜创立了侯氏制碱法,为世界制碱工业作出了杰出贡献。在实际生产的产品碳酸钠中会混有少量的氯化钠,现有纯碱样品22.8g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体全部逸出,得到不饱和氯化钠溶液。反应过程中测得烧杯内溶液的质量(m)与反应时间(t)关系如图所示。试回答:
(2)22.8g样品中碳酸钠的质量为多少?
(3)计算所得溶液中溶质的质量分数。

(2)22.8g样品中碳酸钠的质量为多少?
(3)计算所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某小组欲用质量分数为7.3%的盐酸测一瓶标签破损的NaOH溶液的质量分数.

实验如下:取40g氢氧化钠溶液于烧杯中,然后把60g质量分数为7.3%的稀盐酸慢慢滴入到烧杯中,同时用电子pH计不断读取反应时的pH,得出如图所示的关系。求;
(1)该氢氧化钠溶液的溶质质量分数______。
(2)配制100g上述稀盐酸,需要质量分数为36.5%的浓盐酸多少克_______?

实验如下:取40g氢氧化钠溶液于烧杯中,然后把60g质量分数为7.3%的稀盐酸慢慢滴入到烧杯中,同时用电子pH计不断读取反应时的pH,得出如图所示的关系。求;
(1)该氢氧化钠溶液的溶质质量分数______。
(2)配制100g上述稀盐酸,需要质量分数为36.5%的浓盐酸多少克_______?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】实验室中取2.5g石灰石于烧杯中,将20g足量稀盐酸分批次加入样品中,充分反应后经过滤、干燥、称重得到如下数据:请计算:
已知杂质既不与酸反应也不溶于水。
(1)生成二氧化碳的质量为______ g。
(2)最后所得溶液中氯化钙的质量分数(结果精确到0.1%)。
| 实验次序 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 稀盐酸用量/g | 4.0 | 4.0 | 4.0 | 4.0 | 4.0 |
| 剩余固体质量/g | 2.0 | 1.5 | 1.0 | 0.5 | 0.5 |
已知杂质既不与酸反应也不溶于水。
(1)生成二氧化碳的质量为
(2)最后所得溶液中氯化钙的质量分数(结果精确到0.1%)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】为测定某 溶液的溶质质量分数,化学小组的同学取
溶液的溶质质量分数,化学小组的同学取 溶液100g,向其中滴加一定浓度的
溶液100g,向其中滴加一定浓度的 溶液,随着
溶液,随着 溶液的加入,生成沉淀的质量如表:
溶液的加入,生成沉淀的质量如表:
(1)第Ⅱ组数据n为__________ g;
(2)求该 溶液中溶质的质量分数。(写出计算过程)
溶液中溶质的质量分数。(写出计算过程)
 溶液的溶质质量分数,化学小组的同学取
溶液的溶质质量分数,化学小组的同学取 溶液100g,向其中滴加一定浓度的
溶液100g,向其中滴加一定浓度的 溶液,随着
溶液,随着 溶液的加入,生成沉淀的质量如表:
溶液的加入,生成沉淀的质量如表:| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 | 第Ⅴ组 | 第Ⅵ组 | |
| 氢氧化钠溶液的质量/g | 16 | 32 | 48 | 64 | 80 | 96 |
| 生成沉淀的质量/g | 1.96 | n | 5.88 | 7.84 | 9.80 | 9.80 |
(2)求该
 溶液中溶质的质量分数。(写出计算过程)
溶液中溶质的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某同学在实验室发现一瓶标签残缺(如图所示)的溶液.为了测定此溶液的溶质质量分数,他取出25g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液.反应过程中生成沉淀的质量与所用NaOH溶液质量的关系如图所示.请计算此溶液的溶质质量分数.


您最近一年使用:0次



