已知 ,发酵粉的主要成分是NaHCO3,现取样品20g,加热一段时间后,固体质量为16.9g,向固体中加入过量稀盐酸,蒸发结晶得到14.9固体,假设杂质不参与任何反应,下列判断正确的是
,发酵粉的主要成分是NaHCO3,现取样品20g,加热一段时间后,固体质量为16.9g,向固体中加入过量稀盐酸,蒸发结晶得到14.9固体,假设杂质不参与任何反应,下列判断正确的是
 ,发酵粉的主要成分是NaHCO3,现取样品20g,加热一段时间后,固体质量为16.9g,向固体中加入过量稀盐酸,蒸发结晶得到14.9固体,假设杂质不参与任何反应,下列判断正确的是
,发酵粉的主要成分是NaHCO3,现取样品20g,加热一段时间后,固体质量为16.9g,向固体中加入过量稀盐酸,蒸发结晶得到14.9固体,假设杂质不参与任何反应,下列判断正确的是| A.加热产生二氧化碳和水的质量为3.1g | B.原发酵粉中NaHCO3的质量分数为80% |
| C.16.9g固体中含有碳酸钠的质量为5.3g | D.蒸发结晶得到的固体中不可能含HCl |
更新时间:2024/04/16 07:06:30
|
相似题推荐
多选题
|
较难
(0.4)
【推荐1】下列图像与对应的叙述相符合的是
A.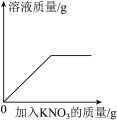 图 A 是一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 图 A 是一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 |
B.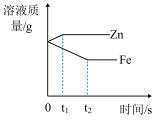 图 B 是分别向足量相同的硫酸铜溶液中加入质量相等的锌粉和铁粉 图 B 是分别向足量相同的硫酸铜溶液中加入质量相等的锌粉和铁粉 |
C.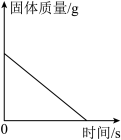 图 C 是高温灼烧一定质量的大理石 图 C 是高温灼烧一定质量的大理石 |
D.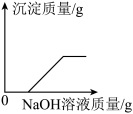 图 D 是向一定质量的 HCl 和 MgCl2的混合溶液中,逐滴加入 NaOH 溶液 图 D 是向一定质量的 HCl 和 MgCl2的混合溶液中,逐滴加入 NaOH 溶液 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】现向20gMgO和CuO的某混合物中加入150g稀盐酸至恰好完全反应,再向所得溶液中加入足量NaOH溶液至充分反应后,生成沉淀的总质量为27.2g,下列说法中,正确的是
| A.原混合物中金属元素的质量为13.6g |
| B.所加稀盐酸的溶质质量分数为14.6% |
| C.参见反应的NaOH的质量为32g |
| D.混合物中MgO质量为12g |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】烧杯中盛有4.9gMgO和Mg(OH)2的固体混合物,向其中加入100g溶质质量分数为7.3%的稀盐酸,恰好完全反应,得到该温度下的不饱和溶液。则下列说法中,正确的是
| A.反应后所得溶液中溶质的质量为9.5g | B.原固体混合物中镁元素的质量为2.4g |
| C.固体混合物中氧元素的质量为2.4g | D.原固体混合物中氧化镁的质量分数约为60% |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】有一包不纯的碳酸钠粉末,可能含有硫酸钠、氢氧化钠中的一种或两种,某兴趣小组为探究其组成做了如下实验:
I、取16g样品于烧杯中加水溶解。再向烧杯中滴加硝酸钡溶液并不断搅拌,烧杯内固体的质量随加入硝酸钡溶液的质量的变化如图甲所示。
Ⅱ、从B点开始,向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图乙所示。
I、取16g样品于烧杯中加水溶解。再向烧杯中滴加硝酸钡溶液并不断搅拌,烧杯内固体的质量随加入硝酸钡溶液的质量的变化如图甲所示。
Ⅱ、从B点开始,向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图乙所示。
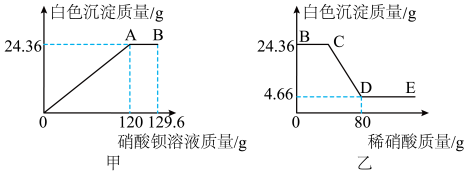
| A.该样品中一定有NaOH,可能有Na2SO4 | B.E点溶液中的阳离子为H+、Na+ |
| C.加入硝酸钡溶液的溶质质量分数为26.1% | D.该样品中NaOH的质量为2.56g |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐3】某 和CaO的混合粉末中钙元素与氧元素的质量比为2:1,现取m g的混合粉末高温煅烧,充分反应后得到固体5.6g,则下列有关说法中,正确的是
和CaO的混合粉末中钙元素与氧元素的质量比为2:1,现取m g的混合粉末高温煅烧,充分反应后得到固体5.6g,则下列有关说法中,正确的是
 和CaO的混合粉末中钙元素与氧元素的质量比为2:1,现取m g的混合粉末高温煅烧,充分反应后得到固体5.6g,则下列有关说法中,正确的是
和CaO的混合粉末中钙元素与氧元素的质量比为2:1,现取m g的混合粉末高温煅烧,充分反应后得到固体5.6g,则下列有关说法中,正确的是| A.所得5.6g固体中只有氧化钙一种物质 |
| B.该mg的混合粉末中氧元素的质量为1.6g |
| C.向m g的混合粉末中加入100g10%稀盐酸充分反应后,所得溶液质量为105.6g |
| D.煅烧过程中生成二氧化碳的总质量为0.55g |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】如图为三种物质的溶解度曲线。下列说法错误的是


| A.约在64℃时,KCl和Na2SO4的溶解度相等 |
| B.在室温至100℃区间,随着温度的升高,Na2SO4的溶解度先增大后减小,醋酸钙则相反 |
| C.分离含少量KCl的Na2SO4溶液,可采用蒸发结晶的方法 |
| D.在40℃时,将40gKCl固体放入60g水后充分搅拌,得到溶质质量分数为40%的KCl溶液 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】甲、乙两种固体物质的溶解度曲线如图所示。下列有关叙述中错误的是
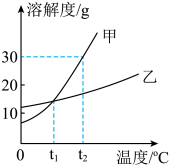

| A.t2℃时,要溶解相同质量的甲、乙两种物质,甲需要水的量多 |
| B.t2℃时,将25g甲物质放入50g水中,所得溶液的质量为75g |
| C.升高温度可将甲物质的饱和溶液变为不饱和溶液 |
| D.当甲物质中含少量乙物质时,可用降温结晶的方法提纯甲物质 |
您最近一年使用:0次




