市场上热销的蒸汽眼罩如图1所示,小组同学打开一个眼罩,剪开后发现有一些黑色固体粉末和一些白色固体。于是对眼罩内填充的物质展开了以下探究。
探究一:黑色粉末是什么?
【作出猜想】同学们利用所学知识,结合眼罩在空气中与水分反应的发热原理,作出如下猜想:①炭粉;②铁粉;③炭粉和铁粉。
(1)【设计实验】
【实验结论】猜想③正确,蒸汽眼罩是利用铁粉生锈发热的原理工作的。
(2)【实验反思】步骤2中,实验结束后应___________ ,避免因操作不当引起试管炸裂。
探究二:白色固体的成分是什么?
【查阅资料】铁生锈过程中含钠离子的化合物能加快反应速率,缩短反应时间。
【作出猜想】①NaOH;②NaCl;③Na2CO3;④Na2SO4。
(3)【交流讨论】小组同学根据蒸汽眼罩的使用环境,认为不可能是NaOH,理由是______ 。
(4)【进行实验】取白色固体于烧杯中加水溶解,静置,取上层清液于试管中,滴加BaCl2溶液,观察到无沉淀产生,则推测白色固体的成分为___________ 。
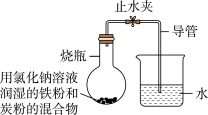
【拓展延伸】通过探究一可知,蒸汽眼罩中的黑色固体是炭粉和铁粉,小组同学想知道在铁粉生锈发热时炭粉起到什么作用?于是利用浓度为3.6%的NaCl溶液,2.0g铁粉与不同质量的炭粉混合进行如图所示实验,打开止水夹,记录烧杯中水开始倒吸进入烧瓶所消耗的时间,如下表:
___________ 。
【反思总结】
(6)蒸汽眼罩虽能缓解疲劳,但也不能长时间佩戴。下列有关蒸汽眼罩的相关说法中正确的是___________(选填字母)。

探究一:黑色粉末是什么?
【作出猜想】同学们利用所学知识,结合眼罩在空气中与水分反应的发热原理,作出如下猜想:①炭粉;②铁粉;③炭粉和铁粉。
(1)【设计实验】
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:取少量黑色粉末于试管中,加入一定量 | 观察到黑色粉末部分溶解,产生气泡,溶液变为浅绿色 | 黑色粉末中有 |
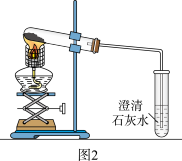
| 步骤2:另取少量黑色粉末用磁铁吸引,将剩余固体与氧化铜粉末混合,用图2所示的装置进行实验。 | 观察到 | 黑色粉末中含有炭粉。 |
【实验结论】猜想③正确,蒸汽眼罩是利用铁粉生锈发热的原理工作的。
(2)【实验反思】步骤2中,实验结束后应
探究二:白色固体的成分是什么?
【查阅资料】铁生锈过程中含钠离子的化合物能加快反应速率,缩短反应时间。
【作出猜想】①NaOH;②NaCl;③Na2CO3;④Na2SO4。
(3)【交流讨论】小组同学根据蒸汽眼罩的使用环境,认为不可能是NaOH,理由是
(4)【进行实验】取白色固体于烧杯中加水溶解,静置,取上层清液于试管中,滴加BaCl2溶液,观察到无沉淀产生,则推测白色固体的成分为
【拓展延伸】通过探究一可知,蒸汽眼罩中的黑色固体是炭粉和铁粉,小组同学想知道在铁粉生锈发热时炭粉起到什么作用?于是利用浓度为3.6%的NaCl溶液,2.0g铁粉与不同质量的炭粉混合进行如图所示实验,打开止水夹,记录烧杯中水开始倒吸进入烧瓶所消耗的时间,如下表:
| 炭粉的质量/g | 0.5 | 1.0 | 2.0 | 2.5 | …… |
| 时间/s | 1468 | 376 | 212 | 162 | …… |
【反思总结】
(6)蒸汽眼罩虽能缓解疲劳,但也不能长时间佩戴。下列有关蒸汽眼罩的相关说法中正确的是___________(选填字母)。
| A.蒸汽眼罩可以循环使用 |
| B.蒸汽眼罩戴的越久,效果越好 |
| C.蒸汽眼罩开封后立即使用,以保证效果 |
2024·江西新余·一模 查看更多[1]
更新时间:2024-05-08 17:29:26
|
相似题推荐
【推荐1】某兴趣小组为探究Mg、Fe、Cu、Ag四种金属的活动性进行如图甲、乙、丙三个实验。(注:所用金属大小形状相同、酸的体积浓度相同)
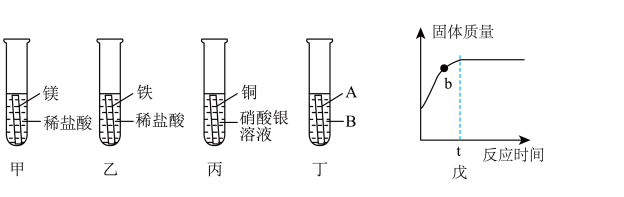
(1)甲试管中的实验现象为_____ 。
(2)小组同学随后发现该实验无法得出四种金属的活动性顺序,于是补充图丁试管中实验,最终得出四种金属活动性:Mg>Fe>Cu>Ag,则补充实验中的试剂A、B分别为_____ (填序号)。
①Zn和CuSO4
②Fe和CuSO4
③Fe和AgNO3
④Zn和AgNO3
(3)小组同学将丙试管中的物质过滤后,向滤液中加入甲中剩余的镁,析出固体质量的变化随反应时间的关系如戊图所示。
①对析出固体的成分提出以下四种猜想:
A Mg、Cu、Ag
B Mg、Cu
C Cu、Ag
D Ag
这四种猜想中明显不合理的是_____ (填编号)。
②写出b点对应溶液中所含的金属离子是_____ (填离子符号)。

(1)甲试管中的实验现象为
(2)小组同学随后发现该实验无法得出四种金属的活动性顺序,于是补充图丁试管中实验,最终得出四种金属活动性:Mg>Fe>Cu>Ag,则补充实验中的试剂A、B分别为
①Zn和CuSO4
②Fe和CuSO4
③Fe和AgNO3
④Zn和AgNO3
(3)小组同学将丙试管中的物质过滤后,向滤液中加入甲中剩余的镁,析出固体质量的变化随反应时间的关系如戊图所示。
①对析出固体的成分提出以下四种猜想:
A Mg、Cu、Ag
B Mg、Cu
C Cu、Ag
D Ag
这四种猜想中明显不合理的是
②写出b点对应溶液中所含的金属离子是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】金属锌与稀硫酸反应生成硫酸锌和氢气,化学课外小组的同学对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与稀硫酸的浓度有关;b.可能与锌的形状有关。
【设计并实验】小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
(1)锌与稀硫酸反应的化学方程式为 _____ 。
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是_____ 。
(3)利用如图装置进行实验时,为了较准确的测量氢气的体积,在读取量气管中液面读数的过程中,应注意_____ (填字母编号)。
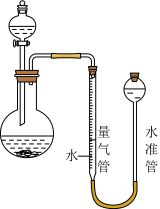
A.读数时视线与凹液面最低处相平。
B.保持水准管静止,待水准管中液面不再上升时再读数。
C.读数前应上下移动水准管,待两管液面相平再读数。
通过上述实验,你得出的结论是硫酸的质量分数越大,反应速率越快。锌与硫酸的接触面积越大,反应速率越快
(4)发生装置中留有氢气,是否会影响实验最终结果_____ (填“是”或“否”)。
(5)下表是小组同学第①组实验的详细数据。
解释第二分钟以后变化的原因 _____ 。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与稀硫酸的浓度有关;b.可能与锌的形状有关。
【设计并实验】小组同学用不同质量分数的硫酸和不同形状的锌进行如下实验。
| 实验编号 | 稀硫酸的浓度(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是
(3)利用如图装置进行实验时,为了较准确的测量氢气的体积,在读取量气管中液面读数的过程中,应注意

A.读数时视线与凹液面最低处相平。
B.保持水准管静止,待水准管中液面不再上升时再读数。
C.读数前应上下移动水准管,待两管液面相平再读数。
通过上述实验,你得出的结论是硫酸的质量分数越大,反应速率越快。锌与硫酸的接触面积越大,反应速率越快
(4)发生装置中留有氢气,是否会影响实验最终结果
(5)下表是小组同学第①组实验的详细数据。
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第4分钟 | 第3分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 9.6mL | 11.9mL | 7.6mL | 6.0mL |
您最近一年使用:0次
【推荐3】M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动。
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【实验1】
(1)取粗细相同的M丝、铜丝、铝丝分别放入盛有等体积、等浓度稀盐酸的3支试管中,进行如下表所示的实验。
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表而致密的氧化膜会先与盐酸反应。
【反思评价】
(2)做金属性质实验时需将金属进行打磨,打磨的目的是___________ 。
【实验2】为进一步确认M、铝、铜这三种金属的活动性顺序,取粗细相同、打磨干净的M丝、铝丝及相关溶液,进行下图所示实验,得出金属活动性顺序:Al>M>Cu。
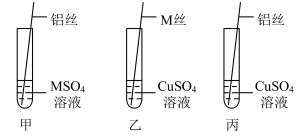
(3)乙中观察到的现象是___________ 。
(4)丙中发生反应的化学方程式为___________ 。
(5)同学们经讨论后认为实验2可以优化,去掉_______ (填编号)实验,也能得出正确的结论。
【拓展迁移】
(6)为验证锌、铜、银三种金属的活动性顺序,设计了下列四种方案,其中不合理的是_______ (填字母)。
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【实验1】
(1)取粗细相同的M丝、铜丝、铝丝分别放入盛有等体积、等浓度稀盐酸的3支试管中,进行如下表所示的实验。
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 根据现象得出金属活动性顺序 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu,M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 |
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表而致密的氧化膜会先与盐酸反应。
【反思评价】
(2)做金属性质实验时需将金属进行打磨,打磨的目的是
【实验2】为进一步确认M、铝、铜这三种金属的活动性顺序,取粗细相同、打磨干净的M丝、铝丝及相关溶液,进行下图所示实验,得出金属活动性顺序:Al>M>Cu。

(3)乙中观察到的现象是
(4)丙中发生反应的化学方程式为
(5)同学们经讨论后认为实验2可以优化,去掉
【拓展迁移】
(6)为验证锌、铜、银三种金属的活动性顺序,设计了下列四种方案,其中不合理的是
| A.锌、CuSO4溶液、银 | B.ZnSO4溶液、铜、银 |
| C.ZnSO4溶液、铜、AgNO3溶液 | D.锌、铜、稀盐酸、AgNO3溶液 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】2023年中央一号文件指出要做好全面推进乡村振兴重点工作,赣南脐橙特色农产品是我市乡村振兴建设中的一项支柱产业。在一次课外实践中,某化学社团走进某赣南脐橙果园开展连续性问题探究。
活动一:测定土壤的酸碱性
【实验方案】
(1)①取少量土壤样品于烧杯中,加蒸馏水搅拌后过滤;
②用玻璃棒蘸取少量滤液,滴在pH试纸上,等试纸显色后与标准比色卡对比,读出pH=6,说明该土壤样品显___________ 性(填“酸”、“中”或“碱”)
活动二:探究土壤是否有硫酸铵
(2)经调查,果园每年都获得大丰收,原因是施放了化肥硫酸铵。于是化学社团对果园土壤是否含有硫酸铵产生了兴趣。
【实验结论】土壤中含有硫酸铵。
活动三:探究硫酸铵溶液是否具有导电性

【实验方案】
(3)社团成员向果农取了化肥硫酸铵(杂质不溶于水),放入烧杯中,加适量水溶解。并接入如图所示的电路中,若观察到___________ ,则说明硫酸铵溶液能导电。
【查阅资料】
(4)①金属能导电是因为金属中存在大量可自由移动的电子。
②溶液能导电的原因是因为溶液中存在自由移动的离子。物质电离可用“电离方程式”来表示,如H2SO4的电离方程式为H2SO4=2H++ ,则硫酸铵的电离方程式为
,则硫酸铵的电离方程式为___________ 。
【拓展延伸】实验小组向烧杯中逐滴加入氢氧化钡溶液,根据电流表读数读数绘制如2所示关系。
(5)图中点___________ (填“A”“B”或“C”)表示硫酸铵溶液和氢氧化钡溶液恰好完全反应。
(6)图中C点溶液中存在的离子有___________ 。
活动四:研究化肥的施用方法
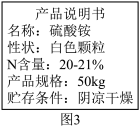
(7)根据果园保存化肥硫酸铵的标签(如图3所示),为保证铵态氮肥的肥 效,下列说法正确的是 (填序号,双选)
活动一:测定土壤的酸碱性
【实验方案】
(1)①取少量土壤样品于烧杯中,加蒸馏水搅拌后过滤;
②用玻璃棒蘸取少量滤液,滴在pH试纸上,等试纸显色后与标准比色卡对比,读出pH=6,说明该土壤样品显
活动二:探究土壤是否有硫酸铵
(2)经调查,果园每年都获得大丰收,原因是施放了化肥硫酸铵。于是化学社团对果园土壤是否含有硫酸铵产生了兴趣。
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:取少量活动一的土壤样品的滤液与试管中,先滴加稀盐酸酸化,无明显现象,再滴加 | 有白色沉淀生成 | 土壤中含有 |
| 步骤2:另取少量土壤样品,加入熟石灰研磨 | 有刺激性气味放出 | 土壤中含有 |
【实验结论】土壤中含有硫酸铵。
活动三:探究硫酸铵溶液是否具有导电性

【实验方案】
(3)社团成员向果农取了化肥硫酸铵(杂质不溶于水),放入烧杯中,加适量水溶解。并接入如图所示的电路中,若观察到
【查阅资料】
(4)①金属能导电是因为金属中存在大量可自由移动的电子。
②溶液能导电的原因是因为溶液中存在自由移动的离子。物质电离可用“电离方程式”来表示,如H2SO4的电离方程式为H2SO4=2H++
 ,则硫酸铵的电离方程式为
,则硫酸铵的电离方程式为【拓展延伸】实验小组向烧杯中逐滴加入氢氧化钡溶液,根据电流表读数读数绘制如2所示关系。
(5)图中点
(6)图中C点溶液中存在的离子有
活动四:研究化肥的施用方法
(7)根据果园保存化肥硫酸铵的标签(如图3所示),为保证铵态氮肥的肥 效,下列说法正确的是 (填序号,双选)

| A.硫酸铵不能高温暴晒 |
| B.铵态氮肥不能与碱性物质混合使用 |
| C.植物叶片发黄,应当施用磷肥促进植物生长 |
| D.土壤酸化常使用氢氧化钠改良酸性土壤 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】管道疏通颗粒是一种新型厨卫管道深层清洁产品,主要是针对厨卫管道内的堵塞进行疏通。某小组对某种管道疏通剂[主要成分为Ca(OH)2、铝粉、缓蚀阻垢剂]的疏通效果进行探究,并探究该种管道疏通颗粒对下水管道的腐蚀情况。
查阅资料:
Ca(OH)2与铝粉混合遇水后发生化学反应,放大量热和气体,可加快疏通毛发等物质。
【实验1】
按表中数据将各固体物质混合均匀后,加入20mL水,观察到有气体产生,并通过测定反应前后温度的变化比较疏通效果(温度升高值越大,疏通效果越好)。
实验数据记录如下:
(1)写出Ca(OH)2在生产、生活中的一种用途是______ 。
(2)要探究铝粉的用量对疏通效果的影响,需对比的实验是①、②和______ (填实验序号)。
(3)对比实验选择的序号是③、⑤、⑥、⑦,其目的是______ 。
(4)由实验1可得知:Ca(OH)2、铝粉、缓蚀阻垢剂的最佳质量比为______ 。
【实验2】
其他条件相同时,改变下水管道材料,测定管道疏通颗粒对各种材料的腐蚀率。
实验结果记录如表格:
(5)管道疏通颗粒腐蚀率最低的材料是______ 。
(6)该管道疏通颗粒不宜对______ 材质的下水管道进行疏通。
(7)进行实验2时,需要控制相同的变量有______ (写2条)。
查阅资料:
Ca(OH)2与铝粉混合遇水后发生化学反应,放大量热和气体,可加快疏通毛发等物质。
【实验1】
按表中数据将各固体物质混合均匀后,加入20mL水,观察到有气体产生,并通过测定反应前后温度的变化比较疏通效果(温度升高值越大,疏通效果越好)。
实验数据记录如下:
| 序号 | Ca(OH)2质量/g | 铝粉质量/g | 缓蚀阻垢剂质量/g | 混合前后温度升高值/℃ |
| ① | 1.3 | 0.55 | 0.18 | 63 |
| ② | 1.3 | 0.75 | 0.18 | 78 |
| ③ | 1.3 | 0.95 | 0.18 | 89 |
| ④ | 1.3 | 1.15 | 0.18 | 83 |
| ⑤ | 1.3 | 0.95 | 0.04 | 86 |
| ⑥ | 1.3 | 0.95 | 0.09 | 87 |
| ⑦ | 1.3 | 0.95 | 0.27 | 87 |
(2)要探究铝粉的用量对疏通效果的影响,需对比的实验是①、②和
(3)对比实验选择的序号是③、⑤、⑥、⑦,其目的是
(4)由实验1可得知:Ca(OH)2、铝粉、缓蚀阻垢剂的最佳质量比为
【实验2】
其他条件相同时,改变下水管道材料,测定管道疏通颗粒对各种材料的腐蚀率。
实验结果记录如表格:
| 材料 | 塑料 | 铜 | 铁 | 钢 | 铝 | 铝合金 |
| 腐蚀率 | 0.1% | 0.4% | 0.5% | 0.3% | 100% | 80% |
(6)该管道疏通颗粒不宜对
(7)进行实验2时,需要控制相同的变量有
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】随着人们生活水平的提高,人们对于食品不但要求营养,更要求健康.市场上出现了一些不添加防腐剂的绿色食品,这种食品中有一个单独包装的保鲜剂,不会危害食品安全.某同学找来一种在空气中放置一段时间的食品保鲜剂,对它进行探究.
【查找资料】
(1)食物腐败是因为微生物在食物上生长.微生物只要得到养分,再加上充足的氧气和水,在适当的条件下就会迅速生长.因此,只要缺少一种条件,就可以防止食物腐败.
(2)常见的具有吸水性的物质有以下几种:
①生石灰 ②铁粉 ③氢氧化钠固体
④硅胶(化学式 ,无色透明粒状固体,无毒无害)
,无色透明粒状固体,无毒无害)
【活动与探究】
(3)初步探究:你认为① ④的物质中,不适合做食品干燥剂的是
④的物质中,不适合做食品干燥剂的是________ ,理由是________ .
(4)实验探究:
【活动反思】
(5)实验2充分反应后试管中所得溶液中的一定含有的溶质是________ .
(6)请根据食物腐败的条件分析,我们除可以使用这些保鲜剂外,还可以采用的保鲜方法是________ .(写出一种即可)
【查找资料】
(1)食物腐败是因为微生物在食物上生长.微生物只要得到养分,再加上充足的氧气和水,在适当的条件下就会迅速生长.因此,只要缺少一种条件,就可以防止食物腐败.
(2)常见的具有吸水性的物质有以下几种:
①生石灰 ②铁粉 ③氢氧化钠固体
④硅胶(化学式
 ,无色透明粒状固体,无毒无害)
,无色透明粒状固体,无毒无害)【活动与探究】
(3)初步探究:你认为①
 ④的物质中,不适合做食品干燥剂的是
④的物质中,不适合做食品干燥剂的是(4)实验探究:
| 实验 | 操作 | 主要现象 | 结论与解释 |
实验 初步判断 初步判断 | 打开这种保鲜剂的包装袋,取少量样品于试管中,进行观察 | 该样品为黑色固体 | 该保鲜剂一定不是 |
实验 对该保鲜剂的有效性进行探究 对该保鲜剂的有效性进行探究 | 向实验 的试管中加入过量的稀盐酸,振荡 的试管中加入过量的稀盐酸,振荡 | 有气泡产生,溶液逐渐变成浅绿色 | 该保鲜剂 |
【活动反思】
(5)实验2充分反应后试管中所得溶液中的一定含有的溶质是
(6)请根据食物腐败的条件分析,我们除可以使用这些保鲜剂外,还可以采用的保鲜方法是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】为了鉴别碳酸钾溶液和氢氧化钾溶液,同学们进行了探究实验:分别取两种溶液于两支试管中,各滴入一定量的氯化钙溶液。观察到一支试管中出现白色浑浊。实验结束后,同学们将废液倒入同一个干净的烧杯中,发现废液变浑浊。同学们对废液进行了过滤,并对滤液的成分进行了探究。
【提出问题】滤液中除水外还含有哪些物质?
【猜想】A.可能含有氢氧化钾、氯化钾和碳酸钾;
B.可能含有氢氧化钾、氯化钾;
C.可能含有氢氧化钾、氯化钾、碳酸钾和氯化钙。
你认为还可能的是什么?__________ (写一种猜想)
【讨论】你认为________ 猜想不合理(填字母),请说明理由______________ 。
【实验设计】设计一个简单的实验,证明你的猜想正确。_______ (写出主要实验步骤和现象)
【反思交流】写出碳酸钾与氯化钙反应的化学方程式_________ 。在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑什么________ ?
【提出问题】滤液中除水外还含有哪些物质?
【猜想】A.可能含有氢氧化钾、氯化钾和碳酸钾;
B.可能含有氢氧化钾、氯化钾;
C.可能含有氢氧化钾、氯化钾、碳酸钾和氯化钙。
你认为还可能的是什么?
【讨论】你认为
【实验设计】设计一个简单的实验,证明你的猜想正确。
【反思交流】写出碳酸钾与氯化钙反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】果蔬洗涤盐既能去除水果和蔬菜表面的农药,又能杀菌、去小虫。小璇同学发现家中有一袋果蔬洗涤盐,其说明书如图所示。她对配料表中的成分很好奇,于是和学习小组的同学们展开了化学探究之旅。
(1)取少量果蔬洗涤盐于烧杯中,加入适量水,搅拌,得到果蔬洗涤盐溶液,用pH试纸测得该溶液的 ,则该果蔬洗涤盐溶液显
,则该果蔬洗涤盐溶液显___________ 性。
任务二:探究果蔬洗涤盐的成分
【查阅资料】
I.果蔬洗涤盐中含有几种常见的钠盐,成分可能是氯化钠、碳酸钠、碳酸氢钠中的一种或几种。
Ⅱ.碳酸氢钠溶液呈碱性,硝酸钙溶液呈中性。
Ⅲ.碳酸氢钠溶液不与硝酸钙溶液反应。
(2)【实验探究】
【反思与评价】
(3)小璇同学认为上述方案不能证明果蔬洗涤盐中含有氯化钠,理由是___________ 。
【拓展延伸】
(4)向碳酸氢钠溶液中加入一定量澄清石灰水,充分反应后,产生白色沉淀,同时还生成纯碱和一种相对分子质量最小的氧化物,请写出该反应的化学方程式___________ 。
(5)在生活中碳酸氢钠不仅可用作果蔬洗涤盐,还可用作___________ (写一种即可)。
【表述与交流】通过实验探究,同学们认识到化学能让我们的生活变得更美好。

(1)取少量果蔬洗涤盐于烧杯中,加入适量水,搅拌,得到果蔬洗涤盐溶液,用pH试纸测得该溶液的
 ,则该果蔬洗涤盐溶液显
,则该果蔬洗涤盐溶液显任务二:探究果蔬洗涤盐的成分
【查阅资料】
I.果蔬洗涤盐中含有几种常见的钠盐,成分可能是氯化钠、碳酸钠、碳酸氢钠中的一种或几种。
Ⅱ.碳酸氢钠溶液呈碱性,硝酸钙溶液呈中性。
Ⅲ.碳酸氢钠溶液不与硝酸钙溶液反应。
(2)【实验探究】
| 实验步骤 | 实验现象 | 分析与结论 |
| ①取少量果蔬洗涤盐溶液于试管中,加入过量硝酸钙溶液,过滤 | 果蔬洗涤盐中含有碳酸钠 | |
| ②取①中滤液,滴加 | 溶液变为红色 | 果蔬洗涤盐中含有碳酸氢钠 |
| ③取①中滤液,先加入过量稀盐酸,再滴加硝酸银溶液 | 产生白色沉淀 | 果蔬洗涤盐中含有氯化钠 |
【反思与评价】
(3)小璇同学认为上述方案不能证明果蔬洗涤盐中含有氯化钠,理由是
【拓展延伸】
(4)向碳酸氢钠溶液中加入一定量澄清石灰水,充分反应后,产生白色沉淀,同时还生成纯碱和一种相对分子质量最小的氧化物,请写出该反应的化学方程式
(5)在生活中碳酸氢钠不仅可用作果蔬洗涤盐,还可用作
【表述与交流】通过实验探究,同学们认识到化学能让我们的生活变得更美好。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】自热火锅带有一个发热包(主要成分是生石灰),遇到水后在3~5秒钟内即可升温,温度可达150℃以上,蒸汽温度达200℃,最长保温时间可达3小时。自热火锅的发热过程无任何污染,成本低廉,但有一定的安全隐患。某校化学兴趣小组对一包久置的发热包成分进行了探究。
【猜想与假设】
猜想1:发热包成分为CaO和Ca(OH)2;
猜想2:发热包成分为Ca(OH)2和CaCO3;
猜想3:发热包成分为CaCO3;
猜想4:……
【进行实验】
操作2中发生的其中一个反应的化学方程式为____ 。
【继续探究】将实验后的废液倒入洁净的废液缸中,观察到溶液呈无色,该烧杯中的液体能否直接倒入下水道?同学们对其中的溶质成分继续进行了如下探究。
【猜想与假设】
猜想1:废液的溶质是CaCl2;
猜想2:废液的溶质是CaCl2、HCl;
猜想3:废液的溶质是CaCl2、Ca(OH)2。
你认为上述哪个猜想不合理?理由是____ 。为进一步确定该溶液的成分,小组成员继续设并完成了如下实验:
【设计实验】
【表达与交流】应向废液中加入适量____ 后再排放。
【反思与评价】如果废液不经过处理就排放,会造成的影响是____ 。
【猜想与假设】
猜想1:发热包成分为CaO和Ca(OH)2;
猜想2:发热包成分为Ca(OH)2和CaCO3;
猜想3:发热包成分为CaCO3;
猜想4:……
【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量样品于试管中,加适量水,振荡,手触摸试管外壁后,滴加几滴酚酞溶液 | 猜想2正确 | |
| 2.另取少量样品于另一试管中,滴加足量的稀盐酸 |
【继续探究】将实验后的废液倒入洁净的废液缸中,观察到溶液呈无色,该烧杯中的液体能否直接倒入下水道?同学们对其中的溶质成分继续进行了如下探究。
【猜想与假设】
猜想1:废液的溶质是CaCl2;
猜想2:废液的溶质是CaCl2、HCl;
猜想3:废液的溶质是CaCl2、Ca(OH)2。
你认为上述哪个猜想不合理?理由是
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量废液于试管中,向其中加入 | 猜想2正确 |
【反思与评价】如果废液不经过处理就排放,会造成的影响是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】实验室有一瓶标签破损的试剂(如图所示),已知它是无色液体,是初中化学常用的试剂。

对此,同学们很感兴趣,决定对其成分进行探究。
【提出问题】这瓶试剂溶质是什么?
【交流研讨】
根据受损标签的情况判断,这瓶试剂不可能是______ (“酸”或“碱”或“盐”)的溶液。
【查阅资料】
①初中化学常见的含钠化合物有 NaCl、NaOH、Na2CO3、NaHCO3、Na2SO4、NaNO3。
②Na2CO3、NaHCO3溶液都呈碱性;NaCl、Na2SO4、NaNO3溶液呈中性。
③室温下(20℃)时,6种物质的溶解度的数据如下:
【得出结论】
小华根据试剂瓶上标注和上表溶解度数据判断,这瓶试剂不可能是______ 溶液。
小亮用洁净的玻璃棒蘸取该溶液,滴到pH试纸上,测得pH>7,他判断该溶液不可能是______ 溶液。
【设计实验】小强为了确定该溶液的成分,进行了如下实验。

对此,同学们很感兴趣,决定对其成分进行探究。
【提出问题】这瓶试剂溶质是什么?
【交流研讨】
根据受损标签的情况判断,这瓶试剂不可能是
【查阅资料】
①初中化学常见的含钠化合物有 NaCl、NaOH、Na2CO3、NaHCO3、Na2SO4、NaNO3。
②Na2CO3、NaHCO3溶液都呈碱性;NaCl、Na2SO4、NaNO3溶液呈中性。
③室温下(20℃)时,6种物质的溶解度的数据如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 | Na2SO4 | NaNO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 | 19.5 | 87 |
小华根据试剂瓶上标注和上表溶解度数据判断,这瓶试剂不可能是
小亮用洁净的玻璃棒蘸取该溶液,滴到pH试纸上,测得pH>7,他判断该溶液不可能是
【设计实验】小强为了确定该溶液的成分,进行了如下实验。
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样品于试管中,滴加 | 立刻产生大量气泡 | 化学方程式是 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某校“非常化学”实验小组的同学在研究酸的化学性质时,做了如图所示5个实验。
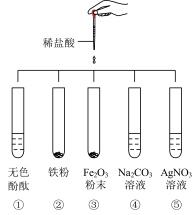
(1)实验后,试管①中溶液呈_______ 色。
(2)实验中,试管③中反应的化学方程式为_______ 。
(3)试管④中有大量气泡产生,该反应属于基本反应类型中的_______ 反应。
(4)试管⑤中发生的化学反应方程式为_______ 。
同学们对反应结束后试管⑤中溶液的成分产生好奇,进行进一步探究。
【提出问题】反应结束后,试管⑤中的溶液里含有哪些溶质?
(5)【猜想与假设】
猜想一:HNO3
猜想二:_______ 。
猜想三:_______ 。
(6)【设计并进行实验】
(7)【反思评价】
经小组同学探究猜想一成立,为了防止废液中的硝酸腐蚀水管,可向其中加入过量的某物质使其变为中性,则该物质可能是_______ (填字母序号)。
A 纯碱 B 碳酸钙 C 生石灰 D 熟石灰

(1)实验后,试管①中溶液呈
(2)实验中,试管③中反应的化学方程式为
(3)试管④中有大量气泡产生,该反应属于基本反应类型中的
(4)试管⑤中发生的化学反应方程式为
同学们对反应结束后试管⑤中溶液的成分产生好奇,进行进一步探究。
【提出问题】反应结束后,试管⑤中的溶液里含有哪些溶质?
(5)【猜想与假设】
猜想一:HNO3
猜想二:
猜想三:
(6)【设计并进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| ①取反应后上清液少许,滴加稀盐酸 | 猜想一成立 | |
| ②取反应后上清液少许,滴加 |
经小组同学探究猜想一成立,为了防止废液中的硝酸腐蚀水管,可向其中加入过量的某物质使其变为中性,则该物质可能是
A 纯碱 B 碳酸钙 C 生石灰 D 熟石灰
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】钙元素是一种重要的金属元素,它形成的物质种类很多。
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂。某实验探究小组的同学通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式_____ 。
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是_____ (填“吸热”或“放热”)。
(3)实验探究小组将Na₂CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和_____
猜想四:NaOH、Na₂CO3和Ca(OH)2经过讨论,大家认为猜想四不合理,原因是_____ 。
(4)【实验过程】
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂。某实验探究小组的同学通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是
(3)实验探究小组将Na₂CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想一:NaOH
猜想二:NaOH和Ca(OH)2
猜想三:NaOH和
猜想四:NaOH、Na₂CO3和Ca(OH)2经过讨论,大家认为猜想四不合理,原因是
(4)【实验过程】
| 实验步骤 | 现象 | 结论 |
| 实验Ⅰ:取滤液,向其中滴入适量Na₂CO3溶液 | 猜想二不成立 | |
| 实验Ⅱ:另取滤液,向其中加入足量 | 产生气泡 | 猜想 |
您最近一年使用:0次



