实验室用含杂质的锌(也称粗锌)与盐酸反应制取氢气,取8.0g含杂质的锌粒于烧杯中(所含杂质不溶于水,也不与酸反应),向其中加入73.0g稀盐酸,恰好完全反应后烧杯内剩余物质的质量为80.8g。计算反应后所得不饱和溶液的溶质质量分数。(结果精确至0.1%)
2024·湖南怀化·二模 查看更多[1]
更新时间:2024-04-22 09:10:46
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】为确定失去标签的盐酸中溶质的质量分数,某化学兴趣小组进行了实验探究,化学小组同学取50 g该盐酸,向其中加入50 g硝酸银溶液,二者恰好完全反应,过滤后称得滤液的质量为85.65 g。(温馨提示:HCl+AgNO3=AgCl↓+HNO3)请计算:
(1)反应后生成沉淀的质量是______g。
(2)该盐酸中溶质的质量分数。(计算结果精确到0.1%)
(1)反应后生成沉淀的质量是______g。
(2)该盐酸中溶质的质量分数。(计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
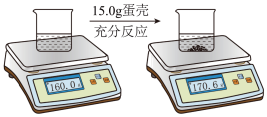
【推荐2】某兴趣小组拟选用鸡蛋壳作为实验室制取二氧化碳的原料。为了测定鸡蛋壳中CaCO3的质量分数是否满足实验要求,该小组同学进行如下实验,将鸡蛋壳洗净、捣碎后准确称量15.0g,全部投入足量稀盐酸中,电子秤的示数变化情况如图:
(1)捣碎鸡蛋壳的目的是_______ 。
(2)根据图示判断:蛋壳中的CaCO3与盐酸反应生成二氧化碳的质量是_______ g,根据此数据计算CaCO3的质量分数为_______ (结果保留到0.1%);
(3)对此计算结果,兴趣小组认为满足实验要求。但有同学认为该结果有可能偏低,理由是_______ 。
(1)捣碎鸡蛋壳的目的是
(2)根据图示判断:蛋壳中的CaCO3与盐酸反应生成二氧化碳的质量是
(3)对此计算结果,兴趣小组认为满足实验要求。但有同学认为该结果有可能偏低,理由是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】化学兴趣小组的同学为确定某铁合金样品是生铁还是钢(假设铁合金样品中只含有铁、碳两种元素),他们取22.6g铁合金样品盛放到锥形瓶中,将100g稀硫酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
请回答下列问题:
(1)表格中的m的值为_______ 。
(2)计算所用稀硫酸溶液的溶质质量分数是多少。
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀硫酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 瓶中物质总质量(g) | 42.4 | m | 82.0 | 101.8 | 121.8 |
(1)表格中的m的值为
(2)计算所用稀硫酸溶液的溶质质量分数是多少。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】控制煤炭硫含量的标准对于保障环境和人类健康具有重要意义。高硫煤燃烧时会产生大量的二氧化硫等有害气体,对环境造成污染,同时也会对人体健康造成危害。因此,发展低硫煤等清洁能源已成为全球的趋势。我国煤的含硫标准:
①低硫煤:含硫量小于1%的是低硫煤。
②中硫煤:含硫量1%-3%的为中硫煤。
③高硫煤:含硫量大于3%的为高硫煤。
若10g样品煤在充足氧气中完全燃烧生成0.4gSO2。试通过计算判断该样品属于哪种煤?
①低硫煤:含硫量小于1%的是低硫煤。
②中硫煤:含硫量1%-3%的为中硫煤。
③高硫煤:含硫量大于3%的为高硫煤。
若10g样品煤在充足氧气中完全燃烧生成0.4gSO2。试通过计算判断该样品属于哪种煤?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定黄铜合金(Cu-Zn)中铜的质量分数,某同学将10g该合金放入到盛有40g足量稀硫酸的烧杯中,充分反应后,测得烧杯中剩余物的质量为49.9g。请列示计算:
(1)生成氢气的质量;
(2)原合金中铜的质量分数(Zn+H2SO4=ZnSO4+H2↑ Zn-65 )
(1)生成氢气的质量;
(2)原合金中铜的质量分数(Zn+H2SO4=ZnSO4+H2↑ Zn-65 )
您最近一年使用:0次
计算题
|
适中
(0.65)
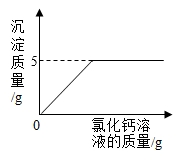
【推荐3】某碳酸钠样品中含少量氯化钠,化学兴趣小组的同学欲通过实验来测定样品中碳酸钠的质量分数。他们取6g该样品,配制成溶液,再向其中加入足量的氯化钙溶液(呈中性),测得加入氯化钙溶液的质量与产生沉淀的质量关系如图所示。请回答下列问题:
(1)该样品中碳酸钠的质量分数是多少?(写出计算步骤,计算结果精确到0.1%)
(2)如果反应开始前,向烧杯中滴加几滴无色酚酞试液,在整个测定过程中可观察到的现象是: 。
(1)该样品中碳酸钠的质量分数是多少?(写出计算步骤,计算结果精确到0.1%)
(2)如果反应开始前,向烧杯中滴加几滴无色酚酞试液,在整个测定过程中可观察到的现象是: 。

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某同学欲测定实验室中某黄铜样品(铜锌合金)中铜的质量分数(不考虑其他杂质)。现称量 20g粉末状黄铜样品放入烧杯中,将 60g稀盐酸分成三等份依次加到其中,每次充分反应后,测定生成气体的质量。生成的气体和稀盐酸质量关系如下图所示。

请计算∶
(1)a 的数值______
(2)此黄铜样品中铜的质量分数为______(结果精确到 0.1%)
(3)所用稀盐酸的溶质质量分数为多少?(结果精确到 0.1%,写出计算过程)

请计算∶
(1)a 的数值______
(2)此黄铜样品中铜的质量分数为______(结果精确到 0.1%)
(3)所用稀盐酸的溶质质量分数为多少?(结果精确到 0.1%,写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学老师带领同学们参观工厂的时候,工人师傅介绍了一种锌的样品(样品中的其它物质既不与酸反应也不溶于水),同学们想测定锌样品中锌的质量,进行了如图所示实验。请根据图中提供的数据进行计算:_____ g。
(2)计算所用稀硫酸中溶质的质量分数(计算结果精确到0.1%).

(2)计算所用稀硫酸中溶质的质量分数(计算结果精确到0.1%).
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室常用溶质质量分数为10%的过氧化氢溶液制取氧气。

(1)在配制过程中,他们发现试剂瓶内壁附着不少气泡,由此推断该瓶过氧化氢溶液的溶质质量分数小于30%,依据是_________ 。
(2)为测定该瓶溶液的溶质质量分数,他们取35g该溶液放入锥形瓶中并加入一定量的二氧化锰。不同时间电子秤的读数如下表所示(不考虑H2O逸出):
请回答:
①反应生成氧气的总质量为_________ g。
②该瓶过氧化氢溶液的溶质质量分数是多少________ ?(写出计算过程,结果保留到0.1%)

(1)在配制过程中,他们发现试剂瓶内壁附着不少气泡,由此推断该瓶过氧化氢溶液的溶质质量分数小于30%,依据是
(2)为测定该瓶溶液的溶质质量分数,他们取35g该溶液放入锥形瓶中并加入一定量的二氧化锰。不同时间电子秤的读数如下表所示(不考虑H2O逸出):
| 反应时间min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 锥形瓶+瓶内物质的总质量/g | 340.00 | 338.78 | 335.64 | 335.20 | 335.20 | 335.20 | 335.20 |
①反应生成氧气的总质量为
②该瓶过氧化氢溶液的溶质质量分数是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知某使用过的电解液中只有硫酸和硫酸铜两种溶质,为测定硫酸铜的质量分数,兴趣小组同学取50g该电解液样品,向其中逐滴加入一定溶质质量分数的氢氧化钠溶液,测得生成沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。回答下列问题:

(1)向电解液中滴加氢氧化钠溶液使用的仪器是________ 。
(2)充分反应生成氢氧化铜的质量为________ g。
(3)图中a点所示溶液中含有的阳离子符号为__________ 。
(4)计算该电解液中硫酸铜的质量分数。(写出计算过程)

(1)向电解液中滴加氢氧化钠溶液使用的仪器是
(2)充分反应生成氢氧化铜的质量为
(3)图中a点所示溶液中含有的阳离子符号为
(4)计算该电解液中硫酸铜的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】一凡同学对生铁的组成进行研究,称取生铁样品 40g,把 500g 稀硫酸分 5 次加入样品中, 测得实验数据见下表:(杂质不溶于水,也不和稀硫酸反应)
(1)第 3 次剩余固体的质量 M=_____ 第 5 次剩余固体的质量 N=_____
(2)该生铁样品中铁的质量分数为_____ 。
(3)计算第 3 次反应结束后所得溶液的溶质质量分数。_____ (写出计算过程,保留一位小数)
| 实验序号 | 加入稀硫酸的质量/g | 剩余固体的质量/g |
| 第 1 次 | 100 | 28.8 |
| 第 2 次 | 100 | 17.6 |
| 第 3 次 | 100 | M |
| 第 4 次 | 100 | 1.2 |
| 第 5 次 | 100 | N |
(1)第 3 次剩余固体的质量 M=
(2)该生铁样品中铁的质量分数为
(3)计算第 3 次反应结束后所得溶液的溶质质量分数。
您最近一年使用:0次



