我们处在一个色彩斑斓的物质世界中。化学社团针对物质开展“颜之有物”的探究。
Ⅰ.物质有自己独特颜色
(1)下列物质与水能形成有色溶液的是________。
(2)氯化铁溶液呈黄色。为探究是哪种粒子使溶液呈黄色,同学们设计了如图所示的对比实验,可选择用作对比的试剂是________ 溶液。
(3)向某溶液中滴加紫色石蕊试剂,溶液变红色,说明该溶液pH________ 7(填“>”、“=”或“<”)。
Ⅲ.颜色变化可作为化学反应发生的一种证据
(4)有些化学反应中伴随着颜色的变化。如实验室模拟炼铁,高温下CO还原氧化铁,观察到固体的颜色变化是________ 。
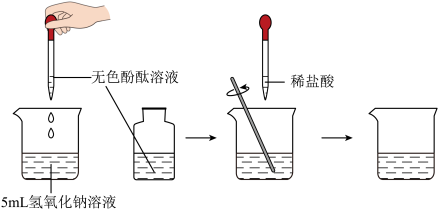
(5)自然界中无明显现象的反应远多于有明显现象的反应,比如稀盐酸和氢氧化钠反应。为验证该反应的发生,设计了如图所示的实验:________ (现象),即可证明两者发生了化学反应。请写出该反应的化学方程式________ 。
(6)颜料可从植物中获取。唐代流行服饰石榴裙因其颜色类似石榴花的红色而得名。古法染色工艺记载:“取石榴之花,入臼细杵之,得厚汁,以之染布,不可加热,可为石榴裙也”。请写出在此染布过程中需要注意的事项________________ (一条即可)。
(7)为测定某生锈铁钉中未生锈的铁的质量,取50g该铁钉放入溶质质量分数为7.3%的稀盐酸中,当表面的铁锈完全除去时恰好消耗300g稀盐酸溶液。请计算该铁钉中未生锈的铁的质量。
Ⅰ.物质有自己独特颜色
(1)下列物质与水能形成有色溶液的是________。
| A.酒精 | B.硫酸铜 | C.牛奶 | D.碳酸钙 |
(2)氯化铁溶液呈黄色。为探究是哪种粒子使溶液呈黄色,同学们设计了如图所示的对比实验,可选择用作对比的试剂是

(3)向某溶液中滴加紫色石蕊试剂,溶液变红色,说明该溶液pH
Ⅲ.颜色变化可作为化学反应发生的一种证据
(4)有些化学反应中伴随着颜色的变化。如实验室模拟炼铁,高温下CO还原氧化铁,观察到固体的颜色变化是
(5)自然界中无明显现象的反应远多于有明显现象的反应,比如稀盐酸和氢氧化钠反应。为验证该反应的发生,设计了如图所示的实验:
(6)颜料可从植物中获取。唐代流行服饰石榴裙因其颜色类似石榴花的红色而得名。古法染色工艺记载:“取石榴之花,入臼细杵之,得厚汁,以之染布,不可加热,可为石榴裙也”。请写出在此染布过程中需要注意的事项
(7)为测定某生锈铁钉中未生锈的铁的质量,取50g该铁钉放入溶质质量分数为7.3%的稀盐酸中,当表面的铁锈完全除去时恰好消耗300g稀盐酸溶液。请计算该铁钉中未生锈的铁的质量。
更新时间:2024-04-22 15:56:04
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
【推荐1】如图所示,A一G是初中化学中常见的几种物质,A为一种钡盐,C为最轻的气体,只有D、F为黑色固体。部分反应物及反应条件已略去,“一”表示两种物质可以相互反应,“→”表示一种物质可以转化为另一种物质,A与B能相互转化,箭头指向生成物。

(1)写出下列物质的化学式:B__________ ;G__________ 。
(2)写出足量B与D的现象:__________ 。
(3)E与F反应的方程式:____________ 。

(1)写出下列物质的化学式:B
(2)写出足量B与D的现象:
(3)E与F反应的方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铁及其化合物在生产生活中应用广泛。
Ⅰ.铁的性质和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的微量元素,此反应的化学方程式为_____ ,该反应的基本反应类型为_____ 。
(2)为防止铁生锈,可对铁制品进行“发蓝"处理,使其表面生成致密氧化物(其中 、O元素质量比为
、O元素质量比为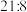 )保护膜,该氧化物的化学式为
)保护膜,该氧化物的化学式为_____ 。
Ⅱ.废铁的再利用
硫酸铁在农业可用作肥料,是花木、果树制造叶绿素的催化剂。用废铁屑(主要成分为 ,含少量
,含少量 和
和 )制备硫酸铁的主要流程如下:
)制备硫酸铁的主要流程如下:
已知: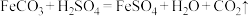

(3)酸溶得到的混合溶液中含_____ 种溶质。
(4)“转化1”温度不宜过高的原因是_____ 。
Ⅲ.铁的冶炼
我国劳动人民在春秋战国时期就会冶铁炼钢,实验室模拟炼铁实验装置如图所示。
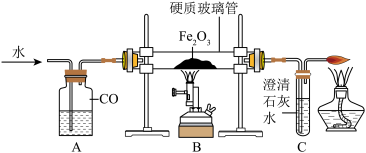
(5)实验时,应先注水片刻后再加热的目的是_____ 。
(6)实验过程中,硬质玻璃管中的现象为_____ 。发生反应的化学方程式为_____ 。
Ⅰ.铁的性质和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的微量元素,此反应的化学方程式为
(2)为防止铁生锈,可对铁制品进行“发蓝"处理,使其表面生成致密氧化物(其中
 、O元素质量比为
、O元素质量比为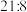 )保护膜,该氧化物的化学式为
)保护膜,该氧化物的化学式为Ⅱ.废铁的再利用
硫酸铁在农业可用作肥料,是花木、果树制造叶绿素的催化剂。用废铁屑(主要成分为
 ,含少量
,含少量 和
和 )制备硫酸铁的主要流程如下:
)制备硫酸铁的主要流程如下:已知:
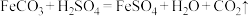

(3)酸溶得到的混合溶液中含
(4)“转化1”温度不宜过高的原因是
Ⅲ.铁的冶炼
我国劳动人民在春秋战国时期就会冶铁炼钢,实验室模拟炼铁实验装置如图所示。

(5)实验时,应先注水片刻后再加热的目的是
(6)实验过程中,硬质玻璃管中的现象为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学源于生活,请你根据学过的化学知识回答下列问题:
(1)“可燃冰”为甲烷的水合物,其化学式为CH4·8H2O,主要是由甲烷与水在高压低温条件下形成的类冰块的着火点类冰状物质,可燃烧。可燃冰中碳、氢、氧元素的质量比为________ ,甲烷中碳元素的质量分数为________ ,甲烷在空气中完全燃烧的化学方程式为________ 。
(2)每年全世界钢铁的产量很高,钢铁是一种________ (填物质类别),其硬度比纯铁________ ,工业上常用一氧化碳在高温条件下还原赤铁矿(主要成分是Fe2O3)的方法炼铁,该反应的化学方程式为______ 。根据金属活动性顺序表,锌比铁的活动性强,可用一个化学反应证明,请写出该反应的化学方程式________ 。铝在空气中有较好的抗腐蚀性能,原因是________ (用化学方程式表示)。
(1)“可燃冰”为甲烷的水合物,其化学式为CH4·8H2O,主要是由甲烷与水在高压低温条件下形成的类冰块的着火点类冰状物质,可燃烧。可燃冰中碳、氢、氧元素的质量比为
(2)每年全世界钢铁的产量很高,钢铁是一种
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】为测得某大理石样品中碳酸钙的质量分数,兴趣小组同学进行了如下实验,过程如图所示:(杂质不溶于水也不与盐酸反应)

求:①反应中生成二氧化碳的质量为_____ ;
②该大理石样品中碳酸钙的质量分数。____

求:①反应中生成二氧化碳的质量为
②该大理石样品中碳酸钙的质量分数。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】碱是初中化学学习的一类重要物质,氢氧化钠和氢氧化钙是两种常见的碱。
Ⅰ、碱的结构
(1)氢氧化钠和氢氧化钙具有相似的化学性质,是因为它们在水溶液中都能解离出______(填字母)。
Ⅱ、碱的性质______ (填“氢氧化钠溶液”或“稀盐酸”)滴加到另一种溶液中;a点溶液中所含的溶质为______ 。
(3)如图2分别将二氧化碳气体通入氢氧化钙溶液和氢氧化钠溶液中。
①观察到试管 A 中溶液变浑浊,证明二氧化碳能与氢氧化钙溶液反应,写出反应的化学方程式;______ 。
②试管B 中未观察到明显现象,甲同学提出向反应后的溶液中滴加无色酚酞溶液,观察到溶液由无色变为______ 色,则证明二氧化碳能与氢氧化钠溶液反应,乙同学认为上述实验方案不合理。请设计实验方案证明两者能发生反应______ 。(简述实验操作和现象)
Ⅲ、碱的用途
(4)请简述氢氧化钙在生产或生活中的一种用途______ 。
(5)某工厂化验室用稀硫酸处理含氢氧化钠的废水。现取废水样品100g倒入烧杯中,然后逐滴加入9.8%的稀硫酸,恰好完全反应时,共消耗稀硫酸的质量为20g,求废水中氢氧化钠的质量分数。
Ⅰ、碱的结构
(1)氢氧化钠和氢氧化钙具有相似的化学性质,是因为它们在水溶液中都能解离出______(填字母)。
| A.氢原子 | B.氢离子 | C.氢氧根离子 | D.水分子 |
Ⅱ、碱的性质

(3)如图2分别将二氧化碳气体通入氢氧化钙溶液和氢氧化钠溶液中。
①观察到试管 A 中溶液变浑浊,证明二氧化碳能与氢氧化钙溶液反应,写出反应的化学方程式;
②试管B 中未观察到明显现象,甲同学提出向反应后的溶液中滴加无色酚酞溶液,观察到溶液由无色变为
Ⅲ、碱的用途
(4)请简述氢氧化钙在生产或生活中的一种用途
(5)某工厂化验室用稀硫酸处理含氢氧化钠的废水。现取废水样品100g倒入烧杯中,然后逐滴加入9.8%的稀硫酸,恰好完全反应时,共消耗稀硫酸的质量为20g,求废水中氢氧化钠的质量分数。
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐3】取22.2g石灰石样品,放入盛有126g稀盐酸的烧杯中,石灰石中的碳酸钙与盐酸恰好完全反应(杂质不反应,也不溶解),烧杯内物质质量变为139.4g 。求
(1)生成二氧化碳的质量。
(2)石灰石中碳酸钙的质量。
(3)反应后所得溶液中溶质的质量分数。
(1)生成二氧化碳的质量。
(2)石灰石中碳酸钙的质量。
(3)反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐1】用如图所示实验验证CO2的性质。

(1)向瓶中通入CO2,当观察到短蜡烛熄灭后,关闭K,继续通入CO2,观察到的现象是什么?该实验说明CO2的性质有哪些?
(2)观察到纸花变红,由此不能得出“CO2能与水发生化学反应”的结论,理由是什么?

(1)向瓶中通入CO2,当观察到短蜡烛熄灭后,关闭K,继续通入CO2,观察到的现象是什么?该实验说明CO2的性质有哪些?
(2)观察到纸花变红,由此不能得出“CO2能与水发生化学反应”的结论,理由是什么?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】填空:
(1)实验室中有A、B两种溶液,经测定,A溶液pH=4.5,B溶液pH=10.2。则A溶液呈______ 性,能使紫色石蕊溶液变______ 色;B溶液呈______ 性,能使无色酚酞溶液变______ 色。
(2)测定pH最简单的方法是使用______ 。测定时,用______ 蘸取待测溶液,滴在______ 上,然后再与______ 对照,得出该溶液的pH。
(3)下列方法可以解决生活中的一些问题:
①服用含氢氧化铝〔Al(OH)3〕的药物可以治疗胃酸过多病症,反应的化学方程式为______ 。
②热水瓶用久后,瓶胆内壁常附着一层水垢【主要成分是CaCO3和Mg(OH)2),可以用______ 来洗涤。写出其与Mg(OH)2反应的化学方程式:______ 。
③实验室中含有盐酸的废水直接倒入下水道会造成铸铁管道腐蚀,所以,需将废液处理后再排放。你的处理方法是______ 。
(1)实验室中有A、B两种溶液,经测定,A溶液pH=4.5,B溶液pH=10.2。则A溶液呈
(2)测定pH最简单的方法是使用
(3)下列方法可以解决生活中的一些问题:
①服用含氢氧化铝〔Al(OH)3〕的药物可以治疗胃酸过多病症,反应的化学方程式为
②热水瓶用久后,瓶胆内壁常附着一层水垢【主要成分是CaCO3和Mg(OH)2),可以用
③实验室中含有盐酸的废水直接倒入下水道会造成铸铁管道腐蚀,所以,需将废液处理后再排放。你的处理方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】氯化氢(HCl)是极易溶于水的无色气体,其水溶液叫盐酸。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是________ 。
(2)在盐酸中加入过量的铁粉充分反应。如图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):


_____ 
_____ 
_____
(3)取2支试管,分别开展如下实验:
实验Ⅰ:在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水。
实验Ⅱ:在充满CO2气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水。
实验Ⅰ和实验Ⅱ滴入水后的现象为___________ 。
(4)向盛有Na2CO3粉末的试管中通入HCl气体,无明显现象;停止通气,再加入少量水,现象是____ ,写出该反应的化学方程式:______________ 。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是
(2)在盐酸中加入过量的铁粉充分反应。如图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):




(3)取2支试管,分别开展如下实验:
实验Ⅰ:在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水。
实验Ⅱ:在充满CO2气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水。
实验Ⅰ和实验Ⅱ滴入水后的现象为
(4)向盛有Na2CO3粉末的试管中通入HCl气体,无明显现象;停止通气,再加入少量水,现象是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】以NaOH溶液和盐酸的反应为例,且已加入酚酞溶液,pH变化曲线如图:

(1)B点所对应溶液中的溶质为(填名称,下同)_____ ;
(2)C点所对应溶液中的溶质为_____ 。

(1)B点所对应溶液中的溶质为(填名称,下同)
(2)C点所对应溶液中的溶质为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】酸、盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)叠氮酸(HN3)常温下是一种无色液体,其水溶液具有酸性,可与NaOH溶液反应得到叠氮化钠(NaN3)。某些汽车安全气囊中装有叠氮化钠。
①叠氮酸在水溶液中解离出H+和_____ (填化学符号)。
②叠氮酸与NaOH溶液的反应属于_____ (填基本反应类型)。
③叠氮化钠受热分解时产生两种单质,该反应的化学方程式为_____ 。
(2)盐酸是一种重要的酸,用于制药、除锈等。

①盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式_____ 。
②利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图。当滴入溶液为V2mL时,形成溶液中所含溶质化学式为_____ ,所得溶液能使紫色石蕊溶液变成_____ 色。
(3)家庭加工馒头、面包等食品时,常在面粉中加入膨松剂(如图),蒸制或烘焙食品时膨松剂会产生大量气体,使面团疏松、多孔,制作的食品松软或酥脆,易于消化吸收。

①信息中提供的膨松剂是_____ (填化学式);
②信息中的膨松剂能使蒸制或烘焙的食品疏松多孔,原理是_____ (用化学方程式解释)。
(1)叠氮酸(HN3)常温下是一种无色液体,其水溶液具有酸性,可与NaOH溶液反应得到叠氮化钠(NaN3)。某些汽车安全气囊中装有叠氮化钠。
①叠氮酸在水溶液中解离出H+和
②叠氮酸与NaOH溶液的反应属于
③叠氮化钠受热分解时产生两种单质,该反应的化学方程式为
(2)盐酸是一种重要的酸,用于制药、除锈等。

①盐酸可用于金属表面除锈,请写出盐酸除铁锈的化学方程式
②利用数字化实验设备,测定盐酸与氢氧化钠溶液反应时溶液pH变化,实验结果如图。当滴入溶液为V2mL时,形成溶液中所含溶质化学式为
(3)家庭加工馒头、面包等食品时,常在面粉中加入膨松剂(如图),蒸制或烘焙食品时膨松剂会产生大量气体,使面团疏松、多孔,制作的食品松软或酥脆,易于消化吸收。

①信息中提供的膨松剂是
②信息中的膨松剂能使蒸制或烘焙的食品疏松多孔,原理是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】在宏观、微观、符号之间建立联系,是化学学科特有的思维方式。

(1)如图是氢氧化钠溶液与盐酸反应时溶液pH变化的示意图。根据图示判断,该实验是将____ (填“氢氧化钠溶液”或“盐酸”)滴加到另一种溶液中。c点的溶质是_______ 。
(2)如果将盐酸滴入氢氧化钠溶液(加入酚酞试液),完全反应时,溶液呈___ 色。它们反应前后的微观示意图如图。

图1是HCl和NaOH在水中解离出离子的示意图,HCl在水中会解离出H+和Cl﹣,可以表示为HCl→H++Cl﹣,NaOH在水中解离可表示为NaOH→Na++Cl﹣。图2是氢氧化钠溶液与盐酸反应的微观示意图,该反应的实质可表示为:H++OH﹣=H2O
(3)BaCl2在水中会解离出的离子是______ (填符号),图3是氯化钡溶液与硫酸钠溶液反应的微观示意图,该)反应的实质可表示为________ ,由此类推,硫酸溶液与碳酸钠溶液反应的实质可表示为______ 。

(1)如图是氢氧化钠溶液与盐酸反应时溶液pH变化的示意图。根据图示判断,该实验是将
(2)如果将盐酸滴入氢氧化钠溶液(加入酚酞试液),完全反应时,溶液呈

图1是HCl和NaOH在水中解离出离子的示意图,HCl在水中会解离出H+和Cl﹣,可以表示为HCl→H++Cl﹣,NaOH在水中解离可表示为NaOH→Na++Cl﹣。图2是氢氧化钠溶液与盐酸反应的微观示意图,该反应的实质可表示为:H++OH﹣=H2O
(3)BaCl2在水中会解离出的离子是
您最近一年使用:0次



