海水淡化是综合利用海洋资源的重要产业。
(1)某工厂淡化海水后得到的淡盐水和浓盐水中盐类物质的含量如表(其他微量盐类忽略不计)。该工厂一套淡化装置每小时产生5000L浓盐水,其中含有NaCl____ kg;国家规定居民生活用水中盐类物质的总含量≤500mg/L,则所得淡盐水中盐类物质的总含量____ (选填“达到”或“未达到”)生活用水的标准。
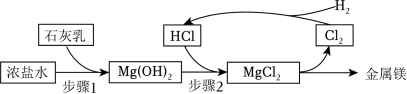
(2)用淡化海水所得的浓盐水可制备金属镁,主要物质间的转化关系如图:____ 。
②图中未涉及的反应类型为____ (填选项)。
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(1)某工厂淡化海水后得到的淡盐水和浓盐水中盐类物质的含量如表(其他微量盐类忽略不计)。该工厂一套淡化装置每小时产生5000L浓盐水,其中含有NaCl
| 水样 | 盐类物质的含量/(g•L-1) | |||
| 氯化钠 | 氯化镁 | 硫酸镁 | 硫酸钙 | |
| 淡盐水 | 0.17 | 0.012 | 4.8×10-4 | 8.5×10-4 |
| 浓盐水 | 45.0 | 3.6 | 3.3 | 0.14 |
②图中未涉及的反应类型为
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
2024九年级下·全国·专题练习 查看更多[1]
(已下线)题型03 工艺流程题-【查漏补缺】2024年中考化学复习冲刺过关(全国通用)
更新时间:2024-05-05 06:55:37
|
相似题推荐
【推荐1】学了酸的化学性质,某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
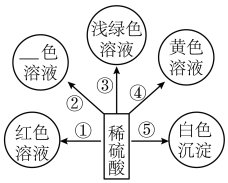
(1)若想实现①,需要加入的试剂是_______ 。
(2)若用Cu(OH)2实现②,会得到_______ 色溶液。
(3)若想实现③,选用的单质是________ 。
(4)若选用氧化铁实现④,此反应的化学方程式为_______ 。
(5)若选用BaCl2溶液实现⑤,此反应的化学方程式为_____ ,基本反应类型为_____ 。

(1)若想实现①,需要加入的试剂是
(2)若用Cu(OH)2实现②,会得到
(3)若想实现③,选用的单质是
(4)若选用氧化铁实现④,此反应的化学方程式为
(5)若选用BaCl2溶液实现⑤,此反应的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
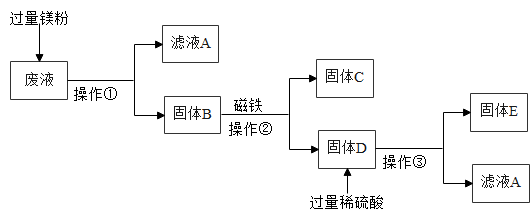
【推荐2】有一包白色粉末,可能含有Ba(OH)2、KNO3、Na2CO3、Na2SO4中的一种或几种,为了确定其成分,进行如下实验:
①取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀.
②过滤,在白色沉淀中加入足量稀盐酸,白色沉淀部分溶解,且有气泡产生.
(1)据此推断,该白色粉末中一定含有_____ ;可能含有_____
(2)写出步骤②中发生反应的化学方程式:_____ ,其基本反应类型是_____ 。
①取一定量的白色粉末加入足量的水,振荡,静置,得白色沉淀.
②过滤,在白色沉淀中加入足量稀盐酸,白色沉淀部分溶解,且有气泡产生.
(1)据此推断,该白色粉末中一定含有
(2)写出步骤②中发生反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】从500 mL溶质质量分数为98%,密度为1.84 g/cm3的浓H2SO4中取出100 mL,这100 mL浓硫酸的溶质质量分数为____ ,溶液质量为____ g,其中含纯硫酸的质量为____ g。若将100 mL98%的浓H2SO4与100 mL水混合,所得溶液的质量为____ g,含纯H2SO4的质量为____ g,溶质的质量分数为____ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室存有一定量的溶质质量分数为5%的氢氧化钠溶液,加热蒸发掉108g水后,所得溶液的溶质质量分数变为20%。求:
(1)原氢氧化钠溶液的质量是______ 克;
(2)原氢氧化钠溶液中含有溶质______ 克。
(1)原氢氧化钠溶液的质量是
(2)原氢氧化钠溶液中含有溶质
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】用工业碳酸钙(含有少量Al2O3、Fe2O3)生产医药CaCl2•2H2O的主要流程如图:
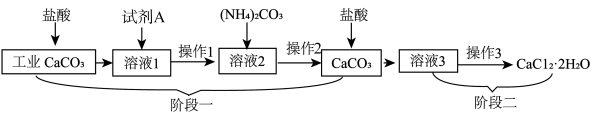
(1)写出工业CaCO3中加入稀盐酸发生反应的化学方程式_____ (任写一个即可);
(2)加入试剂A的目的是除去溶液1中少量AlCl3、FeCl3,试剂A可以选择_____ (选填序号);
a Na2CO3 b Ba(OH)2 c Ca(OH)2
(3)阶段一的目的是_____ 。
(4)阶段二中操作3包括:蒸发浓缩、_____ 、过滤、洗涤等。

(1)写出工业CaCO3中加入稀盐酸发生反应的化学方程式
(2)加入试剂A的目的是除去溶液1中少量AlCl3、FeCl3,试剂A可以选择
a Na2CO3 b Ba(OH)2 c Ca(OH)2
(3)阶段一的目的是
(4)阶段二中操作3包括:蒸发浓缩、
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下表是 20℃时部分物质的溶解度数据。
(1)配制溶液:配制 50g11%氢氧化钠溶液的基本步骤是:计算—称取氢氧化钠固体—量取水—溶解—装瓶贴标签。 用托盘天平称取氢氧化钠固体的质量_________ g。
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向稀氢氧化钠溶液中通入 CO2,先生成 Na2CO3,继续通入 CO2,Na2CO3 会转化为 NaHCO3,已知后者为化合反应,请写出该化合反应的化学方程式:_________ 。 若向 20℃时饱和 Na2CO3 溶液中通入过量的 CO2,可观察到的现象是_________ 。
②结合表格中的有关数据,若以 20℃时,100g 饱和溶液吸收 CO2 的质量最大为依据,则除去 CO 气体中的 CO2 杂质,应选择_________ 溶液(填化学式),欲检验CO2气体的存在,则应选择_________ 溶液(填化学式)。
③将 2.2g CO2 通入 47.8g 一定浓度的 NaOH溶液中充分反应后(反应过程中没有CO2 逸出,水也没有蒸发),溶液中的溶质仅有 Na2CO3和 NaHCO3 两种物质(NaHCO3 在水中电离成 Na+和 HCO3-),则此时溶液中碳元素的质量分数为__________ ,在此反应过程中,你认为钠离子的个数_________ 发生变化?(填写: 有或者没有)
(3)电导率传感器可辅助探究复分解反应的实质。相同条件下,离子浓度越大,电导率越大,溶液导电性越强。将含有酚酞的 Ba(OH)2 溶液平均分成两份置于两个烧杯中 并插入电导率传感器,往其中一份滴加稀硫酸,往另一份滴加硫酸钠溶液,滴加过程中,这两份溶液的滴加速率始终相同,测得溶液的电导率变化如图所示。下列说法正确的是__________

a.乙曲线电导率减小过程中,溶液由红色变为无色
b.乙曲线对应的反应中四种离子数目都减少
c.甲曲线对应氢氧化钡与硫酸钠反应
d.甲曲线上的 M 点代表两种溶液恰好完全反应
物质 | Ca(OH)2 | NaOH | CaCO3 | Ca(HCO3)2 | Na2CO3 | NaHCO3 |
溶解度/g | 0.16 | 109 | 0.0065 | 16.6 | 21.8 | 9.6 |
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向稀氢氧化钠溶液中通入 CO2,先生成 Na2CO3,继续通入 CO2,Na2CO3 会转化为 NaHCO3,已知后者为化合反应,请写出该化合反应的化学方程式:
②结合表格中的有关数据,若以 20℃时,100g 饱和溶液吸收 CO2 的质量最大为依据,则除去 CO 气体中的 CO2 杂质,应选择
③将 2.2g CO2 通入 47.8g 一定浓度的 NaOH溶液中充分反应后(反应过程中没有CO2 逸出,水也没有蒸发),溶液中的溶质仅有 Na2CO3和 NaHCO3 两种物质(NaHCO3 在水中电离成 Na+和 HCO3-),则此时溶液中碳元素的质量分数为
(3)电导率传感器可辅助探究复分解反应的实质。相同条件下,离子浓度越大,电导率越大,溶液导电性越强。将含有酚酞的 Ba(OH)2 溶液平均分成两份置于两个烧杯中 并插入电导率传感器,往其中一份滴加稀硫酸,往另一份滴加硫酸钠溶液,滴加过程中,这两份溶液的滴加速率始终相同,测得溶液的电导率变化如图所示。下列说法正确的是

a.乙曲线电导率减小过程中,溶液由红色变为无色
b.乙曲线对应的反应中四种离子数目都减少
c.甲曲线对应氢氧化钡与硫酸钠反应
d.甲曲线上的 M 点代表两种溶液恰好完全反应
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】以白云石(主要成分为CaCO3·MgCO3)为原料制备氢氧化镁的流程如下图:

已知:①MgCO3 MgO+CO2↑,CaCO3
MgO+CO2↑,CaCO3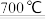 CaO+CO2↑;
CaO+CO2↑;
②反应器中发生的反应是(NH4)2SO4+MgO MgSO4+2NH3↑+H2O。
MgSO4+2NH3↑+H2O。
(1)该流程中,白云石轻烧的温度应低于_______ ℃
(2)该流程中,研磨的目的是_______ ;
(3)该流程中,不考虑H2O,可循环利用的物质是_______ (写化学式)。
(4)硫酸铵与应氧化镁在加热条件下反应生成一种盐、氨气和水。该反应的化学方程式是_______ 。

已知:①MgCO3
 MgO+CO2↑,CaCO3
MgO+CO2↑,CaCO3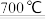 CaO+CO2↑;
CaO+CO2↑;②反应器中发生的反应是(NH4)2SO4+MgO
 MgSO4+2NH3↑+H2O。
MgSO4+2NH3↑+H2O。(1)该流程中,白云石轻烧的温度应低于
(2)该流程中,研磨的目的是
(3)该流程中,不考虑H2O,可循环利用的物质是
(4)硫酸铵与应氧化镁在加热条件下反应生成一种盐、氨气和水。该反应的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】2022年8月1日,国产C919大飞机完成取证试飞,该飞机的制造中9%的用料为钛合金。如图是工业上以金红石(主要成分是TiO2)为原料生产金属(Ti)的流程图;
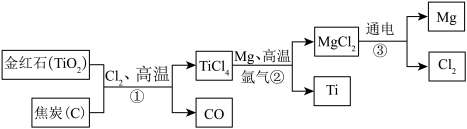
(1)金红石和焦炭要先粉碎处理,目的是_______ 。
(2)反应②要在氢气环境中进行,氩气能作保护气是利用了它的_______ 性质(“物理”或“化学”)。
(3)反应③的化学方程式为_______ ,该反应的基本反应类型是_______ 反应。
(4)该流程中可以循环利用的物质有_______ 。

(1)金红石和焦炭要先粉碎处理,目的是
(2)反应②要在氢气环境中进行,氩气能作保护气是利用了它的
(3)反应③的化学方程式为
(4)该流程中可以循环利用的物质有
您最近一年使用:0次

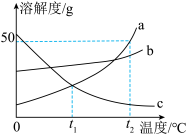
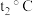 时,配制60g a物质的饱和溶液,需称量a的质量为
时,配制60g a物质的饱和溶液,需称量a的质量为