根据如图所示实验回答问题。______ ,实验过程中,气球先后发生的变化是______ 。
(2)乙实验的目的是______ 。
(3)丙中实验①的现象是______ ,要探究铁、铜、银的金属活动性顺序,X应是______ 溶液。
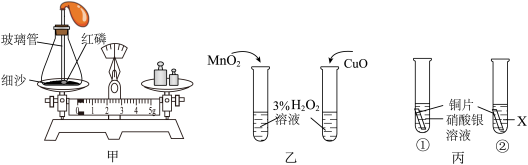
(2)乙实验的目的是
(3)丙中实验①的现象是
更新时间:2024-05-09 15:36:01
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】研究和控制化学反应条件有重要意义。
⑴同学们想探究双氧水的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验。记录各收集一瓶相同体积氧气所需要的时间。
① 取用二氧化锰的仪器是__________

②写出上述反应的文字表达式_______________________ 。
② 实验3中,加入二氧化锰的质量为___________ g。
③ 相同条件下,实验3产生氧气的速率最快,说明_____________________________ 。
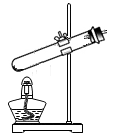
⑵同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气。为了验证加热双氧水也可以产生氧气,同学们选择上右图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是_____________________ 。
⑴同学们想探究双氧水的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验。记录各收集一瓶相同体积氧气所需要的时间。
| 实验 | 30%双氧水的质量(g) | 加入水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 |  | 67 |
① 取用二氧化锰的仪器是

②写出上述反应的文字表达式
② 实验3中,加入二氧化锰的质量为
③ 相同条件下,实验3产生氧气的速率最快,说明

⑵同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气。为了验证加热双氧水也可以产生氧气,同学们选择上右图装置(气密性良好)进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】兴趣小组同学做了如右图实验。实验中迅速涌出柱状的泡沫,可形象地称为“大象牙膏”,其原理主要是 和CuO混合迅速分解产生水和氧气,该反应的化学方程式为
和CuO混合迅速分解产生水和氧气,该反应的化学方程式为________ 。该反应中,CuO起________ 作用。

 和CuO混合迅速分解产生水和氧气,该反应的化学方程式为
和CuO混合迅速分解产生水和氧气,该反应的化学方程式为
您最近一年使用:0次
【推荐3】实验室常用下列装置制取气体,请你根据所学知识回答下列问题:
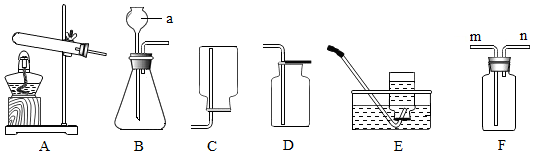
(1)写出图中标号仪器名称。a:_____ 。
(2)实验室用过氧化氢和二氧化锰制取氧气的化学方程式是_____ ,若用E装置收集的氧气不纯,则可能的一种原因是_____ 。
(3)选择F装置采用排空气法收集氧气,则气体应从_____ (填“m”或“n”)端进入。
(4)氨气可由氯化铵和熟石灰固体混合物加热制取。氨气极易溶于水、密度小于空气。由上述信息推知制取氨气的发生和收集装置是_____ (填A﹣E字母代号)。
(5)某科学小组同学提出了“制氧气的药品必须是含氧化合物,但不是所有含氧化合物都可以作为反应物制氧气”的观点,请从下列提供的用品中选择合适的药品及仪器,设计一组对比实验验证该观点是正确的。
用品:氯酸钾、二氧化锰、高锰酸钾、试管(主要成分SiO2)、酒精灯、铁架台、小木条、托盘天平
设计实验:_____ (要求写出操作方法、实验现象)。
(6)为探究过氧化氢溶液浓度、二氧化锰用量、温度对反应速率的影响,设计如下表实验方案:
①实验1、2的实验目的是_____ 。
②表中a、b取值可能是_____ 。

(1)写出图中标号仪器名称。a:
(2)实验室用过氧化氢和二氧化锰制取氧气的化学方程式是
(3)选择F装置采用排空气法收集氧气,则气体应从
(4)氨气可由氯化铵和熟石灰固体混合物加热制取。氨气极易溶于水、密度小于空气。由上述信息推知制取氨气的发生和收集装置是
(5)某科学小组同学提出了“制氧气的药品必须是含氧化合物,但不是所有含氧化合物都可以作为反应物制氧气”的观点,请从下列提供的用品中选择合适的药品及仪器,设计一组对比实验验证该观点是正确的。
用品:氯酸钾、二氧化锰、高锰酸钾、试管(主要成分SiO2)、酒精灯、铁架台、小木条、托盘天平
设计实验:
(6)为探究过氧化氢溶液浓度、二氧化锰用量、温度对反应速率的影响,设计如下表实验方案:
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 二氧化锰用量/g | 温度/℃ | 收集氧气体积/mL | 所需时间/s |
| 1 | 3 | 25 | 0.1 | 20 | 125 | |
| 2 | 3 | 25 | 0.2 | 20 | 125 | |
| 3 | a | 25 | 0.3 | b | 125 | |
| 4 | 4 | 25 | 0.3 | 40 | 125 | |
| 5 | 5 | 25 | 0.3 | 30 | 125 |
②表中a、b取值可能是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究,下图实验装置和选用药品均为教材图示,现分别以A、B、C、D表示如下:

A、B、C、D四个实验分别由甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察,
(1)A实验:白磷刚引燃,立即将锥形瓶放到天平上称量,结论是:质量不守恒;待锥形瓶冷却后,重新放到托盘天平上称量,天平平衡,结论是:质量守恒。你认为结论正确的是___________ (填“前一种”或“后一种”),而导致另一种结论错误的原因是___________ 。
(2)丙组同学认为C实验说明了质量守恒,请你从原子的角度说明为什么?___________ 。乙、丁两组同学得到的错误结论是“实验B、D均说明质量不守恒”,老师引导同学们分析了B、D两个实验反应前后天平不平衡的原因。你从为B实验天平不平衡的原因是___________ ,D实验天平不平衡的原因是___________ 。
(3)如果A装置中只是将药品改为少量的锌和稀硫酸,请问6.5g锌粒和足量稀硫酸最多可产生多少g氢气。

A、B、C、D四个实验分别由甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作、准确的称量和细致的观察,
(1)A实验:白磷刚引燃,立即将锥形瓶放到天平上称量,结论是:质量不守恒;待锥形瓶冷却后,重新放到托盘天平上称量,天平平衡,结论是:质量守恒。你认为结论正确的是
(2)丙组同学认为C实验说明了质量守恒,请你从原子的角度说明为什么?
(3)如果A装置中只是将药品改为少量的锌和稀硫酸,请问6.5g锌粒和足量稀硫酸最多可产生多少g氢气。
您最近一年使用:0次
实验题
|
适中
(0.65)
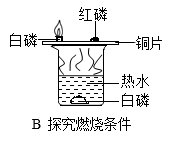
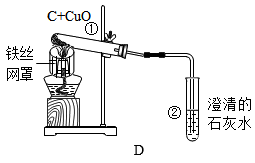
【推荐2】化学是一门以实验为基础的科学,根据下图所示的实验,请回答下列问题:
(1)A实验中,小气球的作用是___ ;
(2)B中依据___ 的现象事实,说明燃烧条件之一是可燃物与氧气接触;
(3)C图所示的实验,产生氢气与氧气的体积比为_ ;在水中加入少量硫酸钠的目 是__ ;
(4)D图所示的实验中,试管①中的实验现象是_ ;酒精灯加铁丝网的作用是______ 。
(5)如图是配置溶质质量分数为10%的NaCl溶液的实验操作示意图:
①用图中序号表示配制溶液的正确操作顺序:_____ ;
②称量NaCl时,天平平衡后的状态如图⑤所示,游码于标尺位置见图,则称取的NaCl质量为_______ g;
③NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的质量分数___ (填“大于”“小于”或“等于”)10%。
 |  |  |  |
(1)A实验中,小气球的作用是
(2)B中依据
(3)C图所示的实验,产生氢气与氧气的体积比为
(4)D图所示的实验中,试管①中的实验现象是
(5)如图是配置溶质质量分数为10%的NaCl溶液的实验操作示意图:
 |  |  |  |  |  |
①用图中序号表示配制溶液的正确操作顺序:
②称量NaCl时,天平平衡后的状态如图⑤所示,游码于标尺位置见图,则称取的NaCl质量为
③NaCl称量完毕放回砝码时,发现10g的砝码有缺损,若其他操作步骤正确,则所配制溶液的质量分数
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律:
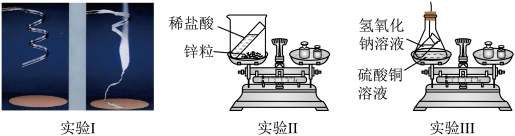
实验I:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量。
实验II:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与 锌粒接触,过一会在称量。
实验III:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉
淀和硫酸钠生成)过一会再称量。数据见下表:
(1)在实验I中,反应后的质量比反应前明显增加,请用质量守恒定律加以解释_______ 。
(2)实验II中发生反应共生成气体的质量是_______ 。
(3)这三个实验中,实验III正确反映了反应物与生成物之间的质量关系。请从分子、原子的角度解释反应前后质量相等的原因___________________ 。
(4)实验I、II不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路_______ 。

实验I:称量镁条,在空气中点燃,待反应结束后,将生成物全部收回再称量。
实验II:将装有稀盐酸的小试管放入装有锌粒的烧杯中,称量,然后将盐酸与 锌粒接触,过一会在称量。
实验III:将装有氢氧化钠溶液的试管放入盛有硫酸铜的锥形瓶中,并在锥型瓶口塞上橡皮塞,称量,然后设法将两种溶液接触(有蓝色氢氧化铜沉
淀和硫酸钠生成)过一会再称量。数据见下表:
| 编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应前/g | 4.8 | 112.6 | 118.4 |
| 反应后/g | 8.0 | 112.4 | 118.4 |
(2)实验II中发生反应共生成气体的质量是
(3)这三个实验中,实验III正确反映了反应物与生成物之间的质量关系。请从分子、原子的角度解释反应前后质量相等的原因
(4)实验I、II不能正确反映反应物和生成物之间的质量关系,选一例说明实验设计中的不当之处,并提出改进思路
您最近一年使用:0次
实验题
|
适中
(0.65)
真题
解题方法
【推荐1】认识金属的性质。如图是关于金属的几个实验。

(1)实验一中能证明铁生锈与水有关的现象是______ 。铁在潮湿的空气中会生锈,而在纯氧中可以燃烧,其燃烧的化学方程式为______ 。
(2)实验二是先向试管中加入一小段打磨过的镁条,然后加入______ ,待反应停止后再向试管中加入铜片,发现铜片表面没有变化,由此可证明活动性顺序是Mg>H>Cu。

(1)实验一中能证明铁生锈与水有关的现象是
(2)实验二是先向试管中加入一小段打磨过的镁条,然后加入
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐2】分类、类比是学习化学常用的方法。
(1)化学是一门以实验为基础的自然科学,初中化学课上做过许多实验,例如:
若按科学探究的方法进行分类,应将实验C归为①___________ 组(填“A”或“B”),理由是②_________ 。
(2)酸和碱反应能生成盐和水。若是强酸和强碱反应。则生成盐溶液显中性,若是强酸和弱碱反应生成的盐溶液则显酸性,同理,弱酸和强碱反应生成盐溶液则显碱性。请根据所学的知识推测:硫酸铵溶液是强酸和弱碱反应生成的盐溶液显①_______ (选填“酸性”“碱性”或“中性”),氯化钾溶液是强酸和强碱反应生成的盐溶液显②______ (选 填“酸性”或“碱性”或“中性”)
(1)化学是一门以实验为基础的自然科学,初中化学课上做过许多实验,例如:
A组 | B组 | 实验C | ||
碱式碳酸铜性质的探究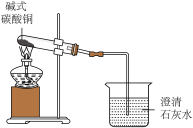 | 甲烷性质的探究 | 铁钉锈蚀条件的探究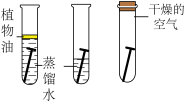 | 金属活动性的探究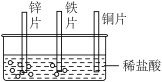 | 燃烧条件的探究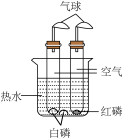 |
(2)酸和碱反应能生成盐和水。若是强酸和强碱反应。则生成盐溶液显中性,若是强酸和弱碱反应生成的盐溶液则显酸性,同理,弱酸和强碱反应生成盐溶液则显碱性。请根据所学的知识推测:硫酸铵溶液是强酸和弱碱反应生成的盐溶液显①
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】某研究小组为验证铁、铜、锌、银的金属活动性顺序,设计如图甲所示三个实验(三种金属均已用砂纸打磨过,其形状和大小相同,稀盐酸的浓度和用量也相同)。
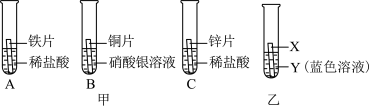
(1)实验前用砂纸打磨金属的目的是___________ 。
(2)一段时间后,实验B中可观察到的现象是___________ ,这说明铜比银的金属活动性___________ (“强”或“弱”),该反应的化学方程式为___________ 。
(3)乙同学认为仅仅通过上述实验不足以得出四种金属的活动性顺序,因此在上述实验的基础上,乙同学又补做了一个实验,装置如图乙所示,且实现了探究目的。乙同学的实验:X是金属___________ ,Y是___________ 蓝色溶液。

(1)实验前用砂纸打磨金属的目的是
(2)一段时间后,实验B中可观察到的现象是
(3)乙同学认为仅仅通过上述实验不足以得出四种金属的活动性顺序,因此在上述实验的基础上,乙同学又补做了一个实验,装置如图乙所示,且实现了探究目的。乙同学的实验:X是金属
您最近一年使用:0次



