解题方法
1 . 下列化学方程式符合题意且书写正确的是
| A.用盐酸除去铁锈:2HCl+FeO=FeCl2+H2O |
B.酒精在空气中燃烧:CH4+2O2 CO2+2H2O CO2+2H2O |
| C.验证质量守恒定律:2HNO3+Na2SO4=2NaNO3+H2SO4 |
| D.医疗上用氢氧化铝治疗胃酸过多症:Al(OH)3+3HCl= AlCl3+3H2O |
您最近一年使用:0次
解题方法
2 . 实验是化学学习常用的方法。有关如图所示实验,下列说法正确的是
A.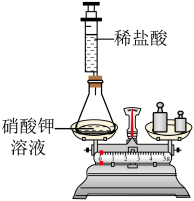 图1实验可用于验证质量守恒定律 图1实验可用于验证质量守恒定律 |
B.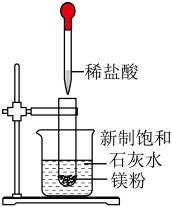 图2实验说明镁和稀盐酸反应放热 图2实验说明镁和稀盐酸反应放热 |
C.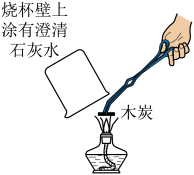 图3实验说明木炭燃烧生成二氧化碳 图3实验说明木炭燃烧生成二氧化碳 |
D.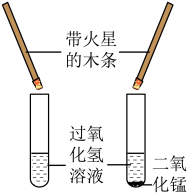 图4实验说明二氧化锰是过氧化氢分解的催化剂 图4实验说明二氧化锰是过氧化氢分解的催化剂 |
您最近一年使用:0次
解题方法
3 . 某研究所利用太阳能聚光器获得的高能量进行热化学循环反应制取 ,其流程如图所示,下列有关说法不正确的是
,其流程如图所示,下列有关说法不正确的是
 ,其流程如图所示,下列有关说法不正确的是
,其流程如图所示,下列有关说法不正确的是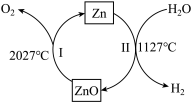
| A.反应Ⅰ属于分解反应 |
| B.反应Ⅱ中锌元素的化合价升高 |
C. 燃烧热值高,是一种理想的清洁能源 燃烧热值高,是一种理想的清洁能源 |
| D.该循环过程中,锌的质量不断减少 |
您最近一年使用:0次
4 . 下列图像与描述相符的是
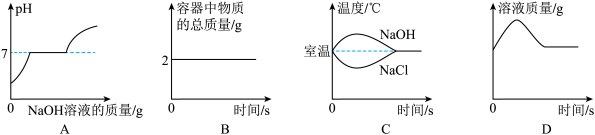
| A.向盛有HCl和BaCl2的混合溶液中,逐滴滴入一定溶质质量分数的NaOH溶液至过量 |
| B.1g硫和1g氧气在密闭容器中充分反应 |
| C.NaOH和NaCl固体室温下分别溶于足量的水中 |
| D.向氢氧化钙的饱和溶液中加入一定量的氧化钙固体 |
您最近一年使用:0次
名校
解题方法
5 . 水是生活中最常见且最重要的物质,下列说法正确的是
| A.生活:油锅着火用水来扑灭 | B.人体:水是人体中重要的营养素 |
| C.实验:溶液的溶剂一定是水 | D.能源:用特殊催化剂可把水变成汽油 |
您最近一年使用:0次
解题方法
6 . 学完新课,同学们回顾“验证质量守恒定律”的实验,对其进行系统整理和思考。
【回顾旧知】“化学反应前后物质的质量关系”的实验探究方案(图1)。_______ (填“向左偏转”、“向右偏转”或“不偏转”)。
(2)实验2观察到反应后天平不平衡,从物质变化的视角解释原因:_______ 。
(3)化学反应中质量守恒的微观本质原因是:在化学反应前后,原子的种类、_______ 和质量不变。
【改进拓展】
(4)该小组同学将上述实验1中的反应装置加以改装(图2所示),同时将红磷换成白磷(白磷着火点40℃),并按下列实验步骤开展探究。
步骤2:从天平上取下装置打开止水夹K1和K2,从K1处缓慢通入约50mL氧气,再关闭K1和K2,再次称量装置总质量为m2g。
步骤3:将锥形瓶浸入80℃的热水中,观察现象。
步骤4:取出装置,恢复至室温并擦干锥形瓶,称量装置总质量为m3g。
①在上述步骤3中气球出现的现象是_______ 。
②三次称量的m1、m2、m3的大小关系是_______ 。
【拓展延伸】实验1中因有氧气参加,故采用密闭装置。实验3为什么也要用密闭装置呢?
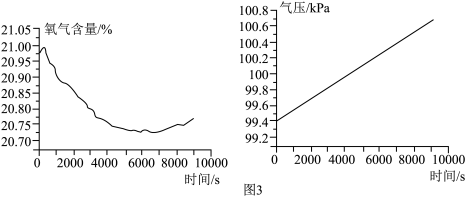
在老师的指导下小组同学再次实验,实验过程中保持溶液温度不变并使用氧气浓度传感器和气体压强传感器测定锥形瓶内氧气浓度和气体压强的变化,绘制如图曲线。_______ ,实验过程中保持溶液温度不变,其目的是_______ 。
【回顾旧知】“化学反应前后物质的质量关系”的实验探究方案(图1)。
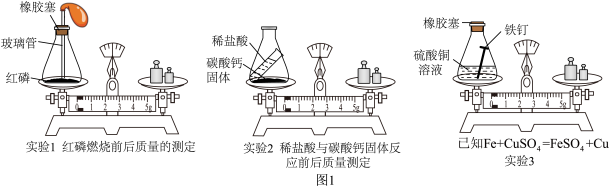
(2)实验2观察到反应后天平不平衡,从物质变化的视角解释原因:
(3)化学反应中质量守恒的微观本质原因是:在化学反应前后,原子的种类、
【改进拓展】
(4)该小组同学将上述实验1中的反应装置加以改装(图2所示),同时将红磷换成白磷(白磷着火点40℃),并按下列实验步骤开展探究。
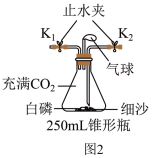
步骤2:从天平上取下装置打开止水夹K1和K2,从K1处缓慢通入约50mL氧气,再关闭K1和K2,再次称量装置总质量为m2g。
步骤3:将锥形瓶浸入80℃的热水中,观察现象。
步骤4:取出装置,恢复至室温并擦干锥形瓶,称量装置总质量为m3g。
①在上述步骤3中气球出现的现象是
②三次称量的m1、m2、m3的大小关系是
【拓展延伸】实验1中因有氧气参加,故采用密闭装置。实验3为什么也要用密闭装置呢?
在老师的指导下小组同学再次实验,实验过程中保持溶液温度不变并使用氧气浓度传感器和气体压强传感器测定锥形瓶内氧气浓度和气体压强的变化,绘制如图曲线。
您最近一年使用:0次
解题方法
7 . 质量守恒定律的发现对化学的发展作出了重要贡献,教师引导同学们了解质量守恒定律的发现史,并体会质量守恒定律重要价值意义。
【活动一】查阅史料,认识质量守恒定律。
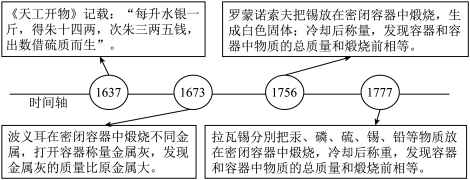
(1)阅读下列信息,回答问题。_______ 两。
②导致波义耳与质量守恒定律失之交臂的具体原因是_______ 。
③与罗蒙诺索夫相比,拉瓦锡得出的实验结论更可靠,其原因是_______ 。
(2)质量守恒定律的发现过程,给我们的启示是_______(多选,填标号)。
【活动二】体会质量守恒定律的重要应用价值
(3)我国著名化学家侯德榜先生在氨碱法的基础上创立了更为先进的侯氏制碱法,促进了世界制碱技术的发展。以NaCl为原料制取纯碱(Na2CO3),从元素守恒的观点来看,还需要补充_______ (填写元素符号)两种元素。
(4)空气是重要的资源,要制取化肥氯化铵(NH4Cl)可直接从空气中获取_______ 作为原料。
(5)下列叙述符合质量守恒定律的是_______(填字母代号)。
【活动一】查阅史料,认识质量守恒定律。
(1)阅读下列信息,回答问题。
②导致波义耳与质量守恒定律失之交臂的具体原因是
③与罗蒙诺索夫相比,拉瓦锡得出的实验结论更可靠,其原因是
(2)质量守恒定律的发现过程,给我们的启示是_______(多选,填标号)。
| A.分析问题应该全面、严谨 |
| B.实验的成功与否,只取决于药品的选择 |
| C.定量方法是科学研究的重要方法 |
| D.科学研究既要尊重事实,也要勇于创新 |
【活动二】体会质量守恒定律的重要应用价值
(3)我国著名化学家侯德榜先生在氨碱法的基础上创立了更为先进的侯氏制碱法,促进了世界制碱技术的发展。以NaCl为原料制取纯碱(Na2CO3),从元素守恒的观点来看,还需要补充
(4)空气是重要的资源,要制取化肥氯化铵(NH4Cl)可直接从空气中获取
(5)下列叙述符合质量守恒定律的是_______(填字母代号)。
| A.50mL水和50mL乙醇混合后总体积小于100mL |
| B.3g碳与9g氧气充分反应后生成12g二氧化碳 |
| C.10克水电解一段时间后,产生氢气和氧气的总质量只有5克 |
您最近一年使用:0次
8 . 某兴趣小组的同学对一份固体样品进行了探究,通过实验已确定该样品由氧化铜和铜粉混合而成。他们称取了20g固体样品,用图甲所示的装置进行实验至反应完全,测定装置B反应前后的数据如图乙所示。请计算:___________ g;
(2)固体样品中氧化铜的质量分数。
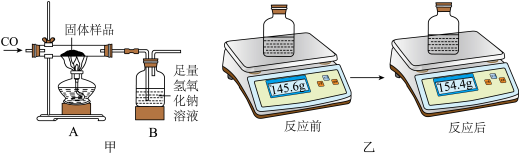
(2)固体样品中氧化铜的质量分数。
您最近一年使用:0次
解题方法
9 . 宋代德化窑白瓷(含CaSiO3)因其纯粹的凝脂白享誉国际。烧制过程中会发生一系列化学反应,其中包括 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.CaCO3属于盐类物质 | B.生成的CaSiO3是黑色固体 |
| C.该反应属于置换反应 | D.该反应前后固体总质量不变 |
您最近一年使用:0次
7日内更新
|
20次组卷
|
2卷引用:2024年吉林省长春市中考一模化学试题
解题方法
10 . 华为Mate60 pro手机一经上市,销售异常火爆,这款手机最大的亮点就是它搭载了国产芯片。芯片的主要成分是纯度极高的硅,其运算速率与硅的纯度有关。
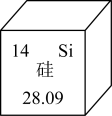
(1)硅元素在元素周期表中的相关信息如图所示,硅的相对原子质量是___________ 。___________ 。(填序号)___________ ,下列关于该反应的说法正确的是___________ (填字母)。
A.反应前后分子数目不发生改变 B.反应中涉及两种单质
C.反应前后硅元素的化合价不变 D.反应遵循质量守恒定律
(1)硅元素在元素周期表中的相关信息如图所示,硅的相对原子质量是
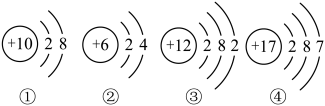
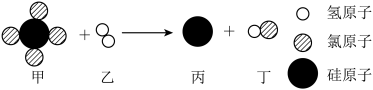
A.反应前后分子数目不发生改变 B.反应中涉及两种单质
C.反应前后硅元素的化合价不变 D.反应遵循质量守恒定律
您最近一年使用:0次



