学完新课,同学们回顾“验证质量守恒定律”的实验,对其进行系统整理和思考。
【回顾旧知】“化学反应前后物质的质量关系”的实验探究方案(图1)。_______ (填“向左偏转”、“向右偏转”或“不偏转”)。
(2)实验2观察到反应后天平不平衡,从物质变化的视角解释原因:_______ 。
(3)化学反应中质量守恒的微观本质原因是:在化学反应前后,原子的种类、_______ 和质量不变。
【改进拓展】
(4)该小组同学将上述实验1中的反应装置加以改装(图2所示),同时将红磷换成白磷(白磷着火点40℃),并按下列实验步骤开展探究。
步骤2:从天平上取下装置打开止水夹K1和K2,从K1处缓慢通入约50mL氧气,再关闭K1和K2,再次称量装置总质量为m2g。
步骤3:将锥形瓶浸入80℃的热水中,观察现象。
步骤4:取出装置,恢复至室温并擦干锥形瓶,称量装置总质量为m3g。
①在上述步骤3中气球出现的现象是_______ 。
②三次称量的m1、m2、m3的大小关系是_______ 。
【拓展延伸】实验1中因有氧气参加,故采用密闭装置。实验3为什么也要用密闭装置呢?
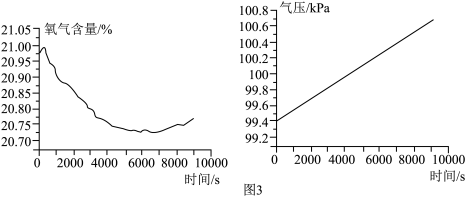
在老师的指导下小组同学再次实验,实验过程中保持溶液温度不变并使用氧气浓度传感器和气体压强传感器测定锥形瓶内氧气浓度和气体压强的变化,绘制如图曲线。_______ ,实验过程中保持溶液温度不变,其目的是_______ 。
【回顾旧知】“化学反应前后物质的质量关系”的实验探究方案(图1)。
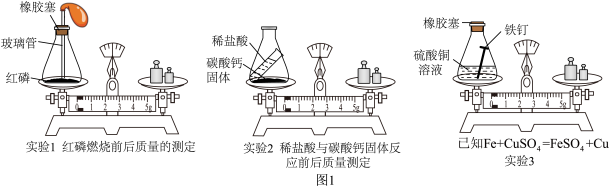
(2)实验2观察到反应后天平不平衡,从物质变化的视角解释原因:
(3)化学反应中质量守恒的微观本质原因是:在化学反应前后,原子的种类、
【改进拓展】
(4)该小组同学将上述实验1中的反应装置加以改装(图2所示),同时将红磷换成白磷(白磷着火点40℃),并按下列实验步骤开展探究。
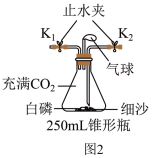
步骤2:从天平上取下装置打开止水夹K1和K2,从K1处缓慢通入约50mL氧气,再关闭K1和K2,再次称量装置总质量为m2g。
步骤3:将锥形瓶浸入80℃的热水中,观察现象。
步骤4:取出装置,恢复至室温并擦干锥形瓶,称量装置总质量为m3g。
①在上述步骤3中气球出现的现象是
②三次称量的m1、m2、m3的大小关系是
【拓展延伸】实验1中因有氧气参加,故采用密闭装置。实验3为什么也要用密闭装置呢?
在老师的指导下小组同学再次实验,实验过程中保持溶液温度不变并使用氧气浓度传感器和气体压强传感器测定锥形瓶内氧气浓度和气体压强的变化,绘制如图曲线。
更新时间:2024-05-24 18:17:30
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】小明在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物。他非常好奇,进行了如下探究。
实验探究1:镁条与碳酸氢钠溶液反应产生什么气体?
甲同学猜想:可能是二氧化碳;
乙同学猜想:可能是氢气。
同学们作出猜想的依据是_______ 。
【设计实验】将产生的气体收集起来,做如下实验:
实验探究2:产生的白色不溶物是什么?
【查阅资料】Mg(OH)2难溶于水;MgCO3微溶于水;这两种物质受热都会分解成两种氧化物。
【提出猜想】猜想1:白色固体是Mg(OH)2
猜想2:白色固体是MgCO3;
猜想3:_______ 。
【实验研究】取白色固体于试管中,滴加足量的稀盐酸,观察到_______ ,得出猜想1一定不正确。写出产生该现象的反应化学方程式_______ ,小明通过进一步实验验证得出猜想3成立,写出实验操作及实验现象_______ 。
实验探究1:镁条与碳酸氢钠溶液反应产生什么气体?
甲同学猜想:可能是二氧化碳;
乙同学猜想:可能是氢气。
同学们作出猜想的依据是
【设计实验】将产生的气体收集起来,做如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 将收集的气体通入澄清石灰水中 | 甲同学猜想错误 | |
| 将收集的气体点燃 | 气体燃烧,产生淡蓝色火焰,有尖锐的爆鸣声 | 乙同学猜想正确 |
【查阅资料】Mg(OH)2难溶于水;MgCO3微溶于水;这两种物质受热都会分解成两种氧化物。
【提出猜想】猜想1:白色固体是Mg(OH)2
猜想2:白色固体是MgCO3;
猜想3:
【实验研究】取白色固体于试管中,滴加足量的稀盐酸,观察到
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】我国著名的闽籍制碱专家侯德榜,在纯碱制造方面做出了重大贡献。用“侯氏制碱法”制得的纯碱中常含有氯化钠等杂质,化学兴趣小组欲对某品牌纯碱样品中碳酸钠的质量分数进行实验探究,在老师的指导下,他们设计了下列两种实验方案进行试验。
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应。
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳。
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
(2)分析滴加的CaCl2溶液要过量的原因: _______ ;
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量。利用沉淀物质量计算Na2CO3的质量分数为91%。如果不洗涤沉淀物会造成测定结果大于91%,这是因为_________ 。
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。

(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的CO2,再接上装置C和D。
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为_______ 。
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿。根据_______ 定律,装置C在反应前后的质量差就是产生CO2的质量,由此计算出该样品中Na2CO3的质量分数。若没有装置D,将会使测定结果 _______ (选填“偏大”或“偏小”)。
资料摘要:
Ⅰ.碳酸钠和氯化钙能发生复分解反应。
Ⅱ.浓硫酸具有很强的吸水性;碱石灰常用于吸收水蒸气和二氧化碳。
[方案一]样品与氯化钙溶液反应,测定Na2CO3的质量分数
(1)样品与氯化钙溶液的反应实验(杂质不与氯化钙溶液反应):
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液。 | 产生白色沉淀 | 反应的化学方程式: |
(3)将反应后的混合物进行过滤,把获得的沉淀物进行洗涤、干燥、称量。利用沉淀物质量计算Na2CO3的质量分数为91%。如果不洗涤沉淀物会造成测定结果大于91%,这是因为
[方案二]样品与稀盐酸反应,测定Na2CO3的质量分数
利用下图所示实验装置(铁架台略去)和试剂,通过测定样品和稀盐酸反应产生的CO2气体的质量,计算Na2CO3的质量分数(装置气密性良好,忽略盐酸的挥发性且每步反应或作用都是完全的)。

(4)打开止水夹K,先对装置A和B(已连接)通入已除去CO2的空气一会儿,以排尽装置A和B中含有的CO2,再接上装置C和D。
(5)关闭止水夹K,加入足量的稀盐酸(杂质不与盐酸反应),装置A中样品产生气体的化学方程式为
(6)待装置A中的反应结束后,再一次打开止水夹K,继续往装置通入已除去CO2的空气一会儿。根据
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小滕和大刘两位同学以“化学反应中的反应物与生成物的质量关系”为课题,进行科学探究活动,请你与他们一起完成下列探究任务。
【提出问题】当物质发生化学反应生成新物质时,反应物的质量总和与生成物的质量总和是否相等?
【实验探究】小滕设计的实验装置和选用的药品如图A所示,大刘设计的实验装置和选用的药品如图B所示。
(1)A图中物质发生反应的化学方程式是______ ;
(2)大刘在锥形瓶中观察到的现象是______ ;
(3)小滕同学用图A装置探究质量守恒定律,实验结束后,观察到天平指针向______ 偏转(选填“左”或“右”)。
【交流评价】
小滕的结论:根据自己的实验得出,参加化学反应的各物质的质量总和,与反应后生成的各物质的质量总和不相等。
大刘的结论:根据自己的实验得出,参加化学反应的各物质的质量总和,与反应后生成的各物质的质量总和相等。
(4)小滕和大刘的结论中错误的是______ 的结论。理由是:______ 。
【结论与解释】
(5)通过上述探究实验,我们可知在验证质量守恒定律时,应该注意的问题是若利用有气体参加或______ 的化学反应来设计实验,应选用______ 的实验装置。
【提出问题】当物质发生化学反应生成新物质时,反应物的质量总和与生成物的质量总和是否相等?
【实验探究】小滕设计的实验装置和选用的药品如图A所示,大刘设计的实验装置和选用的药品如图B所示。
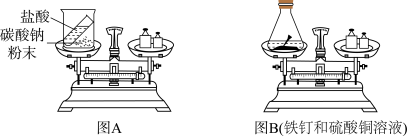
(1)A图中物质发生反应的化学方程式是
(2)大刘在锥形瓶中观察到的现象是
(3)小滕同学用图A装置探究质量守恒定律,实验结束后,观察到天平指针向
【交流评价】
小滕的结论:根据自己的实验得出,参加化学反应的各物质的质量总和,与反应后生成的各物质的质量总和不相等。
大刘的结论:根据自己的实验得出,参加化学反应的各物质的质量总和,与反应后生成的各物质的质量总和相等。
(4)小滕和大刘的结论中错误的是
【结论与解释】
(5)通过上述探究实验,我们可知在验证质量守恒定律时,应该注意的问题是若利用有气体参加或
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】化学兴趣小组探究质量守恒定律的内容,请你与他们一起完成探究任务:
(碳酸钠能溶于水,但和水不反应)
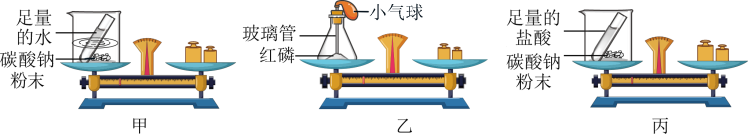
【提出问题】化学反应中,参加反应的物质质量总和与生成物的物质质量总和是否相等?
【进行实验】如图所示:甲、乙、丙同学设计实验装置和选择药品,顺利完成实验。
【收集证据】甲、乙同学都得出的结论:在化学反应中,参加反应的物质质量总和与生成物的质量总和相等。
【交流评价】
(1)请你评价:______ (填“甲”或“乙”)同学的结论是错误的,理由是______ ;
(2)小气球发生的变化情况是______ ;
(3)丙同学实验中足量盐酸与碳酸钠粉末反应的现象是______ ,丙同学的实验______ (填“符合”或“不符合”)质量守恒定律。
(碳酸钠能溶于水,但和水不反应)

【提出问题】化学反应中,参加反应的物质质量总和与生成物的物质质量总和是否相等?
【进行实验】如图所示:甲、乙、丙同学设计实验装置和选择药品,顺利完成实验。
【收集证据】甲、乙同学都得出的结论:在化学反应中,参加反应的物质质量总和与生成物的质量总和相等。
【交流评价】
(1)请你评价:
(2)小气球发生的变化情况是
(3)丙同学实验中足量盐酸与碳酸钠粉末反应的现象是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】用下列实验装置证明质量守恒定律(反应前天平已经调节平衡)。
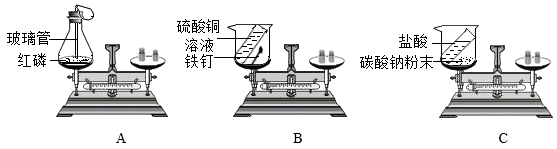
【A实验】该装置中气球的作用是________ ,反应前和反应结束冷却后对比,天平指针________ (选填“偏左”、“偏右”或“不偏转”);
【B实验】铁钉与硫酸铜溶液反应的化学方程式为_______ ,该反应的实验现象是________ 。
【C实验】碳酸钠粉末与稀盐酸反应的化学方程式为_______ ,反应后天平指针会________ (选填“偏左”、“偏右”或“不偏转”):
【谈感受】设计探究质量守恒定律的有关实验中若有气体参与或生成,实验的装置需要________ 处理。

【A实验】该装置中气球的作用是
【B实验】铁钉与硫酸铜溶液反应的化学方程式为
【C实验】碳酸钠粉末与稀盐酸反应的化学方程式为
【谈感受】设计探究质量守恒定律的有关实验中若有气体参与或生成,实验的装置需要
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】物质发生化学变化前后,总质量是否发生改变?是增加、减小还是不变?小刘、小李按下面的步骤进行探究:

【提出假设】物质发生化学变化前后总质量不变。
【设计并进行实验】小刘设计的实验装置和选用的药品如A所示,小李设计的实验装置和选用的药品如B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
这两个实验所发生反应的化学方程式分别为:
小刘的实验:__________ ;
小李的实验:__________ 。
【结论与解释】
小刘认为:在化学反应中,反应后生成的各物质的总质量与参加反应的各物质的总质量相等;小李认为:在化学反应中,反应后生成的各物质的总质量与参加反应的各物质的总质量不相等。
你认为_________ 的结论正确,导致另一个实验结论错误的原因是:______ ;请从原子的角度分析你认为正确的结论的原因:_____ 。
【反思与评价】在探究化学变化中反应物和生成物的质量关系时,若是_____ 的反应,应放在密闭容器中进行实验。

【提出假设】物质发生化学变化前后总质量不变。
【设计并进行实验】小刘设计的实验装置和选用的药品如A所示,小李设计的实验装置和选用的药品如B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
这两个实验所发生反应的化学方程式分别为:
小刘的实验:
小李的实验:
【结论与解释】
小刘认为:在化学反应中,反应后生成的各物质的总质量与参加反应的各物质的总质量相等;小李认为:在化学反应中,反应后生成的各物质的总质量与参加反应的各物质的总质量不相等。
你认为
【反思与评价】在探究化学变化中反应物和生成物的质量关系时,若是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;稀盐酸与氢氧化钠反应生成水和氯化钠)
(1)提出假设:化学反应中,反应物的总质量与生成物的总质量____ 。
(2)确定研究方法:分析推理,查阅资料,实验探究。
(3)设计并进行实验:小刚设计的实验装置和选用药品如图A所示,小洁的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。

(4)实验结论:通过实验,小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等。小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等,你认为结论正确的是____ ,请你谈谈导致另一种结论错误的原因:___ 。
(5)结论分析:请从原子的角度,简要分析你认为正确的结论:__
(6)结论应用:环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式是:I2O5+5CO=I2+5X 根据生成X的多少,可以判断CO的含量,X的化学式是________ 。
(1)提出假设:化学反应中,反应物的总质量与生成物的总质量
(2)确定研究方法:分析推理,查阅资料,实验探究。
(3)设计并进行实验:小刚设计的实验装置和选用药品如图A所示,小洁的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。

(4)实验结论:通过实验,小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等。小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等,你认为结论正确的是
(5)结论分析:请从原子的角度,简要分析你认为正确的结论:
(6)结论应用:环保部门常用I2O5测定空气受CO污染的程度,发生反应的化学方程式是:I2O5+5CO=I2+5X 根据生成X的多少,可以判断CO的含量,X的化学式是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】初三某化学兴趣小组同学。依据教材实验对化学反应前后质量变化进行了探究。
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【实验装置设计】甲、乙、丙小组同学分别设计如图装置:

【讨论与探究】(1)甲小组实验中,白磷燃烧时,在锥形瓶底部加入少量细沙,其目的是:_______ 。
实验现象是_______ 。
(2)请根据乙组和丙组设计的“质量守恒定律”的实验装置进行探究,并按要求完成乙组和丙组。
①乙组实验结束后可观察到天平_______ (是或否)平衡;此反应_______ (填“遵守”或“不遵守”)质量守恒定律。
②丙组过氧化氢溶液分解反应前后各物质质量总和的测定,得出参加化学反应的各物质的质量总和___ (填“大于”、“等于”或“小于”)反应后生成的各物质的质量总和。该反应中二氧化锰起____ 作用。
【实验分析】请你从原子的角度解释质量守恒的原因:____ 。
【反思与交流】通过甲、乙、丙小组实验的探究,你得到的启示是:当有气体参与或有气体生成的反应,如果要验证质量守恒定律,需在____ 的容器中进行。
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【实验装置设计】甲、乙、丙小组同学分别设计如图装置:

【讨论与探究】(1)甲小组实验中,白磷燃烧时,在锥形瓶底部加入少量细沙,其目的是:
实验现象是
(2)请根据乙组和丙组设计的“质量守恒定律”的实验装置进行探究,并按要求完成乙组和丙组。
①乙组实验结束后可观察到天平
②丙组过氧化氢溶液分解反应前后各物质质量总和的测定,得出参加化学反应的各物质的质量总和
【实验分析】请你从原子的角度解释质量守恒的原因:
【反思与交流】通过甲、乙、丙小组实验的探究,你得到的启示是:当有气体参与或有气体生成的反应,如果要验证质量守恒定律,需在
您最近一年使用:0次
【推荐3】铜器在潮湿的空气中容易生锈。铜锈(俗称铜绿)的主要成分是Cu2(OH)2CO3,那么,铜在什么条件下容易生锈呢?为此,小明同学设计了以下实验,请你参与探究。

【提出假设】铜生锈是铜与氧气、___ 和 ___ 共同作用的结果。
【设计方案】为验证假设,小明同学设计了如图1实验方案:
(1)B的实验目的是___ 。
(2)装置C中有一处明显错误,用文字叙述加以改正___ ;NaOH溶液的作用是(用化学方程式表示) ___ 。
(3)小明同学的这个实验方案不完整,还需要再补充一个实验。请在图2框中绘出该实验的装置图。____
【结论】经过探究,得知了铜生锈的条件。

【提出假设】铜生锈是铜与氧气、
【设计方案】为验证假设,小明同学设计了如图1实验方案:
(1)B的实验目的是
(2)装置C中有一处明显错误,用文字叙述加以改正
(3)小明同学的这个实验方案不完整,还需要再补充一个实验。请在图2框中绘出该实验的装置图。
【结论】经过探究,得知了铜生锈的条件。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】空气质量与人类的健康息息相关。某校化学社团开展了微型空气质量“检测站”的组装与使用、并进行了检测某小区地下车库的空气质量、分析某化工厂附近降雨类型、调查空气污染的原因等项目化学习。
任务一:微型空气质量“检测站”的组装
【组装步骤】
①阅读安装说明书。
②将空气质量检测站组件—采样系统(检测站)、分析系统和数据传输系统连接起来(如图)。

③联网调试。
任务二:检测某小区地下车库中的有害气体
【测定实验】利用微型空气质量“检测站”能检验多种空气污染物。用该“检测站”测得某小区地下车库中一氧化碳在不同时间段内的浓度如图。(已知:50ppm为一氧化碳准许成年人置身其中的最大量)
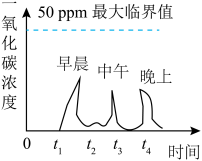
(1)【交流分析】一氧化碳浓度最大的时间段是___________ ,原因可能是___________ 。
任务三:设计实验分析某化工厂区附近降雨的类型
【调查分析】同学们通过走访调查,得知该化工厂区附近所降雨水为酸雨。
【查阅资料】常见酸雨根据致酸物质分为硫酸型酸雨和硝酸型酸雨。
(2)【进行实验】
【反思评价】
(3)步骤2发生的反应的化学方程式为___________ 。
(4)小李同学认为只进行步骤②即可得出结论,理由是___________ 。
任务四:调查空气污染的原因
(5)【交流讨论】空气污染是由___________ (填一种燃料)的燃烧造成的。
(6)【成果分享】同学们通过项目化学习,了解了微型空气质量“检测站”的组装和使用、有害气体的检测等,他们一起制作了保护空气倡议书,请你将其补充完整。
任务一:微型空气质量“检测站”的组装
【组装步骤】
①阅读安装说明书。
②将空气质量检测站组件—采样系统(检测站)、分析系统和数据传输系统连接起来(如图)。

③联网调试。
任务二:检测某小区地下车库中的有害气体
【测定实验】利用微型空气质量“检测站”能检验多种空气污染物。用该“检测站”测得某小区地下车库中一氧化碳在不同时间段内的浓度如图。(已知:50ppm为一氧化碳准许成年人置身其中的最大量)

(1)【交流分析】一氧化碳浓度最大的时间段是
任务三:设计实验分析某化工厂区附近降雨的类型
【调查分析】同学们通过走访调查,得知该化工厂区附近所降雨水为酸雨。
【查阅资料】常见酸雨根据致酸物质分为硫酸型酸雨和硝酸型酸雨。
(2)【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量雨水于试管中,利用pH计检测 | pH | 该化工厂区附近所降雨水为硫酸型酸雨 |
| ②取少量雨水于试管中,向其中滴加 | 有白色沉淀生成 |
【反思评价】
(3)步骤2发生的反应的化学方程式为
(4)小李同学认为只进行步骤②即可得出结论,理由是
任务四:调查空气污染的原因
(5)【交流讨论】空气污染是由
(6)【成果分享】同学们通过项目化学习,了解了微型空气质量“检测站”的组装和使用、有害气体的检测等,他们一起制作了保护空气倡议书,请你将其补充完整。
| 保护空气倡议书 为了使天空更蓝,人类正在积极行动,我们能做的很多,比如,其中一种保护空气的具体做法是 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐2】Vc泡腾片是一种含有大量维生素C的片状药剂,可增强机体抵抗力,用于预防和治疗坏血病等疾病。泡腾片的成份中含有崩解剂,崩解剂在崩解过程中能迅速产生大量气泡(如图1所示)。针对Vc泡腾片投入水中迅速崩解产生大量气泡这一现象,激起了同学们浓厚的兴趣,在老师的指导下,兴趣小组的同学们对某Vc泡腾片的发泡原理进行如下探究活动。请回答相关问题。
【查阅资料】
①该Vc泡腾片的主要成分有:维生素C(化学式为C6H8O6、柠檬酸(H3Ci)、食盐(NaCl)、碳酸氢钠(NaHCO3、淀粉[(C6H10O5)n]、山梨糖醇(C6H14O6)等
②泡腾崩解剂包括酸源和碱源,常用的酸源有柠檬酸等,常用的碱源有碳酸氢钠等。
③柠檬酸是一种有机酸,碳酸氢钠俗称小苏打。
④碱石灰的主要成分为NaOH和CaO的混合物。______ (填“混合物”或“纯净物”),其中维生素C由______ 种元素组成。
【实验探察】
探究一:Vc泡腾片的发泡原理
(2)按如图2装置进行实验,将稀盐酸滴入碳酸氢钠固体中,观察到的现象是:______ ,请写出其反应的化学方程式______ 。
(3)图3是稀盐酸与碳酸氢钠反应的微观示意图,结合图2。实验可知稀盐酸和NaHCO3反应的微观实质是______ 。
实验结论:结合资料得出该Vc泡腾片的发泡原理是柠檬酸与碳酸氢钠发生反应。
探究二:探究Vc泡腾片中NaHCO3的含量
为探究该Vc泡腾片中NaHCO3的含量,同学们进行了如图4所示的探究。
Ⅰ、连接装置,检查装置的气密性
Ⅱ、向B装置中加入10.00g泡腾片,反应前称得D装置及药品的质量为200.00g;
Ⅲ、按图A所示连接好装置后,关闭K,向B装置中加入足是的稀硫酸,B中发生反应的化学方程式为:H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2↑;
Ⅳ、当B装置中不再有气泡产生时,打开K,先通入一段时间的空气(将B装置中产生的CO2气体全部排入D装置),待D装置中质量不再发生变化,称量D装置及药品质量为201.32g。(原装置中的空气对实验结果的影响忽略不计)。
实验结论:
(4)根据以上实验可知:图4中A装置的作用是______ ,该Vc泡腾片中NaHCO3的质量分数为______ 。如果没有E装置,测得NaHCO3的质量分数将______ (填“偏大”或“偏小”或“不变”)。
【实验反思】
①由于Vc泡腾片投入水中会迅速产生大量二氧化碳,直接服用易导致腹胀,腹痛甚至置肠穿孔,所以应先用水溶解摇匀后再服用;
②服用Vc泡腾片请遵医喝。
【查阅资料】
①该Vc泡腾片的主要成分有:维生素C(化学式为C6H8O6、柠檬酸(H3Ci)、食盐(NaCl)、碳酸氢钠(NaHCO3、淀粉[(C6H10O5)n]、山梨糖醇(C6H14O6)等
②泡腾崩解剂包括酸源和碱源,常用的酸源有柠檬酸等,常用的碱源有碳酸氢钠等。
③柠檬酸是一种有机酸,碳酸氢钠俗称小苏打。
④碱石灰的主要成分为NaOH和CaO的混合物。

【实验探察】
探究一:Vc泡腾片的发泡原理
(2)按如图2装置进行实验,将稀盐酸滴入碳酸氢钠固体中,观察到的现象是:
(3)图3是稀盐酸与碳酸氢钠反应的微观示意图,结合图2。实验可知稀盐酸和NaHCO3反应的微观实质是
实验结论:结合资料得出该Vc泡腾片的发泡原理是柠檬酸与碳酸氢钠发生反应。
探究二:探究Vc泡腾片中NaHCO3的含量
为探究该Vc泡腾片中NaHCO3的含量,同学们进行了如图4所示的探究。
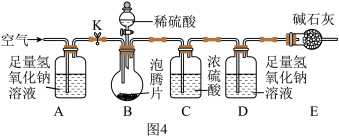
Ⅰ、连接装置,检查装置的气密性
Ⅱ、向B装置中加入10.00g泡腾片,反应前称得D装置及药品的质量为200.00g;
Ⅲ、按图A所示连接好装置后,关闭K,向B装置中加入足是的稀硫酸,B中发生反应的化学方程式为:H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2↑;
Ⅳ、当B装置中不再有气泡产生时,打开K,先通入一段时间的空气(将B装置中产生的CO2气体全部排入D装置),待D装置中质量不再发生变化,称量D装置及药品质量为201.32g。(原装置中的空气对实验结果的影响忽略不计)。
实验结论:
(4)根据以上实验可知:图4中A装置的作用是
【实验反思】
①由于Vc泡腾片投入水中会迅速产生大量二氧化碳,直接服用易导致腹胀,腹痛甚至置肠穿孔,所以应先用水溶解摇匀后再服用;
②服用Vc泡腾片请遵医喝。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】在一次化学课上,老师将几滴酚酞试液滴入氢氧化钠溶液中,溶液奇迹般地变红色。
【提出问题】在NaOH溶液中究竟哪种粒子使酚酞试液变红呢?
【查阅资料】NaOH溶液中存在粒子有:H2O、Na+、OH-。
【小凯猜想】①使酚酞试液变红色的是H2O;②使酚酞试液变红色的是Na+;③使酚酞试液变红色的是OH-。
【实验探究1】制三朵用酚酞试液染成无色的干燥纸花,按如图实验进行操作。

仔细观察上述实验,请回答:
(1)实验(Ⅰ)、(Ⅱ)证实______ 。
(2)猜想______ 成立(填序号)。
【思考】做完探究实验后,小凯同学欣喜异常,马上联想到氨气和氨水是否也能使酚酞试液变红呢?
【查阅资料】实验室常采用加热固体氢氧化钙和氯化铵的混合物来制取氨气;氨气极易溶于水,常温下,1体积水能吸收700体积的氨气,密度比空气小.
【实验探究2】制取氨气
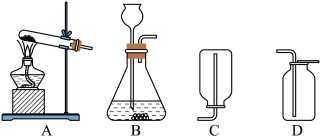
(3)请你从以上装置中选择适合制取氨气的发生装置______ (填字母);收集装置______ (填字母);
(4)小凯同学又制两朵用酚酞试液染成无色的干燥纸花,按如图进行实验探究。

观察发现:(一)中纸花不变色,(二)中纸花变红,请回答下列问题:
通过(一)、(二)实验得出的结论是______ 。
【实验探究3】小凯同学探究欲望持续上升,于是设计了以下装置:用甲、乙两套装置进行如下实验:胶头滴管吸取某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管,一段时间后两装置中气球明显胀大.
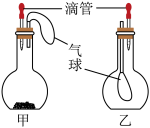
(5)你认为甲装置中滴管和烧瓶所取的试剂是______ ;所发生反应的化学方程式是______ 。
(6)若乙胶头滴管中吸入的是水,则乙烧瓶中应充入的气体是______ 。
【提出问题】在NaOH溶液中究竟哪种粒子使酚酞试液变红呢?
【查阅资料】NaOH溶液中存在粒子有:H2O、Na+、OH-。
【小凯猜想】①使酚酞试液变红色的是H2O;②使酚酞试液变红色的是Na+;③使酚酞试液变红色的是OH-。
【实验探究1】制三朵用酚酞试液染成无色的干燥纸花,按如图实验进行操作。

仔细观察上述实验,请回答:
(1)实验(Ⅰ)、(Ⅱ)证实
(2)猜想
【思考】做完探究实验后,小凯同学欣喜异常,马上联想到氨气和氨水是否也能使酚酞试液变红呢?
【查阅资料】实验室常采用加热固体氢氧化钙和氯化铵的混合物来制取氨气;氨气极易溶于水,常温下,1体积水能吸收700体积的氨气,密度比空气小.
【实验探究2】制取氨气

(3)请你从以上装置中选择适合制取氨气的发生装置
(4)小凯同学又制两朵用酚酞试液染成无色的干燥纸花,按如图进行实验探究。

观察发现:(一)中纸花不变色,(二)中纸花变红,请回答下列问题:
通过(一)、(二)实验得出的结论是
【实验探究3】小凯同学探究欲望持续上升,于是设计了以下装置:用甲、乙两套装置进行如下实验:胶头滴管吸取某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管,一段时间后两装置中气球明显胀大.

(5)你认为甲装置中滴管和烧瓶所取的试剂是
(6)若乙胶头滴管中吸入的是水,则乙烧瓶中应充入的气体是
您最近一年使用:0次



