化学就在我们身边,化学与生产、生活息息相关。
(1)生活中的下列做法不正确的是 (填字母)。
(2)正常雨水的pH约为5.6,其原因是_______ (用化学方程式表示)。
(3)氯化钠是生活中常见的盐。为除去氯化钠中的泥沙和( )杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按以下流程进行实验探究。
)杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按以下流程进行实验探究。_______ (写出两种)。
②加入 溶液时反应的化学方程式为
溶液时反应的化学方程式为_______ 。(提示:微溶物不形成沉淀)
③加入稀盐酸的作用是_______ 。
(4)下图为实验室模拟炼铁的实验装置。_______ 。
②已知集气瓶中盛放过量的氢氧化钠溶液,请设计实验证明实验后溶液中所含溶质的成分_______ 。(简要写出实验步骤、现象和结论)
(5)海水制“碱” v(Na2CO3)中含有少量的氯化钠。向盛有12g该“碱”样品的烧杯中加入足量的水充分溶解后,再加入过量的盐酸,充分反应后释放出二氧化碳4.4g。请计算该“碱”样品中碳酸钠质量分数是多少?(计算结果保留为0.1%)
(1)生活中的下列做法不正确的是 (填字母)。
| A.用甲醛溶液浸泡海鲜食品 |
| B.用洗涤剂除去餐具上的油污 |
| C.用食醋清洗水壶中的水垢 |
| D.用含碳酸氢钠的发酵粉焙制糕点 |
(2)正常雨水的pH约为5.6,其原因是
(3)氯化钠是生活中常见的盐。为除去氯化钠中的泥沙和(
 )杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按以下流程进行实验探究。
)杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按以下流程进行实验探究。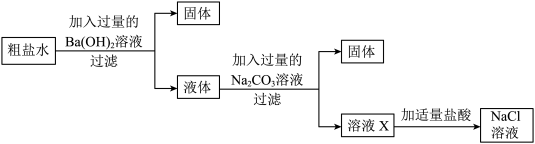
②加入
 溶液时反应的化学方程式为
溶液时反应的化学方程式为③加入稀盐酸的作用是
(4)下图为实验室模拟炼铁的实验装置。
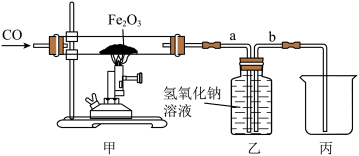
②已知集气瓶中盛放过量的氢氧化钠溶液,请设计实验证明实验后溶液中所含溶质的成分
(5)海水制“碱” v(Na2CO3)中含有少量的氯化钠。向盛有12g该“碱”样品的烧杯中加入足量的水充分溶解后,再加入过量的盐酸,充分反应后释放出二氧化碳4.4g。请计算该“碱”样品中碳酸钠质量分数是多少?(计算结果保留为0.1%)
更新时间:2024-05-16 18:41:57
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】同学们对实验“煅烧石灰石”展开深入探究。资料:石灰石中的杂质高温不分解。
①为证明石灰石已分解,三位同学设计方案如下:
I.甲同学按图一进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式___________________ 。

II.乙同学按图二进行试验,观察到B中液体变________ 色,A实验的作用是___________ 。
III.大家认为甲同学的方案不合理,请分析原因________________ 。
IV.丙同学取一块质量为12.5g的石灰石煅烧,并记录有关数据如下表
根据上述数据判断,___________ 秒时,已经可以证明石灰石开始分解了。240秒时,石灰石已经完全分解了,理由是 _______________ 。
②根据丙同学记录的数据,该石灰石分解共生成_______ 克CO2,物质的量为________ mol。根据化学方程式列式计算:这块石灰石中含碳酸钙的质量是________ 克。
①为证明石灰石已分解,三位同学设计方案如下:
I.甲同学按图一进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式

II.乙同学按图二进行试验,观察到B中液体变
III.大家认为甲同学的方案不合理,请分析原因
IV.丙同学取一块质量为12.5g的石灰石煅烧,并记录有关数据如下表
| 时间(秒) | 0 | 60 | 120 | 180 | 240 | 300 |
| 固体质量(克) | 12.5 | 12.3 | 11.2 | 9.2 | 8.1 | 8.1 |
②根据丙同学记录的数据,该石灰石分解共生成
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组决定以“碱的性质”开展项目式学习.
【任务一】认识碱溶液
(1)该小组同学向氢氧化钠溶液中滴加紫色石蕊溶液,发现溶液变为______________ 色,说明氢氧化钠溶液显碱性.
【任务二】探究碱的化学性质

(2)该小组同学分别向盛有氢氧化钠溶液和氢氧化钙溶液的试管中通入二氧化碳气体,发现其中一支试管中出现了较为明显的实验现象,请写出此试管中发生反应的化学方程式______________ .
(3)该小组同学向滴有酚酞试液的氢氧化钠溶液中通入二氧化碳气体,发现溶液仍为红色,原因是______________ .可另一小组的同学按下图装置进行实验时,却发现试管中溶液的红色褪去了,请你帮助他们分析原因:____________________________ .
【任务三】归纳碱的性质
(4)不同的碱,如氢氧化钠、氢氧化钙等,之所以有相似的化学性质,是因为它们在水溶液中都可以解离出相同的______________ (填符号).
【任务四】运用碱的性质
该兴趣小组在相同条件下,将 下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表.
下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表.
(5)某同学取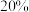 的氢氧化钠溶液
的氢氧化钠溶液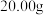 ,敞口放置一段时间后部分变质,得到
,敞口放置一段时间后部分变质,得到 溶液,由此能否计算所得溶液中溶质组成?
溶液,由此能否计算所得溶液中溶质组成?______________ .若能,请计算其组成;若不能,请补充完成实验方案设计,同时说明需要测定的数据(用a表示),并计算a的取值范围.(不要求写出计算过程)____
【任务一】认识碱溶液
(1)该小组同学向氢氧化钠溶液中滴加紫色石蕊溶液,发现溶液变为
【任务二】探究碱的化学性质

(2)该小组同学分别向盛有氢氧化钠溶液和氢氧化钙溶液的试管中通入二氧化碳气体,发现其中一支试管中出现了较为明显的实验现象,请写出此试管中发生反应的化学方程式
(3)该小组同学向滴有酚酞试液的氢氧化钠溶液中通入二氧化碳气体,发现溶液仍为红色,原因是
【任务三】归纳碱的性质
(4)不同的碱,如氢氧化钠、氢氧化钙等,之所以有相似的化学性质,是因为它们在水溶液中都可以解离出相同的
【任务四】运用碱的性质
该兴趣小组在相同条件下,将
 下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表.
下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中物质质量随时间变化如下表.| 时间 | 质量/g | |||||
| 水 | 饱和石灰水 | 稀盐酸 | 浓硫酸 | 氢氧化钠浓溶液 | 氯化钙溶液 | |
| 1天 | 8.16 | 8.37 | 8.64 | 11.18 | 9.38 | 10.25 |
| 2天 | 5.76 | 5.94 | 6.69 | 12.55 | 8.47 | 10.33 |
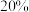 的氢氧化钠溶液
的氢氧化钠溶液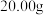 ,敞口放置一段时间后部分变质,得到
,敞口放置一段时间后部分变质,得到 溶液,由此能否计算所得溶液中溶质组成?
溶液,由此能否计算所得溶液中溶质组成?
您最近一年使用:0次
【推荐3】二氧化碳是一种与人类生产、生活有密切关系的气体,某校兴趣小组进行了和二氧化碳相关的研究和实验。
【活动一】
向试管中加入 蒸馏水,滴入1-2滴石蕊溶液,按图Ⅰ、Ⅱ、Ⅲ依次进行实验。
蒸馏水,滴入1-2滴石蕊溶液,按图Ⅰ、Ⅱ、Ⅲ依次进行实验。

(1)在观察溶液颜色变化过程中,还需要的操作是
(2)Ⅱ中试管内(除石蕊外)含有的物质有
(3)Ⅲ中观察到的实验现象是
【活动二】
(4)如下图所示,将一个充满二氧化碳的试管倒立在盛有澄清石灰水的烧杯中,可以观察到的现象是
(5)该实验

【活动迁移】
(6)资料一:第24届冬奥会于2022年2月4日在北京隆重举行,本届冬奥会体现了绿色办奥的理念。冬奥会速滑馆“冰丝带”制冰采用了世界上最先进的二氧化碳跨临界直冷制冰技术。固态二氧化碳叫做
(7)资料二:火星上含有丰富的二氧化碳和镁资源。科学家设想,镁可作为未来火星上的燃料,因为镁能在二氧化碳中燃烧放出大量的热,同时生成氧化镁和碳。该反应的化学方程式为
(8)资料三:科学家利用太阳能,以
 为原料制取炭黑(C)的简易流程如下图所示。请从环保角度谈一谈这项发明的意义
为原料制取炭黑(C)的简易流程如下图所示。请从环保角度谈一谈这项发明的意义
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】从古至今,CO2一直被人类广泛应用。
一、CO2的发现
(1)西晋张华著作《博物志》记载:“烧白石作白灰 ……”,同时分解生成了CO2。白石主要成分同石灰石,白灰主要成分CaO。该反应的化学方程式为______ 。
(2)17世纪初,海尔蒙特发现木炭燃烧后不仅有灰烬,还有不可见的气体产生,他将该气体命名为“森林之精”。烛火在该气体中会熄灭,这说明该气体具有______ 的化学性质。
二、CO2的吸收、应用
(3)CO2吸收:自然界有多种途径吸收CO2。
①绿色植物通过______ 吸收CO2。
②风化岩石中的CaCO3粉末可吸收空气中的CO2和H2O转化为Ca(HCO3)2,该反应的化学方程式为______ 。
(4)CO2的捕捉:利用氨水(NH3·H2O)捕捉CO2,得到高纯度CO2的流程如下

①吸收塔中NH3•H2O常采用雾状喷淋技术,其目的是______ 。
②再生塔中发生反应的化学方程式为______ 。
(5)回收的CO2与H2在催化剂、高温条件下合成甲醇(CH4O)同时生成水。该反应的化学方程式为______ 。
三、CO2的含量测定
m g甲醇与一定量O2置于密闭容器内充分反应,发生的反应如下: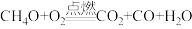
【资料】
1、无水硫酸铜遇水变蓝
2、氢氧化钠溶液不吸收CO,能充分吸收CO2
3、浅绿色氯化亚铜溶液吸收CO生成红色固体Cu2Cl2(CO)2•2H2O
【实验】
(6)连接好装置,______ (填一实验操作步骤)。将生成的气体通入下图装置

【现象】
(7)实验中观察到A装置中固体变蓝,说明有______ 生成;C中出现______ (填现象),说明CO生成。B、C装置都增重,增重的质量总和为ag。
【数据】充分吸收生成的气体后测定,A装置增重3.6g
【计算】
(8)计算下列数值:
①m=______ g ;
②a 的取值范围是2.8g<a g<______ g(结果保留到0.1g,下同)。
③若a=3.6,则生成气体中CO2 的质量为______ g。
一、CO2的发现
(1)西晋张华著作《博物志》记载:“烧白石作白灰 ……”,同时分解生成了CO2。白石主要成分同石灰石,白灰主要成分CaO。该反应的化学方程式为
(2)17世纪初,海尔蒙特发现木炭燃烧后不仅有灰烬,还有不可见的气体产生,他将该气体命名为“森林之精”。烛火在该气体中会熄灭,这说明该气体具有
二、CO2的吸收、应用
(3)CO2吸收:自然界有多种途径吸收CO2。
①绿色植物通过
②风化岩石中的CaCO3粉末可吸收空气中的CO2和H2O转化为Ca(HCO3)2,该反应的化学方程式为
(4)CO2的捕捉:利用氨水(NH3·H2O)捕捉CO2,得到高纯度CO2的流程如下

①吸收塔中NH3•H2O常采用雾状喷淋技术,其目的是
②再生塔中发生反应的化学方程式为
(5)回收的CO2与H2在催化剂、高温条件下合成甲醇(CH4O)同时生成水。该反应的化学方程式为
三、CO2的含量测定
m g甲醇与一定量O2置于密闭容器内充分反应,发生的反应如下:
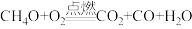
【资料】
1、无水硫酸铜遇水变蓝
2、氢氧化钠溶液不吸收CO,能充分吸收CO2
3、浅绿色氯化亚铜溶液吸收CO生成红色固体Cu2Cl2(CO)2•2H2O
【实验】
(6)连接好装置,

【现象】
(7)实验中观察到A装置中固体变蓝,说明有
【数据】充分吸收生成的气体后测定,A装置增重3.6g
【计算】
(8)计算下列数值:
①m=
②a 的取值范围是2.8g<a g<
③若a=3.6,则生成气体中CO2 的质量为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】氯化钠在工农业上具有广泛的用途。
(1)侯德榜是我国著名的化工专家,对世界纯碱工业的发展作出了突出贡献,纯碱属于_____ (填“酸”、“碱”或“盐”)。制备纯碱的原料是氯化钠、氨气、二氧化碳和水,反应首先生成小苏打和一种氮肥,试写出该步反应的化学方程式:___________ 。
(2)配制500 mL质量分数6%的氯化钠溶液(密度1.04 g/cm3),需要氯化钠的质量为_______ g。
(3)用托盘天平称量所需氯化钠,托盘天平调节平衡后,接下来的操作顺序是______ 。
A.先在左盘纸片上加氯化钠,后在右盘纸片上加砝码和移动游码
B.先在右盘纸片上加砝码和移动游码,后在左盘纸片上加氯化钠
(4)若用质量分数为6%的氯化钠溶液配制100 g质量分数为4%的氯化钠溶液。
①需要6%的氯化钠溶液的质量为_________ g(精确到0.1 g)。
②该溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要的玻璃仪器是_____________ 。
(1)侯德榜是我国著名的化工专家,对世界纯碱工业的发展作出了突出贡献,纯碱属于
(2)配制500 mL质量分数6%的氯化钠溶液(密度1.04 g/cm3),需要氯化钠的质量为
(3)用托盘天平称量所需氯化钠,托盘天平调节平衡后,接下来的操作顺序是
A.先在左盘纸片上加氯化钠,后在右盘纸片上加砝码和移动游码
B.先在右盘纸片上加砝码和移动游码,后在左盘纸片上加氯化钠
(4)若用质量分数为6%的氯化钠溶液配制100 g质量分数为4%的氯化钠溶液。
①需要6%的氯化钠溶液的质量为
②该溶液配制过程中除用到量筒、玻璃棒和胶头滴管外,还需要的玻璃仪器是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】盐类物质是生活中常见的重要化合物,用途广泛。请按要求完成以下探究活动。
(1)根据日常生活经验推测,玉米地的玉米苗叶子发黄,应及时施加的化学肥料是______(填序号)。
(2)盐中含有金属离子(或 )和酸根离子,组成相似的盐具有一些相似的化学性质。
)和酸根离子,组成相似的盐具有一些相似的化学性质。
①硫酸铜、硝酸铜两种物质的溶液均显______ 色,因为它们都具有相同的阳离子:向这两种物质的溶液中分别加入NaOH溶液,有相同的实验现象发生,写出其中一个反应的化学方程式______ 。
②向硫酸铜、硝酸铜两种物质的溶液中分别加入BaC12溶液,能发生反应的物质是______ (填化学式),另外一种物质不反应。
(3)某无色溶液可能由氢氧化钠溶液、氯化钠溶液、碳酸钠溶液中的一种或几种混合而成。为探究其组成,小华同学进行了如下实验:取适量样品放入试管中,滴加酚酞溶液,溶液变红,再向试管中逐滴加入过量的氯化钙溶液,观察到有沉淀产生,过滤后滤液仍为红色。
根据实验现象回答:
①产生沉淀的化学方程式为______ 。
②该样品中一定含有的物质是______ ,可能含有的物质是______ 。(填化学式)
(4)食用纯碱中常含有少量氯化钠。现取某食用纯碱样品10g,加入一定量稀盐酸恰好完全反应,同时产生了2.2g气体,试计算该食用纯碱中碳酸钠的质量分数。
(1)根据日常生活经验推测,玉米地的玉米苗叶子发黄,应及时施加的化学肥料是______(填序号)。
| A.氯化钾 | B.硝酸铵 | C.过磷酸钙 |
 )和酸根离子,组成相似的盐具有一些相似的化学性质。
)和酸根离子,组成相似的盐具有一些相似的化学性质。①硫酸铜、硝酸铜两种物质的溶液均显
②向硫酸铜、硝酸铜两种物质的溶液中分别加入BaC12溶液,能发生反应的物质是
(3)某无色溶液可能由氢氧化钠溶液、氯化钠溶液、碳酸钠溶液中的一种或几种混合而成。为探究其组成,小华同学进行了如下实验:取适量样品放入试管中,滴加酚酞溶液,溶液变红,再向试管中逐滴加入过量的氯化钙溶液,观察到有沉淀产生,过滤后滤液仍为红色。
根据实验现象回答:
①产生沉淀的化学方程式为
②该样品中一定含有的物质是
(4)食用纯碱中常含有少量氯化钠。现取某食用纯碱样品10g,加入一定量稀盐酸恰好完全反应,同时产生了2.2g气体,试计算该食用纯碱中碳酸钠的质量分数。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】酸、碱、盐是九年级化学学习的重要知识,它们具有广泛的用途。
(1)下列关于酸、碱、盐在生产或生活中应用的说法,不合理 的是______ 。
a.可用稀硫酸除铁锈 b.烧碱显碱性,可改良酸性土壤
c.用氯化钠配制生理盐水 d.服用小苏打可治疗胃酸过多症
(2)不同酸具有相似的化学性质,原因是酸在水溶液中都能解离出______ ;但由于不同的酸在水溶液中解离出的酸根离子不同,化学性质也存在差异,如可利用______ 溶液区分稀盐酸和稀硫酸。
(3)向盛有碳酸钠溶液的烧杯中加入少量氢氧化钙固体,充分搅拌后过滤,得到固体和溶液,同学们对固体和溶液中含有的物质进行了如下探究:
①取少量固体于试管中加水振荡,静置后试管底部有固体,向上层清液中滴加酚酞溶液,无明显现象,向试管中滴加稀盐酸,固体溶解并产生气泡。写出反应的化学方程式:______ ;
②请设计实验,证明溶液中含有碳酸钠和氢氧化钠______ 。(写出实验操作和现象)
(4)为减少污染和节约成本,化学小组探究从含有(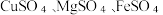 的废液中回收
的废液中回收  和有关金属,实验过程如下图。
和有关金属,实验过程如下图。

①写出一个向废液中加入过量镁粉时发生反应的化学方程式:______ ;
②理论上最终得到的硫酸镁晶体的质量______ (填“大于”“小于”或“等 于”)原废液中硫酸镁的质量。
(5)农业生产上常用一定溶质质量分数的氯化钠溶液进行选种。实验小组取某选种溶液7g,向其中滴加硝酸银溶液至不再产生沉淀,经过滤、洗涤、干燥后,称得沉淀质量为2.87g。计算该溶液中氯化钠的溶质的质量分数。(结果精确到0.1%)
(1)下列关于酸、碱、盐在生产或生活中应用的说法,
a.可用稀硫酸除铁锈 b.烧碱显碱性,可改良酸性土壤
c.用氯化钠配制生理盐水 d.服用小苏打可治疗胃酸过多症
(2)不同酸具有相似的化学性质,原因是酸在水溶液中都能解离出
(3)向盛有碳酸钠溶液的烧杯中加入少量氢氧化钙固体,充分搅拌后过滤,得到固体和溶液,同学们对固体和溶液中含有的物质进行了如下探究:
①取少量固体于试管中加水振荡,静置后试管底部有固体,向上层清液中滴加酚酞溶液,无明显现象,向试管中滴加稀盐酸,固体溶解并产生气泡。写出反应的化学方程式:
②请设计实验,证明溶液中含有碳酸钠和氢氧化钠
(4)为减少污染和节约成本,化学小组探究从含有(
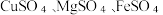 的废液中回收
的废液中回收  和有关金属,实验过程如下图。
和有关金属,实验过程如下图。
①写出一个向废液中加入过量镁粉时发生反应的化学方程式:
②理论上最终得到的硫酸镁晶体的质量
(5)农业生产上常用一定溶质质量分数的氯化钠溶液进行选种。实验小组取某选种溶液7g,向其中滴加硝酸银溶液至不再产生沉淀,经过滤、洗涤、干燥后,称得沉淀质量为2.87g。计算该溶液中氯化钠的溶质的质量分数。(结果精确到0.1%)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】中国承诺在2030年前实现碳达峰,2060年前实现碳中和。请回答下列问题。
(1)“碳”排放:CO2主要来源是化石燃料的燃烧,化石燃料是______ (填“可”或“不可”)再生能源。
(2)“碳”制取:以下是实验室制取气体的常用装置

①写出A装置中的反应原理________ 。
②想要制取纯净、干燥的CO2,装置从左到右依次连接顺序为:A→B→C→D,写出C装置中的试剂名称_______ 。
(3)“碳”捕集:如图是工业上利用NaOH溶液“捕集”CO2的主要技术流程

①吸收器中NaOH溶液采用喷淋方式加入,其优点是_______ ,发生反应的化学方程式是_______ ;整个流程中,可以循环利用的物质是________ 。
②实验室除去CO2也常采用碱液吸收法,请设计实验探究足量NaOH溶液吸收CO2后溶液中溶质成分:__________ 。(简要叙述实验步骤、现象和结论)
(4)“碳”计算:我国研发的“液态太阳燃料合成技术”,在一定条件下,二氧化碳和氢气可以转化为“液态阳光燃料”甲醇(CH3OH),同时生成水。若产生4.8kg甲醇,理论上消耗二氧化碳的质量是多少?
(1)“碳”排放:CO2主要来源是化石燃料的燃烧,化石燃料是
(2)“碳”制取:以下是实验室制取气体的常用装置

①写出A装置中的反应原理
②想要制取纯净、干燥的CO2,装置从左到右依次连接顺序为:A→B→C→D,写出C装置中的试剂名称
(3)“碳”捕集:如图是工业上利用NaOH溶液“捕集”CO2的主要技术流程

①吸收器中NaOH溶液采用喷淋方式加入,其优点是
②实验室除去CO2也常采用碱液吸收法,请设计实验探究足量NaOH溶液吸收CO2后溶液中溶质成分:
(4)“碳”计算:我国研发的“液态太阳燃料合成技术”,在一定条件下,二氧化碳和氢气可以转化为“液态阳光燃料”甲醇(CH3OH),同时生成水。若产生4.8kg甲醇,理论上消耗二氧化碳的质量是多少?
您最近一年使用:0次
【推荐3】2021年世界环境日主题为生态系统恢复(Ecosystem Restoration)
(1)下列属于空气污染物的是_____ 。
a、二氧化硫 b、一氧化碳 c、二氧化氮 d、可吸入颗粒物
(2)下列措施能减少或控制汽车尾气对空气污染的是_____ 。
a.汽车改用压缩天然气为燃料
b.开发清洁能源汽车,如太阳能汽车
c.改进发动机的燃烧方式,使汽油能充分燃烧
d.使用含铅汽油
(3)在汽油中加入适量乙醇作为汽车燃料,能在一定程度上减少汽车尾气的污染。写出乙醇充分燃烧的化学方程式为___________ 。
(4)含氮化合物是重要的化工原料。
①氨气是由_____ (填“分子”、“原子”或“离子”)构成的。
②氨气溶于水显碱性,是因为氨气与水反应生成了碱,请写出这种碱的化学式_____ 。
③NH4NO3是一种重要的氮肥。已知NH4NO3和KCl固体混合物中氮元素的质量分数为28%,则混合物中KCl的质量分数为_____ 。
④请完成鉴别氯化铵和硝酸铵两种溶液的实验报告。
(1)下列属于空气污染物的是
a、二氧化硫 b、一氧化碳 c、二氧化氮 d、可吸入颗粒物
(2)下列措施能减少或控制汽车尾气对空气污染的是
a.汽车改用压缩天然气为燃料
b.开发清洁能源汽车,如太阳能汽车
c.改进发动机的燃烧方式,使汽油能充分燃烧
d.使用含铅汽油
(3)在汽油中加入适量乙醇作为汽车燃料,能在一定程度上减少汽车尾气的污染。写出乙醇充分燃烧的化学方程式为
(4)含氮化合物是重要的化工原料。
①氨气是由
②氨气溶于水显碱性,是因为氨气与水反应生成了碱,请写出这种碱的化学式
③NH4NO3是一种重要的氮肥。已知NH4NO3和KCl固体混合物中氮元素的质量分数为28%,则混合物中KCl的质量分数为
④请完成鉴别氯化铵和硝酸铵两种溶液的实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】2022年2月,第24届冬奥会在北京举办。冬奥吉祥物“冰墩墩”因其造型可爱遭到世人疯抢,造成“一墩难求”现象。同学们利用寒假时间,对“冰墩墩”外壳材料进行探究:
【查阅资料】
Ⅰ.它的硅胶外壳采用了环保PVC(聚氯乙烯)及PC(聚碳酸酯)制作而成。
Ⅱ.环保PVC在一般PVC的基础上添加了助剂和矿粉填料,使它更稳定且耐腐蚀,还剔除了材料中的重金属元素。
Ⅲ. PC(聚碳酸酯)的组成元素有C、H、O三种。
【进行实验】
为测定PC(聚碳酸酯)的化学式,同学们设计了如图所示实验装置:
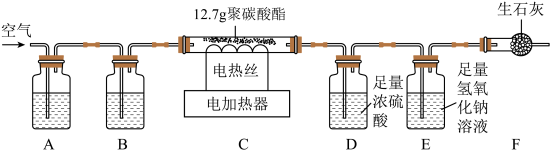
将12.7g聚碳酸酯放在装置C的玻璃管中,燃烧至无固体成分残留。
(1)装置A、B中盛放的试剂分别是_____ (填序号)。
a.足量NaOH溶液、足量浓硫酸b.足量浓硫酸、足量NaOH溶液
(2)装置F的目的是吸收从装置E的气流中带出来的少量水蒸气,生石灰与水蒸气发生反应的化学方程式是_____ 。
【记录数据】
加热前先通入空气一段时间,再称量装置D的质量、装置E和F的总质量(反应前的质量)。聚碳酸酯完全反应后,停止加热,继续通入空气一段时间,再次称量装置D的质量、装置E和F的总质量(反应后的质量)。实验数据如下表所示:
【实验结论】
(3)根据表中数据,得出聚碳酸酯中碳、氢、氧元素的质量比是_____ ,并仿照聚乙烯的化学式(C2H4)n,写出聚碳酸酯的化学式为_____ 。
【实验反思】
(4)实验过程中,加热前要先通入空气一段时间,该操作的作用是_____ 。
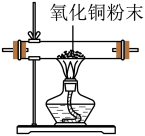
(5)有同学建议,为使实验结果更准确,需要在装置C和D之间增加图所示的装置,其目的是_____ 。
【交流讨论】
(6)鉴别一般PVC(聚氯乙烯)和PE(聚乙烯)的方法、现象和结论是_____ 。
(7)由于重金属盐易使_____ ,所以在生产环保PVC时需要将其剔除,以免造成环境污染。
【查阅资料】
Ⅰ.它的硅胶外壳采用了环保PVC(聚氯乙烯)及PC(聚碳酸酯)制作而成。
Ⅱ.环保PVC在一般PVC的基础上添加了助剂和矿粉填料,使它更稳定且耐腐蚀,还剔除了材料中的重金属元素。
Ⅲ. PC(聚碳酸酯)的组成元素有C、H、O三种。
【进行实验】
为测定PC(聚碳酸酯)的化学式,同学们设计了如图所示实验装置:

将12.7g聚碳酸酯放在装置C的玻璃管中,燃烧至无固体成分残留。
(1)装置A、B中盛放的试剂分别是
a.足量NaOH溶液、足量浓硫酸b.足量浓硫酸、足量NaOH溶液
(2)装置F的目的是吸收从装置E的气流中带出来的少量水蒸气,生石灰与水蒸气发生反应的化学方程式是
【记录数据】
加热前先通入空气一段时间,再称量装置D的质量、装置E和F的总质量(反应前的质量)。聚碳酸酯完全反应后,停止加热,继续通入空气一段时间,再次称量装置D的质量、装置E和F的总质量(反应后的质量)。实验数据如下表所示:
| 装置 | 反应前的质量/g | 反应后的质量/g |
| D | 80 | 86.3 |
| E和F | 70 | 105.2 |
(3)根据表中数据,得出聚碳酸酯中碳、氢、氧元素的质量比是
【实验反思】
(4)实验过程中,加热前要先通入空气一段时间,该操作的作用是
(5)有同学建议,为使实验结果更准确,需要在装置C和D之间增加图所示的装置,其目的是

【交流讨论】
(6)鉴别一般PVC(聚氯乙烯)和PE(聚乙烯)的方法、现象和结论是
(7)由于重金属盐易使
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
【推荐2】世界上的物质丰富多样,有些物质能危害健康,现代社会中,毒品的危害并未完全消除,工农业生产带来的污染依然存在,香烟的产销量依然巨大.“珍爱生命,远离有毒物质”,是我们的一种生活理念,保护环境,建设和谐社会,实现“中国梦”,则是每个公民的责任。

(1)1839年6月,在广州虎门,著名民族英雄林则徐将二百多万斤英国走私鸦片全部销毁,显示了中华民族反对侵略和坚决禁毒的坚强意志。当年销烟的方法是在海滩上挖池,池中注水,且放入____ (填“烧碱”“纯碱”“石灰石”“生石灰”之一),再将鸦片倒入池中销毁。
(2)鸦片的主要成分罂粟碱(化学视为C20H21O4N)中,C,O两种元素的原子个数之比为____ (填最简整数比)。
(3)近期,关于某地农户使用剧毒农药“神农丹”进行大姜种植的报道引人注目。“神农丹”的主要成分是涕灭威(化学式为C7H14O2N2S),在涕灭威中,所含元素质量分数最小的元素是____ 。
(4)香烟中的尼古丁(化学式为C10H14N2)是一种剧毒物质,下列有关说法中,不正确的是_____ ;①吸烟能使人产生依赖性;②尼古丁的相对分子质量为162;③被动吸烟无害健康;④香烟中的尼古丁能诱发癌变;⑤吸烟能防治H7N9禽流感;
A 只有①⑤ B 只有②④ C 只有②③ D 只有③⑤

(1)1839年6月,在广州虎门,著名民族英雄林则徐将二百多万斤英国走私鸦片全部销毁,显示了中华民族反对侵略和坚决禁毒的坚强意志。当年销烟的方法是在海滩上挖池,池中注水,且放入
(2)鸦片的主要成分罂粟碱(化学视为C20H21O4N)中,C,O两种元素的原子个数之比为
(3)近期,关于某地农户使用剧毒农药“神农丹”进行大姜种植的报道引人注目。“神农丹”的主要成分是涕灭威(化学式为C7H14O2N2S),在涕灭威中,所含元素质量分数最小的元素是
(4)香烟中的尼古丁(化学式为C10H14N2)是一种剧毒物质,下列有关说法中,不正确的是
A 只有①⑤ B 只有②④ C 只有②③ D 只有③⑤
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
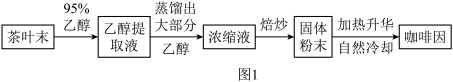
【推荐3】阅读下面科普短文中国是“茶之国”,喝茶已有四千多年的历史。茶叶中含有多种生物碱,咖啡因( )是其中之一,咖啡因具有刺激心脏、促进血液循环及兴奋大脑等作用。从茶叶中提取咖啡因的过程,如图1。
)是其中之一,咖啡因具有刺激心脏、促进血液循环及兴奋大脑等作用。从茶叶中提取咖啡因的过程,如图1。
咖啡因能溶于水,可使用分光光度法比较不同茶叶水提物中咖啡因的含量,结果如表1。吸光度值越高,咖啡因含量越高。
表1 四种茶叶咖啡因吸光度值
实验人员使用信阳毛尖、控制茶叶与水的质量比为1:75进行其他研究,结果如图2、3。咖啡摄入过多容易刺激胃肠道,引起骨质疏松等,生活中应将其摄入量控制在合理范围内。
(1)图1中,获得浓缩液的过程发生的是_______ (填“物理”或“化学”)变化。
(2)由表1可知,咖啡因含量最低的茶叶是______ 。
(3)由图3得出的结论是:在使用信阳毛尖、______ 、_______ 、浸泡3min,浸泡次数4次内,随浸泡次数增加,茶水中咖啡因含量降低。
(4)判断下列说法是否正确(填“对”或“错”)。
①由图2可知,单次浸泡、浸泡时间相同时,温度在80~95°C范围内,浸泡温度越高,茶水中咖啡因含量越高______ 。
②咖啡因摄入过多对人体有害______ 。
 )是其中之一,咖啡因具有刺激心脏、促进血液循环及兴奋大脑等作用。从茶叶中提取咖啡因的过程,如图1。
)是其中之一,咖啡因具有刺激心脏、促进血液循环及兴奋大脑等作用。从茶叶中提取咖啡因的过程,如图1。咖啡因能溶于水,可使用分光光度法比较不同茶叶水提物中咖啡因的含量,结果如表1。吸光度值越高,咖啡因含量越高。
表1 四种茶叶咖啡因吸光度值
| 茶叶品种 | 铁观音 | 滇红茶 | 白毫银针 | 龙井 |
| 吸光度值 | 0.076 | 0.103 | 0.123 | 0.047 |

(1)图1中,获得浓缩液的过程发生的是
(2)由表1可知,咖啡因含量最低的茶叶是
(3)由图3得出的结论是:在使用信阳毛尖、
(4)判断下列说法是否正确(填“对”或“错”)。
①由图2可知,单次浸泡、浸泡时间相同时,温度在80~95°C范围内,浸泡温度越高,茶水中咖啡因含量越高
②咖啡因摄入过多对人体有害
您最近一年使用:0次



