水和溶液在生产、生活中具有广泛的用途。
(1)对天然水进行过滤_______ (填“能”或“不能”)降低水的硬度;自来水厂的吸附池中通常用_______ 吸附水中的一些可溶性杂质。
(2)电解水实验中,正极端玻璃管中产生的气体与负极端玻璃管中产生的气体依次为______ ;请说明水中加入少量硫酸钠能够增强导电性的原因_______ 。
(3)四种固体物质的溶解度数据表和溶解度曲线如表。
_______ (填名称)。
②60℃时,分别在50g水中加入25g表中的四种固体物质,充分搅拌。该条件下,_______ (填化学式,下同)形成的溶液是不饱和溶液,_______ 溶液中溶质的质量分数最小。
③将80℃时269gKNO3的饱和溶液和151.1gKCl的饱和溶液,分别降低温度到20℃,理论上析出KNO3固体的质量比析出KCl固体的质量多______ 。
(1)对天然水进行过滤
(2)电解水实验中,正极端玻璃管中产生的气体与负极端玻璃管中产生的气体依次为
(3)四种固体物质的溶解度数据表和溶解度曲线如表。
| 温度/℃ | 20 | 60 | 80 | |
| 溶解度/g | NaCl | 36.0 | 37.3 | 38.4 |
| KCl | 34.0 | 45.5 | 51.1 | |
| NH4Cl | 37.2 | 55.2 | 65.6 | |
| KNO3 | 31.6 | 110 | 169 | |
②60℃时,分别在50g水中加入25g表中的四种固体物质,充分搅拌。该条件下,
③将80℃时269gKNO3的饱和溶液和151.1gKCl的饱和溶液,分别降低温度到20℃,理论上析出KNO3固体的质量比析出KCl固体的质量多
2024·江苏南京·一模 查看更多[3]
2024年江苏省南京市秦淮区九年级化学一模试卷(已下线)押南京卷非选择题第18题 水和溶液-备战2024年中考化学临考题号押题(南京专用)(已下线)【临考满分卷】2024年中考化学临考满分卷(南京专用)
更新时间:2024-05-11 14:13:50
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,人类的日常生活与工农业生产都离不开水。

(1)如图 1 所示,通电一段时间后,试管 1 中所收集的气体为_______ ,用______ 检验该气体,该实验说明水是由______ 组成的。该反应的文字表达式是______ 。
(2)图 2 是用来净化天然水的简易装置,下面分析错误的是 (填序号)。
(3)图 3 是自来水厂的净水过程示意图,其中活性炭池的作用是_______ 。某同学检验所得自来水是否为硬水,他用的试剂是______ ,若看到_______ 现象为硬水。日常生活中,常用_______ 方法降低水的硬度。

(1)如图 1 所示,通电一段时间后,试管 1 中所收集的气体为
(2)图 2 是用来净化天然水的简易装置,下面分析错误的是 (填序号)。
| A.能杀菌消毒 | B.能得到纯净水 |
| C.能把硬水变为软水 | D.能使天然水变得无色澄清 |
(3)图 3 是自来水厂的净水过程示意图,其中活性炭池的作用是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题。
(1)如图是水通电分解过程中微粒变化的部分示意图,请按它们在化学变化过程中出现的顺序排列:______ (用图中的字母表示),反应的符号表达式是 ______ 。该实验的结论是:水是由 ______ 组成的。

(2)如图为六种原子的结构示意图。

请回答下列问题:
①图中六种元素之间的最本质区别是______ 。
②镁原子在化学反应中容易失去2个电子形成镁离子,镁离子的符号为______ 。
③从原子结构上分析,写出钙元素、氯元素组成化合物的化学式______ 。
④在上述碘的原子结构示意图中,X=______ 。
(3)X、Y、Z为初中化学中常见的三种元素。X的单质为密度最小的气体,Y的单质气体能使带火星的木条复燃,Z的单质通常是一种黄色固体,燃烧产生刺激性气味的气体,请回答下列问题:
①Z元素的名称为______ ,实验室用一种暗紫色固体制取Y单质,该反应的符号表达式是 ______ 。
②X和Y组成的一种液态化合物与一种黑色固态化合物,在常温下反应制取Y单质,该反应的符号表达式是______ 。
(1)如图是水通电分解过程中微粒变化的部分示意图,请按它们在化学变化过程中出现的顺序排列:

(2)如图为六种原子的结构示意图。

请回答下列问题:
①图中六种元素之间的最本质区别是
②镁原子在化学反应中容易失去2个电子形成镁离子,镁离子的符号为
③从原子结构上分析,写出钙元素、氯元素组成化合物的化学式
④在上述碘的原子结构示意图中,X=
(3)X、Y、Z为初中化学中常见的三种元素。X的单质为密度最小的气体,Y的单质气体能使带火星的木条复燃,Z的单质通常是一种黄色固体,燃烧产生刺激性气味的气体,请回答下列问题:
①Z元素的名称为
②X和Y组成的一种液态化合物与一种黑色固态化合物,在常温下反应制取Y单质,该反应的符号表达式是
您最近一年使用:0次
【推荐3】化学与能源、科技、环境密切相关。
(1)能源:H2被视为最理想的清洁能源,某实验小组用如图所示装置完成电解水的实验(所用试管规格相同),下列说法正确的是___________(填字母)。

(2)科技:我国科研人员开发出一种新型纳米纤维催化剂,应用于二氧化碳高效合成甲醇,其过程的微观示意图如图所示,参加反应的两种物质的分子个数比为___________ 。

(3)环境:为推进“双碳目标”的落实,科学家还利用氨气与二氧化碳反应制备尿素,化学方程式表示为 ,该反应涉及的有机物化学式为
,该反应涉及的有机物化学式为___________ ,其含碳量为___________ (只列出计算式)。
(1)能源:H2被视为最理想的清洁能源,某实验小组用如图所示装置完成电解水的实验(所用试管规格相同),下列说法正确的是___________(填字母)。

| A.直流电源a端应为正极 |
| B.a、b两极产生的气体质量比为1:8 |
| C.d试管中的气体先收集满 |
| D.该实验能证明水是由氢原子、氧原子构成的 |

(3)环境:为推进“双碳目标”的落实,科学家还利用氨气与二氧化碳反应制备尿素,化学方程式表示为
 ,该反应涉及的有机物化学式为
,该反应涉及的有机物化学式为
您最近一年使用:0次
【推荐1】下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
(1)从含有少量硝酸钾的氯化钠溶液中提纯出氯化钠,可采用的方法是_____ 。
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是_____ 。
(3)90 ℃时,将一定质量的KNO3溶液按图示进行操作:

90℃时的KNO3溶液是_____ (填“饱和”或“不饱和”)溶液。图中n的数值为_____ 。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | |
| 溶解度/g | NaCl | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38 | 38.5 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | 138 | 169 | 202 | |
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是
(3)90 ℃时,将一定质量的KNO3溶液按图示进行操作:

90℃时的KNO3溶液是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只含少量NaCl的KNO3固体药品。
(1)查阅KNO3和NaCl的溶解度曲线,如图。从图中可得到的一条信息是______________________________ ,50℃时,将85.5g固体药品溶于100g水中,得到的是KNO3的__________ (填“饱和”或“不饱和”)溶液,将KNO3提纯的方法是__________ 。

(2)上明用提纯后的KNO3固体配制1000g溶质质量分数为5%的KNO3溶液,其操作步骤是:计算、__________ 、__________ 、装瓶贴标签。经检测,小明所配溶液中KNO3溶质质量分数偏小,其原因可能是__________ 。
①KNO3固体仍然不纯 ②溶解前,烧杯中有少量水
③量取水时,俯视读数 ④装瓶时,有少量溶液洒出
(3)小红提出,也可用一定量20℃时31.6%的KNO3溶液稀释配制5%的溶液,你认为是否可行?_______ (填“行”或“不行”)。
(1)查阅KNO3和NaCl的溶解度曲线,如图。从图中可得到的一条信息是

(2)上明用提纯后的KNO3固体配制1000g溶质质量分数为5%的KNO3溶液,其操作步骤是:计算、
①KNO3固体仍然不纯 ②溶解前,烧杯中有少量水
③量取水时,俯视读数 ④装瓶时,有少量溶液洒出
(3)小红提出,也可用一定量20℃时31.6%的KNO3溶液稀释配制5%的溶液,你认为是否可行?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图所示为两种物质的溶解度曲线变化图。认真观察后请回答下列问题:

(1)50℃时,NaC1溶解度是________ ,20℃时,将10g氯化钠加入20g水中,充分溶解后所得溶液的质量分数为______ (保留一位小数);
(2)将20℃时,氯化钠和硝酸钾的恰好饱和的溶液升温到50℃,所得溶液溶质质量分数大小关系是:
_______ 
(3)根据溶解度曲线图可知:NaC1的结晶方法一般是_______ ,其原因是__________ 。

(1)50℃时,NaC1溶解度是
(2)将20℃时,氯化钠和硝酸钾的恰好饱和的溶液升温到50℃,所得溶液溶质质量分数大小关系是:


(3)根据溶解度曲线图可知:NaC1的结晶方法一般是
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
真题
【推荐2】A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:

(1)t2℃时,A、B、C三种物质溶解度的大小关系是_____ (用“A、B、C”和“>、<、=”表示)
(2)要使接近饱和的C溶液在保持溶质质量分数不变的情况下变成饱和溶液的方法是_____ 。
(3)将100g质量分数为30%的A溶液由t3℃降温至t1℃,降温后所得溶液中溶质的质量分数是_____ 。
(4)t3℃时,A、B、C三种物质的混合溶液中,A、B、C三种溶质的质量相等,将混合溶液在该温度下恒温蒸发溶剂,首先析出的物质是_____ 。

(1)t2℃时,A、B、C三种物质溶解度的大小关系是
(2)要使接近饱和的C溶液在保持溶质质量分数不变的情况下变成饱和溶液的方法是
(3)将100g质量分数为30%的A溶液由t3℃降温至t1℃,降温后所得溶液中溶质的质量分数是
(4)t3℃时,A、B、C三种物质的混合溶液中,A、B、C三种溶质的质量相等,将混合溶液在该温度下恒温蒸发溶剂,首先析出的物质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图是a、b、c三种物质的溶解度曲线,a与c溶解度曲线交于P点,据图回答问题:
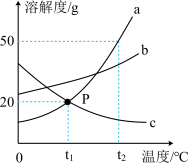
(1)P点的含义是______ 。t2℃时a、b、c三种物质溶解度由小到大的顺序______ 。
(2)从a的饱和溶液中结晶出a物质的方法是______ 。
(3)将t2℃时a、b、c三种物质饱和溶液的温度降到t1℃时,三种溶液中溶质的质量分数由大到小的排列是______ 。
(4)t2℃时,40ga物质加到50g水中不断搅拌,形成溶液的质量为______ g。

(1)P点的含义是
(2)从a的饱和溶液中结晶出a物质的方法是
(3)将t2℃时a、b、c三种物质饱和溶液的温度降到t1℃时,三种溶液中溶质的质量分数由大到小的排列是
(4)t2℃时,40ga物质加到50g水中不断搅拌,形成溶液的质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】图所示为a、b、c三种物质的溶解度曲线,回答下列问题:

(1)P点的含义是______ ;
(2)t2℃时,将30g的a物质加入到50g水中,搅拌,充分溶解后可得到_____ g的溶液;
(3)t1℃时,将c物质的饱和溶液升温到t2℃,此时溶液为______ (填“饱和”或 “不饱和”)溶液;
(4)将t2℃时的a、b、c三种物质的饱和溶液降温至t1℃,溶液中溶质质量分数由小到大的顺序是______ ;
(5)如果a溶液中混有少量的b,可采用______ 的方法将a提纯。

(1)P点的含义是
(2)t2℃时,将30g的a物质加入到50g水中,搅拌,充分溶解后可得到
(3)t1℃时,将c物质的饱和溶液升温到t2℃,此时溶液为
(4)将t2℃时的a、b、c三种物质的饱和溶液降温至t1℃,溶液中溶质质量分数由小到大的顺序是
(5)如果a溶液中混有少量的b,可采用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】分析下表中NaCI和KNO3的溶解度数据,回答相关问题。
(1)20°C时,NaCl 的溶解度为______ g。
(2)在NaCl和KNO3中溶解度受温度变化影响较大的是________ 。
(3)将10g NaCl和55g KNO3分别溶于相同质量的60°C的水后,再降温到20°C。
①要使55g KNO3完全溶解,至少需要_____ g 60°C的水;
②将上述两溶液均降温到20°C时,有晶体析出的是_______ 。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110.0 | 169.0 | 246.0 | |
(2)在NaCl和KNO3中溶解度受温度变化影响较大的是
(3)将10g NaCl和55g KNO3分别溶于相同质量的60°C的水后,再降温到20°C。
①要使55g KNO3完全溶解,至少需要
②将上述两溶液均降温到20°C时,有晶体析出的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
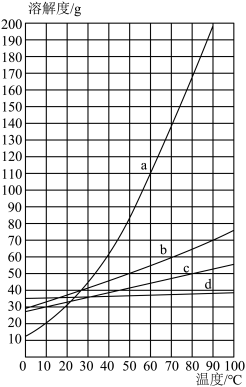
【推荐3】甲物质在水中的溶解度曲线如图,a、b、c、d为图像中的四个点。

(1)t1℃时,50g水中最多能溶解甲物质______ g。
(2)t2℃时,甲物质的溶解度是______ g。
(3)要使甲物质的饱和溶液成为不饱和溶液,可采用的一种方法是______ 。
(4)甲物质的溶液分别处于a、b、c、d四点时,溶液中甲物质的溶质质量分数大小关系正确的是______ (选填下列编号)。
Ⅰ、c>d=b>a Ⅱ、c=d>a=b Ⅲ、c>a>b=d IV、c>a=b>d
(5)若要得到溶质质量分数为30%以上的甲溶液,配制时的温度应不低于______ ℃。

(1)t1℃时,50g水中最多能溶解甲物质
(2)t2℃时,甲物质的溶解度是
(3)要使甲物质的饱和溶液成为不饱和溶液,可采用的一种方法是
(4)甲物质的溶液分别处于a、b、c、d四点时,溶液中甲物质的溶质质量分数大小关系正确的是
Ⅰ、c>d=b>a Ⅱ、c=d>a=b Ⅲ、c>a>b=d IV、c>a=b>d
(5)若要得到溶质质量分数为30%以上的甲溶液,配制时的温度应不低于
您最近一年使用:0次




