化学研究性学习活动小组的同学为测定某种“碳酸钙D3”药片中碳酸钙的含量是否与标签相符(图1是标签的部分信息),进行了如下实验:取8片药片,研碎后逐渐加入质量分数为 的稀盐酸,充分反应,实验相关数据如图2所示(假设其他成分不参加反应)。
的稀盐酸,充分反应,实验相关数据如图2所示(假设其他成分不参加反应)。 的稀盐酸,量取时需要用到量筒和
的稀盐酸,量取时需要用到量筒和______ (填一种仪器)。
(2)请通过计算说明每片药片中碳酸钙的质量是否与标签相符(写出计算过程)。
 的稀盐酸,充分反应,实验相关数据如图2所示(假设其他成分不参加反应)。
的稀盐酸,充分反应,实验相关数据如图2所示(假设其他成分不参加反应)。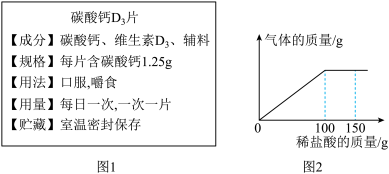
 的稀盐酸,量取时需要用到量筒和
的稀盐酸,量取时需要用到量筒和(2)请通过计算说明每片药片中碳酸钙的质量是否与标签相符(写出计算过程)。
更新时间:2024-05-23 15:37:04
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】根据方程式:锌与硫酸 反应生成氢气和硫酸锌。计算实验室里用13g锌与足量硫酸反应,可制得氢气和硫酸锌的质量各是多少?
反应生成氢气和硫酸锌。计算实验室里用13g锌与足量硫酸反应,可制得氢气和硫酸锌的质量各是多少?
 反应生成氢气和硫酸锌。计算实验室里用13g锌与足量硫酸反应,可制得氢气和硫酸锌的质量各是多少?
反应生成氢气和硫酸锌。计算实验室里用13g锌与足量硫酸反应,可制得氢气和硫酸锌的质量各是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】日常使用的金属材料,大多数属于合金。黄铜是以锌作主要添加的铜合金,用来制造弹壳的黄铜只含有锌和铜。将22g弹壳放在盛有100g稀硫酸的烧杯中(硫酸足量),当弹壳不再溶解后,烧杯中混合物的质量是121.8g。计算:
(1)产生的氢气质量为____ g。
(2)弹壳中锌的质量(写出计算过程)。
(1)产生的氢气质量为
(2)弹壳中锌的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与其他物质反应)中碳酸钙的含量,将25g石灰石研成粉末后加入100g稀盐酸,恰好完全反应后,固体和液体混合物的总质量为116.2g,回答下列问题:
(1)写出实验中发生反应的化学方程式___________ 。
(2)生成二氧化碳的质量是___________ 。
(3)根据已知条件列出求解样品中碳酸钙质量(X)的比例式___________ 。
(4)该样品中碳酸钙的质量分数为___________ 。
(5)若工业上用500t上述石灰石样品充分煅烧制取二氧化碳,同时制得氧化钙的质量为___________ 。
(1)写出实验中发生反应的化学方程式
(2)生成二氧化碳的质量是
(3)根据已知条件列出求解样品中碳酸钙质量(X)的比例式
(4)该样品中碳酸钙的质量分数为
(5)若工业上用500t上述石灰石样品充分煅烧制取二氧化碳,同时制得氧化钙的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某学校的化学兴趣小组为测定石灰石中碳酸钙的质量分数。采用的方法如下:现取25g石灰石样品于烧杯中,缓慢加入稀盐酸(石灰石中的杂质不溶于水,也不与稀盐酸反应),剩余固体质量与加入稀盐酸的质量关系如下图所示。
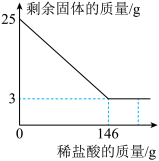
请计算(写出计算过程):
(1)石灰石中碳酸钙的质量分数。
(2)完全反应时生成的二氧化碳的质量。

请计算(写出计算过程):
(1)石灰石中碳酸钙的质量分数。
(2)完全反应时生成的二氧化碳的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】预防新冠肺炎疫情的过程中,常用质量分数为3%~6%的过氧化氢以及84消毒液(主要成分为NaClO)对生活场所杀菌清毒。
(1)实验室配制100 g 6%的过氧化氢溶液,需要过氧化氢的质量为__________ g。
(2)已知100g 84消毒液含氯量(含氯元素的质量分数)为5%,请计算其中所含NaClO的质量分数。
(3)将上述NaClO溶液通电一段时间,电解后负极产生的气体体积为22L,已知氢气的密度约为0.091 g/L。求剩余溶液的溶质质量分数(计算结果请保留一位小数)。
(1)实验室配制100 g 6%的过氧化氢溶液,需要过氧化氢的质量为
(2)已知100g 84消毒液含氯量(含氯元素的质量分数)为5%,请计算其中所含NaClO的质量分数。
(3)将上述NaClO溶液通电一段时间,电解后负极产生的气体体积为22L,已知氢气的密度约为0.091 g/L。求剩余溶液的溶质质量分数(计算结果请保留一位小数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】做电解水实验时,常在水中加入氢氧化钠以增强溶液的导电性,但氢氧化钠本身不会在电解水的过程中发生化学变化,氢氧化钠的质量也不会发生改变。现将8g氢氧化钠的溶液在101g水中并通电,一段时间后生成1g氢气。请回答下列问题:
(1)当生成0.7g氢气时,氢气与氧气在相同条件下的体积比约为_____;
(2)电解过程中,生成1g氢气时所消耗的水的质量;_____
(3)电解水过程中,当生成1g氢气时水溶液中氢氧化钠的质量分数。_____
(1)当生成0.7g氢气时,氢气与氧气在相同条件下的体积比约为_____;
(2)电解过程中,生成1g氢气时所消耗的水的质量;_____
(3)电解水过程中,当生成1g氢气时水溶液中氢氧化钠的质量分数。_____
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】硫酸铜、氯化钠的混合溶液可用于铜着色,为测定某着色液中氯化钠的质量分数,某学习小组量取100mL100g该着色液,向其中滴加硝酸银溶液,测得生成沉淀的质量与加入硝酸银溶液的质量关系如图所示。______ (选填“50”“100”或“250”)mL的量筒,还需要用到的一种仪器是______ 。
(2)恰好完全反应时消耗硝酸银溶液的质量为______ g。
(3)计算该着色液中氯化钠的质量分数。(写出计算过程)
(4)若量取该着色液时,仰视读数,则所测氯化钠的质量分数将______ (选填“偏大”“偏小”或“不变”)。
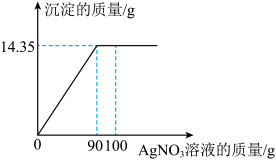
(2)恰好完全反应时消耗硝酸银溶液的质量为
(3)计算该着色液中氯化钠的质量分数。(写出计算过程)
(4)若量取该着色液时,仰视读数,则所测氯化钠的质量分数将
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】氢化钙(CaH2)是一种固体还原剂。遇水发生反应: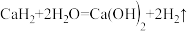 为了测定某样品中氢化钙的含量,实验小组取样品15.0g于烧杯中,加入20.0g水(20.0mL),用玻璃棒搅拌,实验后测得烧杯中剩余物质总质量为34.2g(杂质不参与反应)。
为了测定某样品中氢化钙的含量,实验小组取样品15.0g于烧杯中,加入20.0g水(20.0mL),用玻璃棒搅拌,实验后测得烧杯中剩余物质总质量为34.2g(杂质不参与反应)。
(1)求该样品中氢化钙的质量分数(要求写出计算过程)。
(2)与样品标签的标注对比,发现计算出的氢化钙的质量分数比标签的标注数值小,其原因可能有___________。
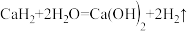 为了测定某样品中氢化钙的含量,实验小组取样品15.0g于烧杯中,加入20.0g水(20.0mL),用玻璃棒搅拌,实验后测得烧杯中剩余物质总质量为34.2g(杂质不参与反应)。
为了测定某样品中氢化钙的含量,实验小组取样品15.0g于烧杯中,加入20.0g水(20.0mL),用玻璃棒搅拌,实验后测得烧杯中剩余物质总质量为34.2g(杂质不参与反应)。(1)求该样品中氢化钙的质量分数(要求写出计算过程)。
(2)与样品标签的标注对比,发现计算出的氢化钙的质量分数比标签的标注数值小,其原因可能有___________。
| A.实验时未用玻璃棒充分搅拌,导致反应未充分进行 |
| B.用量筒量水时俯视读数了 |
| C.生成的Ca(OH)2微溶,部分未溶解形成沉淀了 |
| D.实验时间过长,反应后的溶液吸收了空气中的二氧化碳 |
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】江西省作为农业大省,农业关乎全省经济建设大局,农业的发展离不开化肥,某同学用某品牌的硝酸铵钙化肥(含有硝酸钙和硝酸铵)进行如下实验:取9.0克化肥样品溶解于41.0mL蒸馏水中,然后分5次加入一定量的Na2CO3溶液,充分反应后过滤(化肥中其他成分易溶于水,并且不会与碳酸钠反应),得到沉淀的质量如表。
(1)量取41.0mL蒸馏水所用量筒的规格最好为______ (选填“10”、“50”或“100”)mL。
(2)第五次加入碳酸钠溶液时,沉淀为什么没增加的原因:_____ 。
(3)请你设计实验方案除去硝酸钙中含有少量的硝酸铵:______ 。
(4)计算化肥样品中硝酸钙的质量分数。(写出计算过程,结果保留0.1%)
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 碳酸钠溶液质量(g) | 20.0 | 20.0 | 20.0 | 20.0 | 20.0 |
| 沉淀的总质量(g) | 1.0 | 2.0 | 3.0 | 4.0 | 4.0 |
(2)第五次加入碳酸钠溶液时,沉淀为什么没增加的原因:
(3)请你设计实验方案除去硝酸钙中含有少量的硝酸铵:
(4)计算化肥样品中硝酸钙的质量分数。(写出计算过程,结果保留0.1%)
您最近一年使用:0次



