盐湖提钾后产生的天然结晶水氯镁石中含有较多量的 ,少量的KCl、NaCl及泥沙。图1为从天然结晶水氯镁石提纯结晶水氯镁石
,少量的KCl、NaCl及泥沙。图1为从天然结晶水氯镁石提纯结晶水氯镁石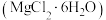 的某工艺流程。
的某工艺流程。 易溶于水和乙醇,KCl和NaCl微溶于乙醇;
易溶于水和乙醇,KCl和NaCl微溶于乙醇;
②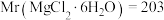 ;
;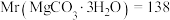 。
。
(1)“溶解”时,天然结晶水氯镁石粉碎的主要目的是______ ;选用无水乙醇而不选用水进行溶解的原因是______ 。
(2)操作完毕后展开滤纸,若黑色代表滤渣,则看到的情况最接近图中______ (填字母)。 的过程只是一个简单的溶解-析出过程,其具有的优点有
的过程只是一个简单的溶解-析出过程,其具有的优点有______ 。不考虑操作因素,产生 晶体实际质量可能大于理论质量的原因是
晶体实际质量可能大于理论质量的原因是______ 。
(4)研究发现:天然结晶水氯镁石表面的孔隙较少,上述流程提纯得到的 晶体表面孔隙较多,根据流程图分析,可能的原因是
晶体表面孔隙较多,根据流程图分析,可能的原因是______ 。
(5) 在一定条件下会分解生成
在一定条件下会分解生成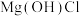 、
、 和水,该反应的化学方程式为
和水,该反应的化学方程式为______ 。
为进一步探究水氯镁石的分解,取一定质量 加热至590℃时,生成一种仅含两种元素的固体物质,测得过程中固体的质量变化率约为80%(已知:固体的质量变化率=
加热至590℃时,生成一种仅含两种元素的固体物质,测得过程中固体的质量变化率约为80%(已知:固体的质量变化率=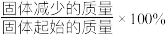 ),则该固体物质的化学式为
),则该固体物质的化学式为______ 。
(6)结晶水氯镁石可生产 。某天然结晶水氯镁石中
。某天然结晶水氯镁石中 的含量为81.2%,现需生产13.8t的
的含量为81.2%,现需生产13.8t的 ,求至少所需该种天然结晶水氯镁石的质量。
,求至少所需该种天然结晶水氯镁石的质量。______
 ,少量的KCl、NaCl及泥沙。图1为从天然结晶水氯镁石提纯结晶水氯镁石
,少量的KCl、NaCl及泥沙。图1为从天然结晶水氯镁石提纯结晶水氯镁石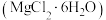 的某工艺流程。
的某工艺流程。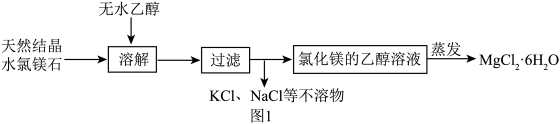
 易溶于水和乙醇,KCl和NaCl微溶于乙醇;
易溶于水和乙醇,KCl和NaCl微溶于乙醇;②
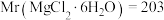 ;
;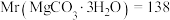 。
。(1)“溶解”时,天然结晶水氯镁石粉碎的主要目的是
(2)操作完毕后展开滤纸,若黑色代表滤渣,则看到的情况最接近图中

 的过程只是一个简单的溶解-析出过程,其具有的优点有
的过程只是一个简单的溶解-析出过程,其具有的优点有 晶体实际质量可能大于理论质量的原因是
晶体实际质量可能大于理论质量的原因是(4)研究发现:天然结晶水氯镁石表面的孔隙较少,上述流程提纯得到的
 晶体表面孔隙较多,根据流程图分析,可能的原因是
晶体表面孔隙较多,根据流程图分析,可能的原因是(5)
 在一定条件下会分解生成
在一定条件下会分解生成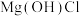 、
、 和水,该反应的化学方程式为
和水,该反应的化学方程式为为进一步探究水氯镁石的分解,取一定质量
 加热至590℃时,生成一种仅含两种元素的固体物质,测得过程中固体的质量变化率约为80%(已知:固体的质量变化率=
加热至590℃时,生成一种仅含两种元素的固体物质,测得过程中固体的质量变化率约为80%(已知:固体的质量变化率=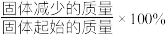 ),则该固体物质的化学式为
),则该固体物质的化学式为(6)结晶水氯镁石可生产
 。某天然结晶水氯镁石中
。某天然结晶水氯镁石中 的含量为81.2%,现需生产13.8t的
的含量为81.2%,现需生产13.8t的 ,求至少所需该种天然结晶水氯镁石的质量。
,求至少所需该种天然结晶水氯镁石的质量。
2024·江苏扬州·二模 查看更多[3]
2024年江苏省扬州市高邮市中考二模化学试题(已下线)专题12 工业流程-【好题汇编】2024年中考化学二模试题分类汇编(江苏专用)(已下线)专题18 工艺流程图题-【好题汇编】2024年中考化学二模试题分类汇编(全国通用)
更新时间:2024-06-14 12:46:11
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】根据如图所示实验回答下列问题:
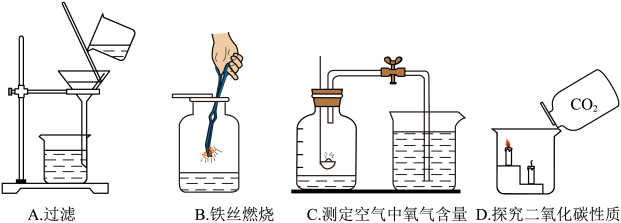
(1)实验A中玻璃棒的作用是_______ ;
(2)实验B中水的作用是_______ ,把ag铁丝放在氧气中完全燃烧,通过计算可知生产bg四氧化三铁,请判断a_______ b(选填“>”、“<”或“=”);
(3)实验C中,烧杯中的水进入集气瓶中的体积为_______ ;
(4)实验D证明了二氧化碳具有的性质是_______ 。

(1)实验A中玻璃棒的作用是
(2)实验B中水的作用是
(3)实验C中,烧杯中的水进入集气瓶中的体积为
(4)实验D证明了二氧化碳具有的性质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下表是 20℃时部分物质的溶解度数据。
(1)配制溶液:配制 50g11%氢氧化钠溶液的基本步骤是:计算—称取氢氧化钠固体—量取水—溶解—装瓶贴标签。 用托盘天平称取氢氧化钠固体的质量_________ g。
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向稀氢氧化钠溶液中通入 CO2,先生成 Na2CO3,继续通入 CO2,Na2CO3 会转化为 NaHCO3,已知后者为化合反应,请写出该化合反应的化学方程式:_________ 。 若向 20℃时饱和 Na2CO3 溶液中通入过量的 CO2,可观察到的现象是_________ 。
②结合表格中的有关数据,若以 20℃时,100g 饱和溶液吸收 CO2 的质量最大为依据,则除去 CO 气体中的 CO2 杂质,应选择_________ 溶液(填化学式),欲检验CO2气体的存在,则应选择_________ 溶液(填化学式)。
③将 2.2g CO2 通入 47.8g 一定浓度的 NaOH溶液中充分反应后(反应过程中没有CO2 逸出,水也没有蒸发),溶液中的溶质仅有 Na2CO3和 NaHCO3 两种物质(NaHCO3 在水中电离成 Na+和 HCO3-),则此时溶液中碳元素的质量分数为__________ ,在此反应过程中,你认为钠离子的个数_________ 发生变化?(填写: 有或者没有)
(3)电导率传感器可辅助探究复分解反应的实质。相同条件下,离子浓度越大,电导率越大,溶液导电性越强。将含有酚酞的 Ba(OH)2 溶液平均分成两份置于两个烧杯中 并插入电导率传感器,往其中一份滴加稀硫酸,往另一份滴加硫酸钠溶液,滴加过程中,这两份溶液的滴加速率始终相同,测得溶液的电导率变化如图所示。下列说法正确的是__________

a.乙曲线电导率减小过程中,溶液由红色变为无色
b.乙曲线对应的反应中四种离子数目都减少
c.甲曲线对应氢氧化钡与硫酸钠反应
d.甲曲线上的 M 点代表两种溶液恰好完全反应
物质 | Ca(OH)2 | NaOH | CaCO3 | Ca(HCO3)2 | Na2CO3 | NaHCO3 |
溶解度/g | 0.16 | 109 | 0.0065 | 16.6 | 21.8 | 9.6 |
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向稀氢氧化钠溶液中通入 CO2,先生成 Na2CO3,继续通入 CO2,Na2CO3 会转化为 NaHCO3,已知后者为化合反应,请写出该化合反应的化学方程式:
②结合表格中的有关数据,若以 20℃时,100g 饱和溶液吸收 CO2 的质量最大为依据,则除去 CO 气体中的 CO2 杂质,应选择
③将 2.2g CO2 通入 47.8g 一定浓度的 NaOH溶液中充分反应后(反应过程中没有CO2 逸出,水也没有蒸发),溶液中的溶质仅有 Na2CO3和 NaHCO3 两种物质(NaHCO3 在水中电离成 Na+和 HCO3-),则此时溶液中碳元素的质量分数为
(3)电导率传感器可辅助探究复分解反应的实质。相同条件下,离子浓度越大,电导率越大,溶液导电性越强。将含有酚酞的 Ba(OH)2 溶液平均分成两份置于两个烧杯中 并插入电导率传感器,往其中一份滴加稀硫酸,往另一份滴加硫酸钠溶液,滴加过程中,这两份溶液的滴加速率始终相同,测得溶液的电导率变化如图所示。下列说法正确的是

a.乙曲线电导率减小过程中,溶液由红色变为无色
b.乙曲线对应的反应中四种离子数目都减少
c.甲曲线对应氢氧化钡与硫酸钠反应
d.甲曲线上的 M 点代表两种溶液恰好完全反应
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】研究“水”可从多角度展开。
(1)水的电解

①宏观现象:按图所示装置,通电一段时间后,试管A、B中产生气体的体积比约为______ ;
②微观分析:该反应中发生分解的微粒名称是______ 。
(2)水的性质:
水能与许多物质发生化学反应,写出一个有水参加的化合反应______ 。
(3)水的用途
列举水在实验室中的一种用途______ 。
(4)水的净化
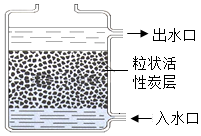
①如图是活性炭净水器示意图,其中粒状活性炭层的作用是______ 。
A.消毒 B.过滤 C.吸附 D.降低硬度
②使用山泉水之前加热煮沸,除了杀菌消毒外,还有______ 作用。
(1)水的电解

①宏观现象:按图所示装置,通电一段时间后,试管A、B中产生气体的体积比约为
②微观分析:该反应中发生分解的微粒名称是
(2)水的性质:
水能与许多物质发生化学反应,写出一个有水参加的化合反应
(3)水的用途
列举水在实验室中的一种用途
(4)水的净化
①如图是活性炭净水器示意图,其中粒状活性炭层的作用是

A.消毒 B.过滤 C.吸附 D.降低硬度
②使用山泉水之前加热煮沸,除了杀菌消毒外,还有
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐2】下列四个实验是判断稀硫酸与NaOH,NaCl,Na2CO3、Ba(NO3)2溶液能否发生复分解反应:
A H2SO4+NaOH B H2SO4+NaCl C H2SO4+Na2CO3 D H2SO4+Ba(NO3)2
(1)复分解反应发生的条件是___ ;
(2)能发生反应,但没有明显现象的是___ (填序号)
(3)实验D中发生反应的化学方程式为___ 。
A H2SO4+NaOH B H2SO4+NaCl C H2SO4+Na2CO3 D H2SO4+Ba(NO3)2
(1)复分解反应发生的条件是
(2)能发生反应,但没有明显现象的是
(3)实验D中发生反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】2020年12月12日,国家主席习近平在气候峰会上发表的重要讲话中提到,中国 将采取更加有力的政策和措施,力争在2030年前二氧化碳排放达到峰值,即“碳达峰”; 争取在2060年前实现“碳中和”(即通过植树造林、节能减排等形式,以抵消自身产生 的二氧化碳排放量,实现二氧化碳“零排放”)。我国对全世界宣布“碳中和”目标,彰显了大国的责任和担当。根据此材料,结合所学知识,回答以下问题:
(1)“碳”排放:
①化石燃料的燃烧是CO2排放的主要因素。化石燃料主要包括煤炭、_____ 和天然气。
②下列燃料在O2中燃烧时,不会产生CO2的是__________ (填序号)。
A.天然气 B.氢气 C.腓(N2H4) D.石蜡(C19H40)
(2)“碳"吸收。自然界有多种途径吸收CO2。
①绿色植物通过_____ 作用吸收CO2。
②风化的岩石如CaCO3粉末可吸收空气中的CO2和H2O转化为Ca(HCO3)2该反应的化学方程式为.__________ 。
③实验室用氧氧化钠溶液吸收CO2,用氢氧化钙溶液检验CO2的存在,吸收CO2时不用氢氧化钙的原因是__________ 。
(3)“碳”利用。将CO2作为资源是实现碳中和的有效方法。以CO2和H2为原料,再一定条件下可以合成C2H6O,该产物C2H6O中,C、H、O的质量比为________ 。
(1)“碳”排放:
①化石燃料的燃烧是CO2排放的主要因素。化石燃料主要包括煤炭、
②下列燃料在O2中燃烧时,不会产生CO2的是
A.天然气 B.氢气 C.腓(N2H4) D.石蜡(C19H40)
(2)“碳"吸收。自然界有多种途径吸收CO2。
①绿色植物通过
②风化的岩石如CaCO3粉末可吸收空气中的CO2和H2O转化为Ca(HCO3)2该反应的化学方程式为.
③实验室用氧氧化钠溶液吸收CO2,用氢氧化钙溶液检验CO2的存在,吸收CO2时不用氢氧化钙的原因是
(3)“碳”利用。将CO2作为资源是实现碳中和的有效方法。以CO2和H2为原料,再一定条件下可以合成C2H6O,该产物C2H6O中,C、H、O的质量比为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,人类的生产生活离不开水。
(1)1800年,尼科尔森(英)用伏打电池在常温下对水通电进行分解,得到氢气和氧气。
①该实验中正极和负极产生气体的体积之比为___________ ;
②以下实验中能够验证水的组成的实验是___________ ;
A.过氧化氢分解 B.氢气在氧气中燃烧 C.将水煮沸蒸发 D.电解水
(2)如图为利用膜技术净化水的部分过程。___________ (填“过滤”或“蒸发”)类似。
②经过超滤膜后得到的净化水属于___________ (填“混合物”或“纯净物”)。
(1)1800年,尼科尔森(英)用伏打电池在常温下对水通电进行分解,得到氢气和氧气。
①该实验中正极和负极产生气体的体积之比为
②以下实验中能够验证水的组成的实验是
A.过氧化氢分解 B.氢气在氧气中燃烧 C.将水煮沸蒸发 D.电解水
(2)如图为利用膜技术净化水的部分过程。
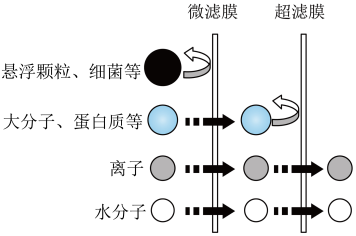
②经过超滤膜后得到的净化水属于
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐2】国内拥有许多再生资源基地,可回收处理大量废旧塑料电器及玻璃等,某品牌电器的废旧电路板中还有Fe、Cu、Ag、Ni(镍,银白色金属)等金属,如下图是某车间回收部分金属的工艺流程,已知,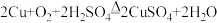 。
。

回答下列问题。
(1)操作①中,使用的玻璃仪器除烧杯外,还需_________ 。
(2)滤液②中含有的溶质是_________ 。
(3)由工艺流程,可以得出Ni、Fe的金属活动性强弱顺序是Fe_____ Ni(填“>”或“<”)。
(4)滤液③中加入足量铁粉的主要目的是______ ,固体A除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入适量的______ ,发生反应的化学方程式为_______ 。
(5)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是________ 。
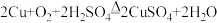 。
。
回答下列问题。
(1)操作①中,使用的玻璃仪器除烧杯外,还需
(2)滤液②中含有的溶质是
(3)由工艺流程,可以得出Ni、Fe的金属活动性强弱顺序是Fe
(4)滤液③中加入足量铁粉的主要目的是
(5)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐3】国家大力推广新能源汽车,新能源汽车的动力之一是锂电池。
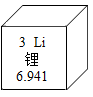
(1)下图是锂元素在元素周期表中的信息及原子结构示意图。下列说法不正确的是__________。

(2)下图是从钴酸锂废极片〔主要成分为钴酸锂(LiCoO2)〕中回收得到Co2O3和Li2CO3的一种工艺流程。

①操作1中,粉碎废极片的目的是________ ;
②实验室中完成操作2、3时,需用到的玻璃仪器是__________ ;
③操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,则该反应的化学方程式为________ ;
④操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而_______ (填“增大”或“减小”)。
(1)下图是锂元素在元素周期表中的信息及原子结构示意图。下列说法不正确的是__________。


| A.锂原子的中子数为3 |
| B.锂原子在化学反应中容易失去一个电子 |
| C.锂原子的相对原子质量为6.941 |
| D.氯化锂的化学式为LiCl2 |

①操作1中,粉碎废极片的目的是
②实验室中完成操作2、3时,需用到的玻璃仪器是
③操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,则该反应的化学方程式为
④操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而
您最近一年使用:0次
【推荐1】溶液在工农业生产和人们的日常生活中有着重要的应用。
(1)将下列物质加入水中,充分搅拌能形成无色溶液的是 (填序号)
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示。_______ ;
② 将 t2℃时相同质量的甲、乙两种物质的饱和溶液降温至 t1℃,所得两种溶液中溶剂质量由大到小的顺序是______ ;
③ t2℃时,将ng 甲固体加入100g水中,完全溶解形成溶液,放入一木块,木块漂浮在甲溶液中,降温到t1℃,析出32.4g 甲固体,此时甲溶液中的小木块浸入液体的体积_________ ( 填“变大”、“变小”或“不变”); n 的数值是_________ ;
(3)某同学配制75g 溶质质量分数为6%的氯化钠溶液。配制过程有以下步骤: a.称量及 量取 b.计算 c.溶解 d.装瓶贴标签,正确顺序是_______ (填序号);若用量筒量取水时俯视读数,其它操作正确,则所得溶液的质量分数 _____ 6%(填“>”、“<”或“=”)。
(1)将下列物质加入水中,充分搅拌能形成无色溶液的是 (填序号)
| A.面粉 | B.硝酸钾 | C.高锰酸钾 | D.冰 |
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示。
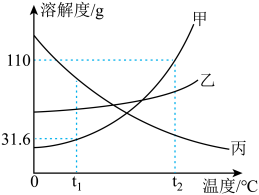
② 将 t2℃时相同质量的甲、乙两种物质的饱和溶液降温至 t1℃,所得两种溶液中溶剂质量由大到小的顺序是
③ t2℃时,将ng 甲固体加入100g水中,完全溶解形成溶液,放入一木块,木块漂浮在甲溶液中,降温到t1℃,析出32.4g 甲固体,此时甲溶液中的小木块浸入液体的体积
(3)某同学配制75g 溶质质量分数为6%的氯化钠溶液。配制过程有以下步骤: a.称量及 量取 b.计算 c.溶解 d.装瓶贴标签,正确顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】工业纯碱中含少量氯化钠。兴趣小组采用如图装置测定工业纯碱样品中碳酸钠的质量分数。实验中测得浓氢氧化钠溶液质量增加4.4g。

(1)计算样品中碳酸钠的质量______ 。
(2)实验分析:该方法测得的碳酸钠的质量分数误差较大,原因可能是_______ 。

(1)计算样品中碳酸钠的质量
(2)实验分析:该方法测得的碳酸钠的质量分数误差较大,原因可能是
您最近一年使用:0次



