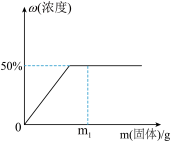
在室温下,向50g的水中加入某固体物质,所得溶液的质量分数(ω)与加入该物质的质量(m)的对应关系,如图所示。______ 。
(2)根据图,该固态物质在室温下的溶解度为______ g。
(3)若加入的固体物质质量为m1时,将混合体系的温度降低,所得溶液的浓度小于50%,则该物质的溶解度随温度升高而______ (填“增大”、“减小”或“不变”)。在室温下,加入的固体物质质量为m1时,若再加入30g水,固体恰好完全溶解,则m1=______ 。
(2)根据图,该固态物质在室温下的溶解度为
(3)若加入的固体物质质量为m1时,将混合体系的温度降低,所得溶液的浓度小于50%,则该物质的溶解度随温度升高而
2024·重庆·三模 查看更多[2]
更新时间:2024-06-18 22:24:42
|
相似题推荐
【推荐1】溶液与人们的生活密不可分。
(1)下列物质分别放入水中,能形成溶液的是___________ (填字母,下同)。
A 酒精 B 面粉 C 汽油 D 石灰石
(2)下列物质溶于水时,温度没有明显变化的是___________ 。
A 烧碱 B 硝酸铵 C 氯化钠 D 浓硫酸
(3)向装有等量水的A、B、C三个烧杯中分别加入10g、25g、25 g NaNO3固体,充分溶解后,现象如图1所示。

①烧杯中的溶液一定属于饱和溶液的是___________ (填字母)。
②图2中能表示NaNO3溶解度曲线的是___________ (填“甲”或“乙”)
③由图2分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是___________ (填字母)。
A 甲、乙都是饱和溶液 B 所含溶剂质量:甲<乙
C 溶液质量:甲>乙 D 溶质质量分数:甲>乙
(1)下列物质分别放入水中,能形成溶液的是
A 酒精 B 面粉 C 汽油 D 石灰石
(2)下列物质溶于水时,温度没有明显变化的是
A 烧碱 B 硝酸铵 C 氯化钠 D 浓硫酸
(3)向装有等量水的A、B、C三个烧杯中分别加入10g、25g、25 g NaNO3固体,充分溶解后,现象如图1所示。

①烧杯中的溶液一定属于饱和溶液的是
②图2中能表示NaNO3溶解度曲线的是
③由图2分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是
A 甲、乙都是饱和溶液 B 所含溶剂质量:甲<乙
C 溶液质量:甲>乙 D 溶质质量分数:甲>乙
您最近一年使用:0次
【推荐2】在t℃时,分别取甲、乙两固体物质的溶液,恒温蒸发水分,得到析出晶体质量与蒸发水的质量的关系如图所示(析出晶体不含结晶水)。

(1)蒸发水之前,甲形成的溶液是______ 溶液(填“饱和”或“不饱和”)。
(2)t℃时,甲、乙的溶解度大小关系为:甲______ 乙(填“<”、“>”或“=”)。
(3)P点时,乙溶液的溶质质量分数是______ 。
(4)下列说法不正确的是______(填字母)。
(5)工业上电解饱和食盐水制得NaOH、H2和Cl2,写出该反应的化学方程式______ ,该反应中Cl元素的化合价由______ 价变为0价。
(6)侯氏制碱的原理为:NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl;2NaHCO3 Na2CO3+CO2↑+H2O。结合如图回答下列问题:
Na2CO3+CO2↑+H2O。结合如图回答下列问题:

①NH4Cl溶液中混有少量NaCl,可用______ 方法提纯NH4Cl。
②60℃后,NaHCO3的溶解度无数据的原因可能是______ 。
(7)如图是配制50g质量分数为10%的氯化钠溶液的操作过程示意图,试回答:

①请指出图中两个明显的错误处,请填写错误操作序号______ 。
②若将错误更正后,进行实验,应称量氯化钠的质量是______ g;如果向托盘上加氯化钠时,指针偏向分度盘的右边,应进行的操作是______ 。
③量取水时,应选用______ 的量筒(从10mL,100mL中选择);量水读数时,量筒必须平放,视线要跟量筒内______ 处保持水平。
④若将错误更正后重新配制溶液,测得溶液中溶质质量分数小于10%。请你分析可能的原因有______ (填字母)。
A.用量筒量取水时俯视读数
B.配制溶液的烧杯用少量蒸馏水润洗
C.氯化钠晶体不纯
D.盛装溶液的试剂瓶用蒸馏水润洗
E.C操作中发现一部分氯化钠撒在烧杯外边
⑤若用溶质质量分数为20%NaCl溶液配制上述溶液,应取20%NaCl溶液______ g。

(1)蒸发水之前,甲形成的溶液是
(2)t℃时,甲、乙的溶解度大小关系为:甲
(3)P点时,乙溶液的溶质质量分数是
(4)下列说法不正确的是______(填字母)。
| A.甲中含有少量乙时,可用降温结晶的方法提纯乙 |
| B.t℃时,等质量的甲、乙饱和溶液,降温到相同温度,析出甲的质量小于乙 |
| C.用固体乙配制50g 6%的乙溶液,主要实验步骤是:计算、称量、混匀 |
| D.P点表示t℃时甲和乙的溶解度相等 |
(6)侯氏制碱的原理为:NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl;2NaHCO3
 Na2CO3+CO2↑+H2O。结合如图回答下列问题:
Na2CO3+CO2↑+H2O。结合如图回答下列问题:
①NH4Cl溶液中混有少量NaCl,可用
②60℃后,NaHCO3的溶解度无数据的原因可能是
(7)如图是配制50g质量分数为10%的氯化钠溶液的操作过程示意图,试回答:

①请指出图中两个明显的错误处,请填写错误操作序号
②若将错误更正后,进行实验,应称量氯化钠的质量是
③量取水时,应选用
④若将错误更正后重新配制溶液,测得溶液中溶质质量分数小于10%。请你分析可能的原因有
A.用量筒量取水时俯视读数
B.配制溶液的烧杯用少量蒸馏水润洗
C.氯化钠晶体不纯
D.盛装溶液的试剂瓶用蒸馏水润洗
E.C操作中发现一部分氯化钠撒在烧杯外边
⑤若用溶质质量分数为20%NaCl溶液配制上述溶液,应取20%NaCl溶液
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
真题
解题方法
【推荐3】研究物质的溶解对于生产、生活有着重要意义。
①下表是硝酸钾的部分溶解度数据。
由表中数据可知,硝酸钾的溶解度随温度升高而______ (选填“变大”或“变小”)。60℃时硝酸钾饱和溶液中,溶质与溶剂的质量比为_______ ,能将该饱和溶液转化为不饱和溶液的一种方法是________ 。
②探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如下图所示:

坐标图中,符合实验结果的描点可能是___________ (选填编号)。

③取等质量甲和乙两种物质(均不含结晶水)进行如下图所示实验,最终烧杯中析出固体的质量乙大于甲。

40℃时,甲的溶解度______ (选填“大于”“等于”或“小于”)乙的溶解度根据本实验结果,能否判断40~80℃间甲、乙哪种物质的溶解度变化随温度影响更大_____ (选填“能”或“不能”)。
①下表是硝酸钾的部分溶解度数据。
| 温度(℃) | 20 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 31.6 | 63.9 | 110 | 169 |
②探究20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如下图所示:

坐标图中,符合实验结果的描点可能是

③取等质量甲和乙两种物质(均不含结晶水)进行如下图所示实验,最终烧杯中析出固体的质量乙大于甲。

40℃时,甲的溶解度
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】请根据图中A、B、C三种固体物质的溶解度曲线,回答下列问题。

(1)t2℃时,三种固体物质的溶解度由小到大的顺序是_______________
(2)M点含义:_______________________
(3)将t2℃时C的饱和溶液转化为不饱和溶液,你的方法是____________
(4)要从AB的混合物中提纯A物质,方法是_________________

(1)t2℃时,三种固体物质的溶解度由小到大的顺序是
(2)M点含义:
(3)将t2℃时C的饱和溶液转化为不饱和溶液,你的方法是
(4)要从AB的混合物中提纯A物质,方法是
您最近一年使用:0次
【推荐2】如图是甲、乙两种固体物质的溶解度曲线。据图回答:

(1)20℃时,等质量的甲、乙饱和溶液中,溶剂的质量甲_______ 乙(填“>”或“=”或“<”)。
(2)10℃时,30g甲物质放入50g水中,所得溶液溶质质量分数为_________ 。
(3)10℃时,欲将20%的乙溶液变成该温度下30%的溶液,可以选择 。(填字母)
(4)将30℃时甲、乙两物质饱和溶液各100g分别蒸发10g水,然后降低温度到10℃,对所得溶液的下列说法中不正确的是 。(填字母)

(1)20℃时,等质量的甲、乙饱和溶液中,溶剂的质量甲
(2)10℃时,30g甲物质放入50g水中,所得溶液溶质质量分数为
(3)10℃时,欲将20%的乙溶液变成该温度下30%的溶液,可以选择 。(填字母)
| A.增加溶质 | B.蒸发溶剂 | C.增加溶剂 | D.无法做到 |
| A.都是饱和溶液 | B.溶液质量甲<乙 |
| C.溶质质量甲=乙 | D.溶质质量分数甲=乙 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
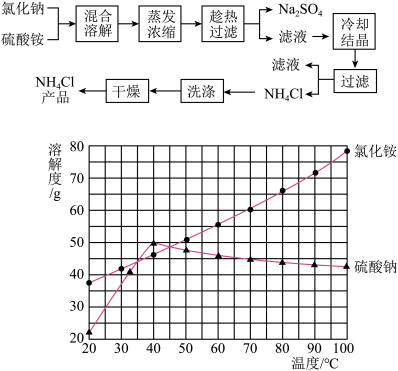
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl_____ g。
(2)实验室进行蒸发浓缩用到的主要仪器有_____ 、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为_____ 。
(4)不用其他试剂,检查NH4Cl产品是否纯净的方法及操作是_____ 。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是_____ 。

氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl
(2)实验室进行蒸发浓缩用到的主要仪器有
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为
(4)不用其他试剂,检查NH4Cl产品是否纯净的方法及操作是
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】甲、乙两种固体(均不含结晶水)的溶解度曲线如图所示,请回答:

①_____ ℃时,甲、乙的溶解度相等。
②t1℃时,甲的饱和溶液中溶质质量分数是_____ 。
③t2℃时,80g乙放入100g水中充分溶解,可以得到该温度时乙的_____ (选填“饱和”或“不饱和”)溶液,溶液质量为_____ g。
④将t2℃时等质量的甲、乙饱和溶液,降温至t℃(t1<t<t2),相关分析正确的是_____ 。(选填编号)
at2℃时,甲、乙两溶液的溶质质量分数之比为75:50
b降温过程中,甲、乙两溶液的溶剂质量之比不变
c降温至t℃时,甲、乙两溶液的溶质质量可能相等
d降温至t℃时,甲、乙两溶液的质量可能相等

①
②t1℃时,甲的饱和溶液中溶质质量分数是
③t2℃时,80g乙放入100g水中充分溶解,可以得到该温度时乙的
④将t2℃时等质量的甲、乙饱和溶液,降温至t℃(t1<t<t2),相关分析正确的是
at2℃时,甲、乙两溶液的溶质质量分数之比为75:50
b降温过程中,甲、乙两溶液的溶剂质量之比不变
c降温至t℃时,甲、乙两溶液的溶质质量可能相等
d降温至t℃时,甲、乙两溶液的质量可能相等
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】如图为A、B两种固体物质的溶解度曲线。
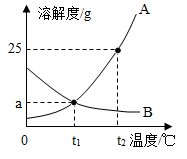
(1) 在______ ℃时,A、B两种物质的溶解度相等;
(2) t2℃时,100g水中溶解_____ g A物质恰好饱和,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水_______ g;
(3) t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,则溶质的质量分数的大小关系为________ (填“A=B”“A>B”或“A<B”)。

(1) 在
(2) t2℃时,100g水中溶解
(3) t2℃时,分别将恰好饱和的A、B两种物质的溶液降温至t1℃,则溶质的质量分数的大小关系为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】工业上用硫铁矿(主要成分是FeS2)在空气中焙烧去硫后烧渣(主要成分为Fe2O3、FeO、Al2O3、SiO2,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O)的流程如图所示:

已知:①焙烧过程主要反应为:
②Fe3+、A13+、Fe2+在溶液中开始沉淀至沉淀完全的pH值如下表:
(l)“浸取”时生成Fe3+的化学方程式为___________ 。能提高烧渣浸取速率的措施有___________ (填字母)。
a将烧渣粉碎 b降低硫酸的浓度 c快速搅拌
(2)“还原”的目的是将溶液中的Fe3+完全转化为Fe2+。若还原剂X是铁粉,反应化学方程式
为___________ 。若还原剂X是SO2,反应方程式为: ,采用SO2作还原剂的优点是
,采用SO2作还原剂的优点是___________ 。
(3)“调pH”时,pH的最佳范围是___________ (用不等式表示),滤渣Ⅱ的成分是___________ (写化学式)。
(4)FeSO4·7H2O的溶解度曲线如图所示,“过滤Ⅱ”后,经___________ 、___________ 、过滤、少量冰水洗涤、低温干燥等步骤可得到FeSO4·7H2O晶体。


已知:①焙烧过程主要反应为:

②Fe3+、A13+、Fe2+在溶液中开始沉淀至沉淀完全的pH值如下表:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.1 | 3.5 | 6.5 |
| 沉淀完全的pH | 3.2 | 4.7 | 9.7 |
a将烧渣粉碎 b降低硫酸的浓度 c快速搅拌
(2)“还原”的目的是将溶液中的Fe3+完全转化为Fe2+。若还原剂X是铁粉,反应化学方程式
为
 ,采用SO2作还原剂的优点是
,采用SO2作还原剂的优点是(3)“调pH”时,pH的最佳范围是
(4)FeSO4·7H2O的溶解度曲线如图所示,“过滤Ⅱ”后,经

您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】在某温度下,分别向盛有等质量蒸馏水的两烧杯中逐渐加入固体溶质甲或乙,图中x表示所加固体的质量,y表示溶液中溶质与水的质量比。
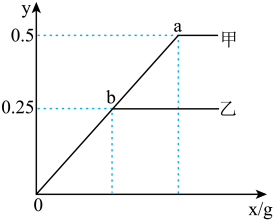
(1)该温度时,乙的溶解度为_______________ 。
(2)从50g该温度下甲的饱和溶液中取走25g溶液,然后加水到50g搅拌均匀:再倒出25g溶液,在剩余溶液中再加水25g搅拌 均匀:第三次再倒出25g溶液,剩余溶液的质量分数为_________ 。
(3)该温度时,现有质量分数均为w%的两份乙溶液:200g与300g,若将两份溶液分别蒸发80g水,再一起冷却到原温度时,依次析出晶体为mg与ng,则m与n的关系为___________ 。

(1)该温度时,乙的溶解度为
(2)从50g该温度下甲的饱和溶液中取走25g溶液,然后加水到50g搅拌均匀:再倒出25g溶液,在剩余溶液中再加水25g搅拌 均匀:第三次再倒出25g溶液,剩余溶液的质量分数为
(3)该温度时,现有质量分数均为w%的两份乙溶液:200g与300g,若将两份溶液分别蒸发80g水,再一起冷却到原温度时,依次析出晶体为mg与ng,则m与n的关系为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】气体的溶解度也有一定的变化规律。
(1)打开可乐瓶,逸出大量气泡。由此可见,压强越小,CO2的溶解度越____ 。为增大CO2的溶解度,可采用的一种方法是____ ;
(2)不同温度下,氧气的溶解度随压强的变化如图所示,图中t1对应的温度为40 ℃,则t2对应的温度____ (填编号)。
a.大于40 ℃ b.小于40 ℃ c.无法确定

(1)打开可乐瓶,逸出大量气泡。由此可见,压强越小,CO2的溶解度越
(2)不同温度下,氧气的溶解度随压强的变化如图所示,图中t1对应的温度为40 ℃,则t2对应的温度
a.大于40 ℃ b.小于40 ℃ c.无法确定

您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】t2℃时,将甲、乙两种固体各 80g 分别放到盛有 100g 水的两个烧杯中,充分溶解后, 恢复到 t2℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:

(1)M 点的含义是_____ 。
(2)向烧杯①的溶液中继续加入 15g 甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是_____ 。
(3)将 t2℃等质量的甲、乙饱和溶液分别降温到 t1℃时,所得溶液的有关说法正确的是_____ (填字母序号)
A 甲溶液仍为饱和溶液
B 两溶液质量:甲<乙
C 两溶液中溶剂质量甲=乙
D 两溶液中溶质质量:甲>乙
(4)气体的溶解度也有一定的变化规律,不同的温度下,氧气的溶解度随压强而变化的情况如图所示,若 t1℃对应的温度为 40℃,则 t2对应的温度_____ (填字母序号)。

A 大于 40℃
B 小于 40℃
C 无法确定

(1)M 点的含义是
(2)向烧杯①的溶液中继续加入 15g 甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是
(3)将 t2℃等质量的甲、乙饱和溶液分别降温到 t1℃时,所得溶液的有关说法正确的是
A 甲溶液仍为饱和溶液
B 两溶液质量:甲<乙
C 两溶液中溶剂质量甲=乙
D 两溶液中溶质质量:甲>乙
(4)气体的溶解度也有一定的变化规律,不同的温度下,氧气的溶解度随压强而变化的情况如图所示,若 t1℃对应的温度为 40℃,则 t2对应的温度

A 大于 40℃
B 小于 40℃
C 无法确定
您最近一年使用:0次



