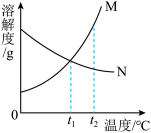
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
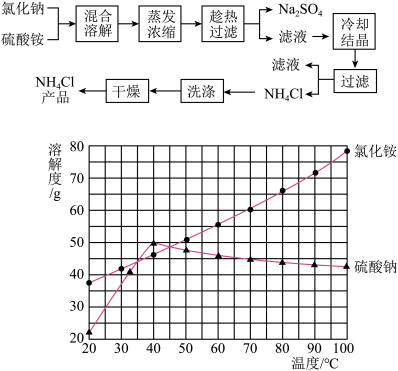
氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl_____ g。
(2)实验室进行蒸发浓缩用到的主要仪器有_____ 、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为_____ 。
(4)不用其他试剂,检查NH4Cl产品是否纯净的方法及操作是_____ 。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是_____ 。

氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl
(2)实验室进行蒸发浓缩用到的主要仪器有
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为
(4)不用其他试剂,检查NH4Cl产品是否纯净的方法及操作是
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是
更新时间:2020-05-27 23:46:52
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】回答问题
(1)近年来许多试验证实,食盐摄入量与高血压发病率有一定关系,膳食中食盐摄入过多,可引起高血压。为预防冠心病和高血压,世界卫生组织建议每人每日摄入6g以下食盐。食盐的主要成分是氯化钠,氯化钠的化学式为_______ 。
(2)A、B、C三种物质各40克,它们发生化合反应时,生成80克新物质D。再增加10克B,B与C恰好完全反应,若再加入适量的B和C恰好将A反应完,则还可以生成D的质量为_______ 克。
(1)近年来许多试验证实,食盐摄入量与高血压发病率有一定关系,膳食中食盐摄入过多,可引起高血压。为预防冠心病和高血压,世界卫生组织建议每人每日摄入6g以下食盐。食盐的主要成分是氯化钠,氯化钠的化学式为
(2)A、B、C三种物质各40克,它们发生化合反应时,生成80克新物质D。再增加10克B,B与C恰好完全反应,若再加入适量的B和C恰好将A反应完,则还可以生成D的质量为
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】实验室中常用乙醇(C2H5OH)作燃料,乙醇完全燃烧的化学方程式是______ 。现有一定质量的乙醇和氧气混合于密闭容器内,在一定条件下完全反应生成CO和CO2的混合物12.6g且质量比为1:11,同时生成水的质量为______ 。
您最近一年使用:0次
【推荐3】C、H2、CO三大还原剂都具有可燃性和还原性,重庆一中某化学拓展小组设计如图所示实验装置,分别对三种还原剂有关问题进行探究。

(1)按装置进行规范实验,操作正确的顺序为_______ 。
①通入气体X ②点燃A处酒精灯 ③熄灭A处酒精灯 ④停止通入气体X
(2)当观察到A中黑色固体变红。B中固体变蓝,C中溶液变浑浊时,说明X气体是CO和H2,若将BC交换位置,不能检验的气体是_______ 。
(3)若将A中CuO换成一种黑色固体混合物,实验中持续通入N2,观察到A中黑色固体变红,C中澄清石灰水变浑浊,该黑色固体成分是_______ 。
(4)果糖完全燃烧只生成H2O和CO2,为确定果糖中是否含有氧元素用D装置替换A,通入一定量O2,实验后测得果糖减少的质量为a,B装置增加的质量为b,C中产生沉淀质量为c,氧化铜的作用是_______ 。理论上需要满足式子_______ (用a、b、c表示)时,说明果糖中含氧元素。


(1)按装置进行规范实验,操作正确的顺序为
①通入气体X ②点燃A处酒精灯 ③熄灭A处酒精灯 ④停止通入气体X
(2)当观察到A中黑色固体变红。B中固体变蓝,C中溶液变浑浊时,说明X气体是CO和H2,若将BC交换位置,不能检验的气体是
(3)若将A中CuO换成一种黑色固体混合物,实验中持续通入N2,观察到A中黑色固体变红,C中澄清石灰水变浑浊,该黑色固体成分是
(4)果糖完全燃烧只生成H2O和CO2,为确定果糖中是否含有氧元素用D装置替换A,通入一定量O2,实验后测得果糖减少的质量为a,B装置增加的质量为b,C中产生沉淀质量为c,氧化铜的作用是

您最近一年使用:0次
【推荐1】如图是KNO3和NaCl的溶解度曲线,试回答下列问题。

(1)曲线B表示___________ (填“KNO3”或“NaCl”)。
(2)70℃时溶解度A___________ (填“<”“>”“=”)B。
(3)除去KNO3中混入的少量NaCl,可采用___________ 方法。
(4)40℃时30gA放入100g水中,充分溶解,所得溶液的溶质质量分数=___________ (计算结果精确到0.1%,下同)。
(5)10℃时在四个烧杯中分别放入等质量的固体A,分别倒入不同质量的水,充分搅拌,倒入水的质量以及固体A剩余的情况如下表所示。
则4号烧杯所得溶液中溶质质量分数(ω)的取值范围是___________ 。

(1)曲线B表示
(2)70℃时溶解度A
(3)除去KNO3中混入的少量NaCl,可采用
(4)40℃时30gA放入100g水中,充分溶解,所得溶液的溶质质量分数=
(5)10℃时在四个烧杯中分别放入等质量的固体A,分别倒入不同质量的水,充分搅拌,倒入水的质量以及固体A剩余的情况如下表所示。
| 烧杯编号 | 1 | 2 | 3 | 4 |
| 倒入水的质量/g | 25 | 50 | 100 | 200 |
| 剩余固体情况 | 有 | 有 | 无 | 无 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:

(1)P点的含义是_____________________________ 。
(2)t2℃时,30g a物质加入到50g水中不断搅拌,能形成溶液的质量为_____ 。溶质的质量分数是____ (精确到0.1)
(3)t2℃时,a、b、c三种物质的溶解度按由小到大的排列顺序是_________________ 。
(4)t1℃时,P点所表示的b物质的溶液是_______ (饱和/不饱和)溶液。
(5)若a中混有的少量b,除去b而提纯a的方法是__________________ 。
(6)a、b、c三种物质的饱和溶液由t2℃降到t1℃时,a、b、c三种物质的溶质质量分数由小到大的排列顺序是_________________ 。

(1)P点的含义是
(2)t2℃时,30g a物质加入到50g水中不断搅拌,能形成溶液的质量为
(3)t2℃时,a、b、c三种物质的溶解度按由小到大的排列顺序是
(4)t1℃时,P点所表示的b物质的溶液是
(5)若a中混有的少量b,除去b而提纯a的方法是
(6)a、b、c三种物质的饱和溶液由t2℃降到t1℃时,a、b、c三种物质的溶质质量分数由小到大的排列顺序是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】如图是对海水综合利用的示意图。

(1)粗盐提纯。粗盐中还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,他们在溶液中主要以 、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入
、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入______ 等试剂将其转化为沉淀除去。第②步操作中蒸发结晶时玻璃棒的作用是______ 。
(2)海水制镁。使海水中氯化镁转化为沉淀,方程式是______ 。由镁单质的制取,我们可以判断氯化钠通电制取钠单质的反应方程式是______ 。
(3)海水制碱。我国科学家发明的联合制碱法的反应方程式是______ ,反应后碳酸氢钠先结晶析出的原因是______ 。该方法的最大优点是反应后的氯化铵可以作______ 肥。

(1)粗盐提纯。粗盐中还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,他们在溶液中主要以
 、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入
、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入(2)海水制镁。使海水中氯化镁转化为沉淀,方程式是
(3)海水制碱。我国科学家发明的联合制碱法的反应方程式是
您最近一年使用:0次
【推荐2】硝酸钾、氯化钾是常见的化肥,可促进农作物生长发育。
(1)从化肥的种类分析,硝酸钾属于__________ 肥。
(2)根据表格分析,下列说法,正确的是__________ (填标号)。
a.硝酸钾的溶解度大于氯化钾
b.20℃时,将40g的KCl放入100g水中,所得溶液质量为140g
c.将40℃时的KCl饱和溶液降温至20℃,会有晶体析出
d.若要除去硝酸钾固体中混有的少量氯化钾,可采用降温结晶法
(3)研究发现,棉花种植过程中,叶面喷施3%的硝酸钾溶液可有效预防红叶茎枯病。
①欲配制500g溶质质量分数为3%的硝酸钾溶液,需要KNO3的质量为__________ g。
②下列操作会导致所配制溶液的溶质质量分数偏大的是__________ (填标号)
a.用天平称量硝酸钾固体时。所用砝码生锈
b.用量筒量取水时仰视读数
c.将配制好的溶液装瓶后,烧杯内有溶液残留
d.向烧杯中加水时有水洒出
③硝酸钾可作为无土栽培的一种营养液。现将100g3%的硝酸钾溶液稀释到1%,用于培植营养液,则需加水的体积是__________ mL。(水的密度为1g·cm-3)
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCI | 28 | 31.2 | 34.2 | 37.2 | 40.1 | 42.6 | 45.8 | 51.3 | |
(2)根据表格分析,下列说法,正确的是
a.硝酸钾的溶解度大于氯化钾
b.20℃时,将40g的KCl放入100g水中,所得溶液质量为140g
c.将40℃时的KCl饱和溶液降温至20℃,会有晶体析出
d.若要除去硝酸钾固体中混有的少量氯化钾,可采用降温结晶法
(3)研究发现,棉花种植过程中,叶面喷施3%的硝酸钾溶液可有效预防红叶茎枯病。
①欲配制500g溶质质量分数为3%的硝酸钾溶液,需要KNO3的质量为
②下列操作会导致所配制溶液的溶质质量分数偏大的是
a.用天平称量硝酸钾固体时。所用砝码生锈
b.用量筒量取水时仰视读数
c.将配制好的溶液装瓶后,烧杯内有溶液残留
d.向烧杯中加水时有水洒出
③硝酸钾可作为无土栽培的一种营养液。现将100g3%的硝酸钾溶液稀释到1%,用于培植营养液,则需加水的体积是
您最近一年使用:0次
【推荐3】
(1)目前,我国一些城市推广使用“乙醇汽油”作汽车燃料:
①乙醇属于_________________ 化合物(填“有机”或“无机”)。
②写出乙醇完全燃烧的化学方程式:_____________________________________ 。
(2)将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如右图所示:
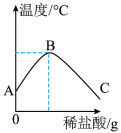
①由图知,稀盐酸与氢氧化钠溶液发生的反应是_________ (填“放热”或“吸热”)反应。
②从A到B过程中,烧杯中溶液的pH逐渐__________ 。B点表示的含义是 ______________ 。
(3)小明家菜地里的蔬菜叶子发黄了,妈妈叫他去买化肥碳酸氢铵(NH4HCO3)来施用,当他到化肥商店时,碳酸氢铵刚好缺货,你建议他买_____________ (填“尿素”或“氯化钾”),也能起到与碳酸氢铵相同的作用。
(1)目前,我国一些城市推广使用“乙醇汽油”作汽车燃料:
①乙醇属于
②写出乙醇完全燃烧的化学方程式:
(2)将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如右图所示:

①由图知,稀盐酸与氢氧化钠溶液发生的反应是
②从A到B过程中,烧杯中溶液的pH逐渐
(3)小明家菜地里的蔬菜叶子发黄了,妈妈叫他去买化肥碳酸氢铵(NH4HCO3)来施用,当他到化肥商店时,碳酸氢铵刚好缺货,你建议他买
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】杂卤石属于“呆矿”,主要成分有K2SO4、MgSO4、CaSO4、不溶性成分等,可作为一种钾资源。实验室模拟工厂用杂卤石溶浸液制备硫酸钾,流程如下:(假设不溶性成分不参加反应)

(1)在实验流程中,“加过量的石灰乳”的目的是除去溶浸液中的___________ ,用石灰乳而不用澄清石灰水的原因是__________________________________________ 。
(2)X溶液中的溶质是______________ (写名称)。
(3)固体B含有杂卤石中的不溶性成分和加试剂时所产生的_______________ (写化学式)。
(4)向溶液A中加稀硫酸时,所发生中和反应的化学方程式为_________________ 。
(5)操作b的名称是___________ ,需要用到的仪器有铁架台、酒精灯、玻璃棒和________ 。

(1)在实验流程中,“加过量的石灰乳”的目的是除去溶浸液中的
(2)X溶液中的溶质是
(3)固体B含有杂卤石中的不溶性成分和加试剂时所产生的
(4)向溶液A中加稀硫酸时,所发生中和反应的化学方程式为
(5)操作b的名称是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】从盐湖中提取的某种矿物主要含有KC1,还有少量MgSO4、CaC12及不溶性杂质SiO2.从该矿物中提取KC1的流程如下图:

回答下列问题:
(1)滤渣1的主要成分是_______ 。(填化学式)
(2)生成滤渣Ⅱ的化学方程式是________ 。
(3)向滤液Ⅱ中加入过量盐酸可以除去过量的Y溶液,除此之外盐酸还具有的作用是______ 。
(4)蒸发溶液得到KC1固体的过程中,要用玻璃棒不断搅拌,目的是________ 。

回答下列问题:
(1)滤渣1的主要成分是
(2)生成滤渣Ⅱ的化学方程式是
(3)向滤液Ⅱ中加入过量盐酸可以除去过量的Y溶液,除此之外盐酸还具有的作用是
(4)蒸发溶液得到KC1固体的过程中,要用玻璃棒不断搅拌,目的是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐3】提纯某KCl样品(含有少量的MgCl2和K2SO4)的方案(所加试剂均过量)如下:
样品 溶液
溶液 浊液
浊液 滤液
滤液 溶液
溶液
回答下列问题:
(1)步骤①和③的实验操作均用到的玻璃仪器有玻璃棒和_____ 。
(2)步骤②得到的浊液中含有Mg(OH)2和BaSO4沉淀,写出生成BaSO4的化学方程式_____ 。
(3)确定步骤③所加的K2CO3是否过量的方法是:在加入K2CO3后的浊液中取少量上层澄清液于试管,然后滴加K2CO3溶液,若没有白色沉淀生成,则说明所加K2CO3_____ .。
(4)步骤④得到的溶液的溶质除了KCl外,还含有_____ (填化学式)。若要得到KCl晶体,还要进行如下操作:将溶液倒入 _____ (填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到 _____ 时(填现象),停止加热,用余热使水分蒸干。
样品
 溶液
溶液 浊液
浊液 滤液
滤液 溶液
溶液回答下列问题:
(1)步骤①和③的实验操作均用到的玻璃仪器有玻璃棒和
(2)步骤②得到的浊液中含有Mg(OH)2和BaSO4沉淀,写出生成BaSO4的化学方程式
(3)确定步骤③所加的K2CO3是否过量的方法是:在加入K2CO3后的浊液中取少量上层澄清液于试管,然后滴加K2CO3溶液,若没有白色沉淀生成,则说明所加K2CO3
(4)步骤④得到的溶液的溶质除了KCl外,还含有
您最近一年使用:0次