学习小组为测定一瓶失去标签的硝酸银溶液的溶质质量分数,向100g该硝酸银溶液中滴加一定溶质质量分数的盐酸,实验数据如下表所示:
请分析并计算:
(1)表中m的值为______ 。
(2)计算该硝酸银溶液的溶质质量分数。
| 时间/s | 0 | 30 | 60 | 90 | 120 |
| 产生沉淀的质量/g | 0 | 4.8 | m | 14.35 | 14.35 |
(1)表中m的值为
(2)计算该硝酸银溶液的溶质质量分数。
更新时间:2024-05-28 11:35:17
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】在一次探究实验中,某学习小组将a 克高锰酸钾充分加热至不再放出气体为止,若试管中剩余固体的质量随时间变化关系如图所示。请计算:
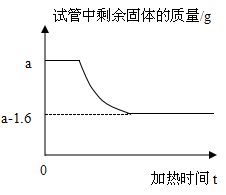
(1)根据质量守恒定律,反应生成氧气的质量为_______g。
(2)该小组加入的高锰酸钾的质量(即a克)是多少?(要求写出计算过程)
(3)反应后剩余固体中钾、锰两种元素的质量比为__________。

(1)根据质量守恒定律,反应生成氧气的质量为_______g。
(2)该小组加入的高锰酸钾的质量(即a克)是多少?(要求写出计算过程)
(3)反应后剩余固体中钾、锰两种元素的质量比为__________。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验室用34克过氧化氢溶液和1克二氧化锰制取氧气,实验的相关数据如图所示。请回答:
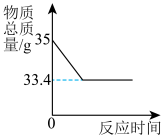
(1)二氧化锰作为催化剂在化学反应前后本身的_______ 都没有发生变化。
(2)反应生成氧气的质量为_______ g。
(3)反应中过氧化氢与氧气的质量比是多少?(在化学方程式中对应位置写出即可)

(1)二氧化锰作为催化剂在化学反应前后本身的
(2)反应生成氧气的质量为
(3)反应中过氧化氢与氧气的质量比是多少?(在化学方程式中对应位置写出即可)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为测定某瓶碳酸钠溶液的溶质质量分数,小云同学取50g该碳酸钠溶液于烧杯中,逐滴加入50g溶质质量分数为10.4%的氯化钡溶液,恰好完全反应。
请计算:(提示: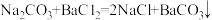 )
)
(1)参加反应的氯化钡的质量为 g。
(2)该瓶碳酸钠溶液的溶质质量分数。
请计算:(提示:
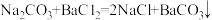 )
)(1)参加反应的氯化钡的质量为 g。
(2)该瓶碳酸钠溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】现有氧化铜和铜的混合物,对其成分进行分析。取24g此样品,向其中分三次加入相同溶质质量分数的稀硫酸,使之充分反应,每次所用稀硫酸的质量及剩余固体的质量记录于下表:
试回答下列问题∶
(1)上述表格中m 的值为______。
(2)CuO的质量为______g。
(3)稀硫酸中硫酸的溶质质量分数是______(保留到小数点后一位)。
(4)氧化铜溶解完全所消耗的稀硫酸的质量为______g。
| 第一次 | 第二次 | 第三次 | |
| 加入稀硫酸的质量(g) | 80 | 160 | 240 |
| 充分反应后剩余固体质量(g) | 8 | 4 | m |
试回答下列问题∶
(1)上述表格中m 的值为______。
(2)CuO的质量为______g。
(3)稀硫酸中硫酸的溶质质量分数是______(保留到小数点后一位)。
(4)氧化铜溶解完全所消耗的稀硫酸的质量为______g。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】碳酸钠和碳酸氢钠是生活中常见的盐。已知碳酸钠很稳定受热不易分解,碳酸氢钠受热易分解,生成碳酸钠,其反应的化学方程式为:______ 。某同学进行如下实验:将碳酸钠和碳酸氢钠的混合物13.7g充分加热至质量不再改变,冷却至室温,再向其中加入100g质量分数为7.3%的盐酸恰好完全反应。则原混合物中碳酸钠的质量为______ g。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某氢氧化钙中含有碳酸钙杂质,称取研细的样品12.5g放入锥形瓶中,加入32.5g水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,测得加入盐酸的质量与锥形瓶中物质的质量关系如下表所示。
(1)加入盐酸的质量在0~25g时,相应的化学方程式是___________ 。
(2)求样品中氢氧化钙的质量分数?
| 加入盐酸的质量/g | 0 | 25 | 37.5 |
| 锥形瓶中物质的质量/g | 45 | 70 | 79.2 |
(2)求样品中氢氧化钙的质量分数?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】BaCl2是一种重金属盐,其水溶液具有很强的毒性。若误服了BaCl2溶液可立即服用MgSO4溶液解毒。为测定某BaCl2溶液的溶质质量分数,现取 100g 该BaCl2溶液,加入100g MgSO4溶液,两者恰好完全反应,过滤后所得滤液质量为 176.7g。
(1)反应生成沉淀的质量为 g。
(2)原BaCl2溶液中溶质的质量分数。
(1)反应生成沉淀的质量为 g。
(2)原BaCl2溶液中溶质的质量分数。
您最近一年使用:0次




