“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为xNaCl+2H2O=xNaOH+H2↑+Cl2↑。在20℃时,取136g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g。已知:20℃时,NaCl的溶解度为36g。
请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= 。
(2)通过计算,上述过程中同时产生H2的质量为 g。
(3)计算电解后剩余溶液中NaCl的质量分数(写出详细的计算过程,结果精确到0.1%)。
请分析并计算回答:
(1)运用质量守恒定律可知上述反应中x= 。
(2)通过计算,上述过程中同时产生H2的质量为 g。
(3)计算电解后剩余溶液中NaCl的质量分数(写出详细的计算过程,结果精确到0.1%)。
2015·北京·一模 查看更多[1]
更新时间:2016-11-28 12:49:26
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】钢铁工业是国家的支柱产业之一。
(1)现有290t含四氧化三铁80%的磁铁矿石。这些矿石中含四氧化三铁的质量为______t。
(2)若用这些铁矿石炼铁,理论上可炼出含铁96%的生铁的质量是多少?(写出计算过程)
(3)查阅资料得知:CO与Fe2O3在不同条件下反应生成铁的同时,也会生成一些Fe3O4。某实验室用CO与Fe2O3在密闭容器中隔绝空气加强热来测试某温度下的反应结果,假如某次测试实验前后收集的数据如下表,请回答相关问题。
表中α的值为 ;容器内发生反应的化学方程式可表示为 。
(1)现有290t含四氧化三铁80%的磁铁矿石。这些矿石中含四氧化三铁的质量为______t。
(2)若用这些铁矿石炼铁,理论上可炼出含铁96%的生铁的质量是多少?(写出计算过程)
(3)查阅资料得知:CO与Fe2O3在不同条件下反应生成铁的同时,也会生成一些Fe3O4。某实验室用CO与Fe2O3在密闭容器中隔绝空气加强热来测试某温度下的反应结果,假如某次测试实验前后收集的数据如下表,请回答相关问题。
| 物质 | CO | Fe2O3 | Fe | Fe3O4 | CO2 |
| 反应前质量/g | 5.6 | 32 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.6 | α | 8.8 |
表中α的值为 ;容器内发生反应的化学方程式可表示为 。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】甲醇( CH3OH )是一种有毒,有酒的气味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应: 8CH3OH+nO2 mCO2+2CO + 16H2O。若反应生成3.6g 水,请计算:
mCO2+2CO + 16H2O。若反应生成3.6g 水,请计算:
①m值是____;
②参加反应的氧气质量是________克?(写出规范计算步骤)
 mCO2+2CO + 16H2O。若反应生成3.6g 水,请计算:
mCO2+2CO + 16H2O。若反应生成3.6g 水,请计算: ①m值是____;
②参加反应的氧气质量是________克?(写出规范计算步骤)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。小柯利用如图装置测定疏通剂中铝的质量分数。

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O=_____NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。_____

Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
| 反应前总质量m1 | 反应后总质量m2 |
| 371.84g | 371.24g |
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O=_____NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。_____
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
名校
【推荐1】小宇用配制的10%的CuSO4溶液测定一瓶NaOH溶液中溶质的质量分数。
(1)下图是配制CuSO4溶液的操作过程,正确的顺序是_________(填序号)。
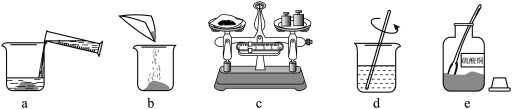
(2)取NaOH溶液25g,向其中加入10%的CuSO4溶液40g时恰好完全反应。则NaOH溶液中溶质的质量分数为______。
(1)下图是配制CuSO4溶液的操作过程,正确的顺序是_________(填序号)。

(2)取NaOH溶液25g,向其中加入10%的CuSO4溶液40g时恰好完全反应。则NaOH溶液中溶质的质量分数为______。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
解题方法
【推荐2】一定质量的金属铁和稀硫酸恰好完全反应,产生气体的质量为0.2 g。
(1)反应后溶液中溶质FeSO4的质量为_____g。
(2)向反应后的溶液中加入BaCl2溶液,当加入的BaCl2溶液质量为208 g时,恰好完全反应,此时生成沉淀的质量为________g。
(3)计算所加BaCl2溶液的溶质质量分数__________。
(1)反应后溶液中溶质FeSO4的质量为_____g。
(2)向反应后的溶液中加入BaCl2溶液,当加入的BaCl2溶液质量为208 g时,恰好完全反应,此时生成沉淀的质量为________g。
(3)计算所加BaCl2溶液的溶质质量分数__________。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】在一烧杯中盛有20g CaCl2和NaCl的混合固体粉末,向其中逐渐滴加溶质的质量分数为10.6%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示.请根据题意回答下列问题:
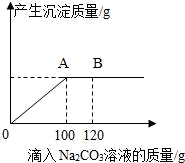
(1)当滴加了100gNa2CO3溶液时,产生沉淀质量为_____g.
(2)当滴加了120gNa2CO3溶液时,烧杯中溶液中的溶质是_____(写化学式).
(3)当滴加了100gNa2CO3溶液时,通过计算求此时所得不饱和溶液中溶质的质量分数_____.(计算结果精确至0.1%)

(1)当滴加了100gNa2CO3溶液时,产生沉淀质量为_____g.
(2)当滴加了120gNa2CO3溶液时,烧杯中溶液中的溶质是_____(写化学式).
(3)当滴加了100gNa2CO3溶液时,通过计算求此时所得不饱和溶液中溶质的质量分数_____.(计算结果精确至0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g。向烧杯中逐渐加入氧化铜并搅拌,烧杯中溶液的质量与加入氧化铜的质量关系如下图所示。当恰好完全反应时,所得的溶液为不饱和溶液。
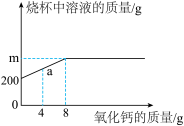
(1)m=_____ g。
(2)求原混合溶液中H2SO4的质量分数_____ (写出计算过程)。
(3)恰好完全反应时所得溶液中含有硫酸铜的质量为_____ g。
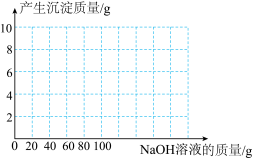
(4)取图象中a点对应的溶液,滴入8%的氢氧化钠溶液。请画出产生沉淀的质量随加入氢氧化钠溶液的质量的关系曲线_____ 。

(1)m=
(2)求原混合溶液中H2SO4的质量分数
(3)恰好完全反应时所得溶液中含有硫酸铜的质量为
(4)取图象中a点对应的溶液,滴入8%的氢氧化钠溶液。请画出产生沉淀的质量随加入氢氧化钠溶液的质量的关系曲线

您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】为测定某Cu-Zn合金中铜的质量分数,某同学将10g该合金放入到盛有40g稀硫酸的烧杯中,恰好反应后,测得烧杯中剩余物的质量为49.8g。
(1)生成氢气的质量为___________ g。
(2)计算原合金中铜的质量分数______ 。
(3)反应后所得溶液中溶质的质量分数_____ 。(结果保留一位小数)
(1)生成氢气的质量为
(2)计算原合金中铜的质量分数
(3)反应后所得溶液中溶质的质量分数
您最近一年使用:0次



