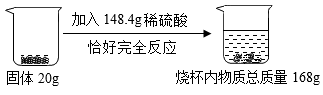
实验中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。

请根据以上信息计算:
(1)生成二氧化碳的质量为 1 克。
(2)样品中碳酸钙的质量分数为 2 。
(3)C烧杯中溶液的溶质质量分数 3 ?

请根据以上信息计算:
(1)生成二氧化碳的质量为
(2)样品中碳酸钙的质量分数为
(3)C烧杯中溶液的溶质质量分数
更新时间:2019-01-30 18:14:09
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】为了测定某化工厂由氯化钡和氯化钠组成的产品中氯化钠 的成分。小明取16.25g固体样品,全部溶于143.6g水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录如下图所示的曲线关系。
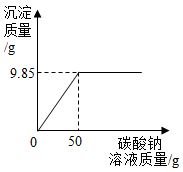
(1)产品中氯化钠的质量分数。
(2)当氯化钡与碳酸钠恰好完全反应时,所得溶液中溶质的质量分数。

(1)产品中氯化钠的质量分数。
(2)当氯化钡与碳酸钠恰好完全反应时,所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
名校
【推荐2】铜锌合金又叫黄铜,外观酷似黄金,极易以假乱真。某化学兴趣小组用图I所示装置测定黄铜中锌的含量。将足量的稀硫酸全部加入锥形瓶中,充分反应后天平示数的变化如图Ⅱ所示。请计算:

(1)生成氢气______g。
(2)黄铜样品中锌的质量分数。(写出计算过程)

(1)生成氢气______g。
(2)黄铜样品中锌的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】实验室有一变质的氢氧化钠样品(样品中只含碳酸钠杂质,且成分均匀),为测量样品中Na2CO3的质量分数,同学们取质量、大小相同的4个烧杯,分别加入一定质量分数的稀盐酸100g,再分别加入4份质量不同的样品,充分反应后记录实验数据如下:(注:Na2CO3+2HCl=2NaCl+H2O+CO2↑)
(1)碳酸钠(Na2CO3)中碳元素和氧元素的质量比为___________。
(2)第2组实验中生成CO2的质量为___________,表中m的值为___________。
(3)样品中Na2CO3的质量分数。
| 实验组别 | 1 | 2 | 3 | 4 |
| 反应前稀盐酸+烧杯质量(g) | 150 | 150 | 150 | 150 |
| 固体样品质量(g) | 5 | 10 | 15 | 20 |
| 反应后烧杯内物质+烧杯质量(g) | m | 157.8 | 161.7 | 166.0 |
(1)碳酸钠(Na2CO3)中碳元素和氧元素的质量比为___________。
(2)第2组实验中生成CO2的质量为___________,表中m的值为___________。
(3)样品中Na2CO3的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】石灰石是我市重要的自然资源,石灰石中碳酸钙的含量是影响其经济价值的重要指标。 某同学为帮助当地百姓测定某石灰石样品中碳酸钙的含量,进行了下图的实验(石灰石中的杂质不溶于水,也不与稀盐酸反应)。

(1)反应前把石灰石样品粉碎的目的是_____ 。
(2)计算此石灰石样品中碳酸钙的质量分数(写出计算过程,结果精确至0.1%)。

(1)反应前把石灰石样品粉碎的目的是
(2)计算此石灰石样品中碳酸钙的质量分数(写出计算过程,结果精确至0.1%)。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】为测定石灰石样品的纯度,取4g该样品,将40g稀盐酸平均分成4份,分4次加入到样品中,充分反应后测定剩余固体的质量,数据见下表。
(1)该石灰石样品中碳酸钙的质量分数是多少?
(2)求100g这种石灰石跟足量盐酸反应,生成二氧化碳的质量是多少?
| 次数 | 1 | 2 | 3 | 4 |
| 加入盐酸质量/g | 10 | 10 | 10 | 10 |
| 剩余固体质量/g | 2.5 | 1.0 | 0.4 | 0.4 |
(1)该石灰石样品中碳酸钙的质量分数是多少?
(2)求100g这种石灰石跟足量盐酸反应,生成二氧化碳的质量是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】石灰石的主要成分是碳酸钙。现取80.0g石灰石样品,平均分成四份分别与质量分数相同的盐酸反应来制备二氧化碳气体(杂质不与盐酸反应,也不溶于水),各组的实验数据如下表。
通过计算回答:
(1)上表格表m是多少?哪个组的组同学加入的盐酸恰好完全反应?
(2)该种石灰石样品中碳酸钙的质量分数为多少?(要求有计算过程)
| 实验分组 | 甲组 | 乙组 | 丙组 | 丁组 |
| 石灰石样品质量/g | 20.0 | 20.0 | 20.0 | 20.0 |
| 加入稀盐酸质量/g | 30.0 | 60.0 | 90.0 | 120.0 |
| 二氧化碳质量/g | 2.2 | m | 6.6 | 6.6 |
通过计算回答:
(1)上表格表m是多少?哪个组的组同学加入的盐酸恰好完全反应?
(2)该种石灰石样品中碳酸钙的质量分数为多少?(要求有计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐1】为测定某镁银合金中金属镁的含量,称取10g合金粉末放入一洁净烧杯中,量取200g稀硫酸平均分四次加入,充分反应后,测得实验数据记录如图:

(1)Y= 。
(2)计算所用硫酸溶质的质量分数。
(3)计算合金中金属镁的百分含量。

(1)Y= 。
(2)计算所用硫酸溶质的质量分数。
(3)计算合金中金属镁的百分含量。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】现有一包含有杂质的BaCl2固体样品(杂质不溶于水),为了研究样品的组成,进行了如下试验。请回答下列问题:

(1)实验发生反应的化学方程式为_____。
(2)列出求解硝酸银溶液中溶质质量(x)的比例式_____。
(3)200g固体样品加水充分溶解后,所得溶液的溶质质量分数为_____。
(4)在C烧杯加入多少克水使其中滤液的溶质质量分数为10%_____。
(5)向烧杯中加入硝酸银溶液的过程中,用数据说明滤液中溶质的变化情况是_____。
(6)样品中BaCl2的纯度为_____。

(1)实验发生反应的化学方程式为_____。
(2)列出求解硝酸银溶液中溶质质量(x)的比例式_____。
(3)200g固体样品加水充分溶解后,所得溶液的溶质质量分数为_____。
(4)在C烧杯加入多少克水使其中滤液的溶质质量分数为10%_____。
(5)向烧杯中加入硝酸银溶液的过程中,用数据说明滤液中溶质的变化情况是_____。
(6)样品中BaCl2的纯度为_____。
您最近一年使用:0次