取氯酸钾和二氧化锰的混合物26g,加热至混合物固体质量不再减少为止,冷却后称得剩余固体质量为16.4g ,将剩余固体加入一定量的水中,充分搅拌后过滤,滤液是10%的氯化钾溶液(假设溶液无损失)。计算:
(1)生成氧气的质量。
(2)二氧化锰的质量。
(3)氯化钾溶液中水的质量。
(1)生成氧气的质量。
(2)二氧化锰的质量。
(3)氯化钾溶液中水的质量。
更新时间:2019-01-30 18:14:09
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】150ml稀盐酸(密度1.1g/cm3)加入到盛有53g含少量杂质的石灰石的烧杯中,恰好反应(石灰石杂质不溶于水,也不与盐酸及生成物反应),反应后烧杯中物质的总质量为196g。计算:
(1)反应生成的二氧化碳的质量。
(2)石灰石中碳酸钙的质量分数。
(3)生成物溶液中溶质的质量分数。
(1)反应生成的二氧化碳的质量。
(2)石灰石中碳酸钙的质量分数。
(3)生成物溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某兴趣小组测定贝壳中碳酸钙的含量。现取 克贝壳捣碎,放入烧杯中,然后向其中加入
克贝壳捣碎,放入烧杯中,然后向其中加入 克稀盐酸,充分反应。
克稀盐酸,充分反应。 贝壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应
贝壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应 。测得烧杯中的反应剩余物的质量
。测得烧杯中的反应剩余物的质量

 与反应时间
与反应时间

 的关系如图所示
的关系如图所示 忽略水蒸气的挥发
忽略水蒸气的挥发 。
。
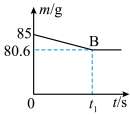
(1)产生二氧化碳的质量为______ g。
(2)该贝壳中碳酸钙的质量分数 结果保留
结果保留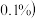
 克贝壳捣碎,放入烧杯中,然后向其中加入
克贝壳捣碎,放入烧杯中,然后向其中加入 克稀盐酸,充分反应。
克稀盐酸,充分反应。 贝壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应
贝壳中除碳酸钙外的其他成分都不溶于水,且不与稀盐酸反应 。测得烧杯中的反应剩余物的质量
。测得烧杯中的反应剩余物的质量

 与反应时间
与反应时间

 的关系如图所示
的关系如图所示 忽略水蒸气的挥发
忽略水蒸气的挥发 。
。
(1)产生二氧化碳的质量为
(2)该贝壳中碳酸钙的质量分数
 结果保留
结果保留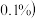
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进展了如下实验:取25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,向烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解),实验测得烧杯中剩余物质的质量与参加盐酸的质量之间的关系如下图:求:
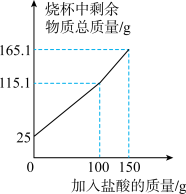
(1)产生CO2的总质量为___________ g。
(2)当加入稀盐酸___________ 克时鸡蛋壳样品已经完全反应?
(3)鸡蛋壳中碳酸钙的质量分数。

(1)产生CO2的总质量为
(2)当加入稀盐酸
(3)鸡蛋壳中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐1】某工厂采用烟气脱硫工艺,能消除二氧化硫,并将其转化为硫酸钙等产品,实现“变废为宝”,反应的化学方程式为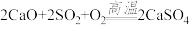 ,该工厂每天产生的二氧化硫的质量为3.2t。
,该工厂每天产生的二氧化硫的质量为3.2t。
(1)理论上该工厂每天需要氧化钙的质量是多少?
(2)该工厂燃烧的煤中含硫1.6%,若其中的硫元素全部转化为二氧化硫,该工厂每天消耗煤的质量为t。
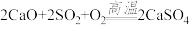 ,该工厂每天产生的二氧化硫的质量为3.2t。
,该工厂每天产生的二氧化硫的质量为3.2t。(1)理论上该工厂每天需要氧化钙的质量是多少?
(2)该工厂燃烧的煤中含硫1.6%,若其中的硫元素全部转化为二氧化硫,该工厂每天消耗煤的质量为t。
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐2】请回答并完成下列计算。
(1)实验室要配制50g溶质质量分数为8%的氢氧化钠溶液,需称取______g氢氧化钠固体。
(2)向上述配制好的溶液中加入50g稀硫酸,恰好完全反应,求反应后所得溶液中溶质的质量分数为__________。(反应的化学方程式:2NaOH + H2SO4==Na2SO4 + 2H2O)
(1)实验室要配制50g溶质质量分数为8%的氢氧化钠溶液,需称取______g氢氧化钠固体。
(2)向上述配制好的溶液中加入50g稀硫酸,恰好完全反应,求反应后所得溶液中溶质的质量分数为__________。(反应的化学方程式:2NaOH + H2SO4==Na2SO4 + 2H2O)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某碳酸钾样品中有少量氯化钾杂质,为测定样品中碳酸钾的含量,同学们进行了如下实验:称取该样品20g完全溶解在100g水中,加入100gCaCl2溶液时恰好完全反应,过滤后得到210g滤液。
请计算:
(1)生成沉淀的质量是__________________________g;
(2)该样品中碳酸钾的质量分数___________;
(3)所得溶液中溶质的质量分数_______________。(结果精确到0. 1% )
请计算:
(1)生成沉淀的质量是__________________________g;
(2)该样品中碳酸钾的质量分数___________;
(3)所得溶液中溶质的质量分数_______________。(结果精确到0. 1% )
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%-4.3%,钢中碳的含量为0.03%-2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示,注:碳既不溶于水也不与稀盐酸发生反应。
请根据相关信息完成下列计算:
(1)恰好完全反应时,生成氢气的质量为_________ g。
(2)通过计算判断样品是钢还是生铁____________ ?(计算结果保留到0%)
(3)反应后得到的溶液中溶质的质量分数____________ 。(计算结果保留到0.1%)
| 烧杯质量 | 样品的质量 | 稀盐酸的质量 | 烧杯+剩余物的总质量 |
| 50g | 5.8g | 94.6g | 150.2g |
请根据相关信息完成下列计算:
(1)恰好完全反应时,生成氢气的质量为
(2)通过计算判断样品是钢还是生铁
(3)反应后得到的溶液中溶质的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】为了测定某铜、锌合金的组成,称取10g该合金粉末,在粉末中连续6次加入稀硫酸反应,每加一次稀硫酸,记录完全反应后所得剩余固体的质量,实验数据如下:
(注意:以下各题,只要求填写计算结果,不要求写计算过程)
(1)据表中数据,计算该合金中锌的质量为 ;
(2)计算所加稀硫酸的溶质的质量分数为 (精确到0.1%);
(3)计算恰好完全反应后所得溶液的溶质的质量分数为 (精确到0.1%)。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g)[ | 8.7 | 7.4 | 6.1 | 4.8 | 3.5 | 3.5 |
(1)据表中数据,计算该合金中锌的质量为 ;
(2)计算所加稀硫酸的溶质的质量分数为 (精确到0.1%);
(3)计算恰好完全反应后所得溶液的溶质的质量分数为 (精确到0.1%)。
您最近一年使用:0次




