某实验小组的同学为了测定实验室中氯酸钾样品的杂质含量,取一定质量的该样品与1g二氧化锰混合,其总质量为6g,然后依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
试计算:
(1)完全反应后产生的氧气的总质量是_____ ;
(2)原样品中杂质的质量是多少?_____ 。
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 4.24 | 4.16 | 4.08 | 4.08 |
(1)完全反应后产生的氧气的总质量是
(2)原样品中杂质的质量是多少?
更新时间:2016-11-28 13:34:09
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】把9.6g镁条粉放在给定质量的氧气中燃烧,有关实验数据如下表所示。请回答下列问题:
(1)在该反应中,参加反应的Mg和O2的微粒个数比为:________;
(2)第一次实验中,参加反应的Mg的质量为_____g;第二次实验中,参加反应的Mg和生成的MgO的质量比为:_______(写最简整数比);
(3)计算第三次试验中生成MgO的质量。
| 实验编号 | ① | ② | ③ |
| O2的质量(g) | 2.4 | 3.2 | 9.6 |
| MgO的质量(g) | 6 |
(1)在该反应中,参加反应的Mg和O2的微粒个数比为:________;
(2)第一次实验中,参加反应的Mg的质量为_____g;第二次实验中,参加反应的Mg和生成的MgO的质量比为:_______(写最简整数比);
(3)计算第三次试验中生成MgO的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为了检测石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学分别用质量分数相同的盐酸与样品充分反应进行试验测定。(样品中的杂质不含钙元素,不溶与水,且不与盐酸反应)。测得数据如下表:
请回答:
(1)10.0g样品与45.0g盐酸充分反应后,盐酸是否还有剩余______ (是或否);
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程)
(3)有一种含碳酸钙和氧化钙的混合物,测得其中钙元素的质量分数为50%。取该混合物16g,经高温煅烧后,将所得剩余固体全部投入足量盐酸中,固体全部溶解生成氯化钙,则生成氯化钙的质量为______ 。
| 1 | 甲 | 乙 | 丙 | 丁 |
| 所取石灰石样品质量/g | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量/g | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量/g | 6.0 | 4.0 | 2.0 | 2.0 |
请回答:
(1)10.0g样品与45.0g盐酸充分反应后,盐酸是否还有剩余
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程)
(3)有一种含碳酸钙和氧化钙的混合物,测得其中钙元素的质量分数为50%。取该混合物16g,经高温煅烧后,将所得剩余固体全部投入足量盐酸中,固体全部溶解生成氯化钙,则生成氯化钙的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在实验室里,常用稀盐酸与大理石或石灰石反应来制取二氧化碳气体。现称取12.5克大理石样品放入锥形瓶中,再向锥形瓶中滴加稀盐酸(杂质不参加反应),稀盐酸的用量与产生二氧化碳的质量关系如图所示,请你计算:
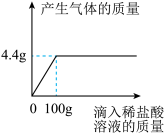
(1)恰好完全反应时锥形瓶中剩余物质的总质量是_______克。
(2)大理石样品中碳酸钙的质量分数是多少?_________

(1)恰好完全反应时锥形瓶中剩余物质的总质量是_______克。
(2)大理石样品中碳酸钙的质量分数是多少?_________
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】用氯酸钾制取氧气,化学方程式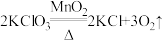 。现将 28.8g 氯酸钾与 6.6g二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.8g。回答:
。现将 28.8g 氯酸钾与 6.6g二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.8g。回答:
(1)生成氧气的质量____________ ;
(2)通过计算后,判断固体剩余物中____________ (填“含”或“不含”)有氯酸钾;
(3)列式计算剩余固体中氯化钾的质量为。____________ 。
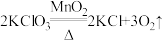 。现将 28.8g 氯酸钾与 6.6g二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.8g。回答:
。现将 28.8g 氯酸钾与 6.6g二氧化锰的混合物加热一段时间后,冷却,称量剩余固体的质量为 25.8g。回答:(1)生成氧气的质量
(2)通过计算后,判断固体剩余物中
(3)列式计算剩余固体中氯化钾的质量为。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某实长小组同学用氯酸钾和二氧化锰的混合物制取氧气。取一定质量的氯酸钾与1g二氧化锰混合,依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表
试计算:(1)完全反应后产生的氧气的总质量为_____g。
(2)原氯酸钾和二氧化锰的总质量是多少?_____
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 3.20 | 2.88 | 2.49 | 2.49 |
试计算:(1)完全反应后产生的氧气的总质量为_____g。
(2)原氯酸钾和二氧化锰的总质量是多少?_____
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】小明同学用不纯的氯酸钾样品(杂质受热不分解)与2g二氧化锰混合放在大试管中加热制取氧气,测得试管中剩余固体的质量与反应时间的关系如图所示。求:
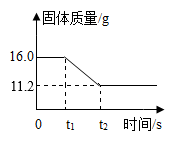
(1)氯酸钾在_______ 时刻开始分解。
(2)小明同学共制得氧气_________ g。
(3)小明所用样品中氯酸钾的质量是多少?(写出计算过程)。

(1)氯酸钾在
(2)小明同学共制得氧气
(3)小明所用样品中氯酸钾的质量是多少?(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某化学兴趣小组同学取氯酸钾和二氧化锰的混合物15.5g加热来制取氧气。测得反应时间与剩余固体的质量如下表所示:
(1)T3时刻产生氧气的质量是______ g。
(2)该小组取用的氯酸钾的质量是多少?(用化学方程式计算,下同)
(3)T2时刻,剩余固体中氯元素的质量分数是______ 。
| 反应时间 | T0 | T1 | T2 | T3 | T4 | T5 | T6 |
| 剩余固体质量 | 15.5 | 15.5 | 14.2 | 12.2 | 11.1 | 10.7 | 10.7 |
(1)T3时刻产生氧气的质量是
(2)该小组取用的氯酸钾的质量是多少?(用化学方程式计算,下同)
(3)T2时刻,剩余固体中氯元素的质量分数是
您最近一年使用:0次



