以下是对实验室制取氧气的条件进行的探究。
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计了以下对比实验:①将3.0g氯酸钾与1.0g二氧化锰混合加热;②将xg氯酸钾与1.0g氧化铜均匀混合加热;在相同的温度下,比较两组实验产生氧气的快慢
①中的化学方程式是:_________
②中x的值应为:________
(2)乙同学探究了影响过氧化氢分解速度的某种因素,数据如下:
由上表可得到的结论是,在相同条件下, __________ ,过氧化氢分解得越快。
(3)丙同学用如图装置进行影响过氧化氢分解速度某种因素的实验探究,通过________ 比较,也能达到实验目的。
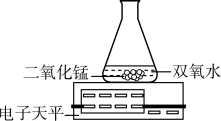
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲同学设计了以下对比实验:①将3.0g氯酸钾与1.0g二氧化锰混合加热;②将xg氯酸钾与1.0g氧化铜均匀混合加热;在相同的温度下,比较两组实验产生氧气的快慢
①中的化学方程式是:
②中x的值应为:
(2)乙同学探究了影响过氧化氢分解速度的某种因素,数据如下:
| 编号 | 过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | 二氧化锰的质量 | 相同时间内产生氧气的体积 |
| ① | 50.0g | 1% | 0.1g | 9mL |
| ② | 50.0g | 2% | 0.1g | 16mL |
| ③ | 50.0g | 4% | 0.1g | 31mL |
(3)丙同学用如图装置进行影响过氧化氢分解速度某种因素的实验探究,通过

更新时间:2016/11/28 13:40:08
|
相似题推荐
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】现有一包白色粉末可能由氢氧化钠、硫酸钠、碳酸钠、无水硫酸铜中的一种或几种组成。某同学欲探究这一粉末的组成,现做如下实验:
(1)步骤一:取少量白色粉末于试管中,加入足量蒸馏水,得无色透明溶液,由此可知,粉末中一定不含有_____ (填物质的化学式)
(2)步骤二:再取少量白色粉末于试管中,并滴加过量的稀盐酸,观察到_____ , 说明粉末中一定含有碳酸钠,请写出该反应的化学方程式是_____
(3)请你根据该同学实验所得现象,推测这一粉末的可能组成。
推测一:碳酸钠 推测二:碳酸钠、氢氧化钠;
推测三:碳酸钠、硫酸钠 推测四:_____
(4)若要证明推测三成立(即该粉末由碳酸钠、硫酸钠组成),请你在该同学实验基础上设计后续实验,以确定这包粉末的组成。
(1)步骤一:取少量白色粉末于试管中,加入足量蒸馏水,得无色透明溶液,由此可知,粉末中一定不含有
(2)步骤二:再取少量白色粉末于试管中,并滴加过量的稀盐酸,观察到
(3)请你根据该同学实验所得现象,推测这一粉末的可能组成。
推测一:碳酸钠 推测二:碳酸钠、氢氧化钠;
推测三:碳酸钠、硫酸钠 推测四:
(4)若要证明推测三成立(即该粉末由碳酸钠、硫酸钠组成),请你在该同学实验基础上设计后续实验,以确定这包粉末的组成。
| 实验操作 | 预期现象和必要结论 |
| 步骤.1:取少量该同学做的步骤二反应后的溶液于试管中,加入 | |
| 步骤2:重新取少量白色粉末于试管中,加足量蒸馏水溶解,加入 | |
| 步骤3:取少量 |
您最近一年使用:0次
【推荐2】人类的生产、生活离不开金属材料,金属材料的应用推动了社会发展。
(1)下列出土文物中属于金属材料的是___________(填字母序号)。
(2)铁是目前使用最广的金属,请写出工业上以赤铁矿为原料炼铁的化学方程式:___________ 。
(3)被誉为“中国天眼”的FAST,是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰。某小组同学探究这三种金属的活动性顺序,请你参与:
【猜想】猜想①:Mn>Fe>Cu;猜想②:Fe>Mn>Cu;猜想③:___________ 。
【实验】
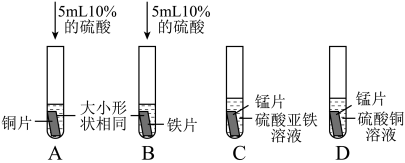
①能验证铁、铜活动性顺序的现象是___________ 。
②C中可观察到明显的现象,反应的化学方程式为___________ (已知锰元素在生成物中显+2价)。
③通过以上实验,证明猜想___________ 正确。实验A~D中不需要做的实验是___________ (填序号)。
(4)实验后,对所用金属片进行回收,其意义是___________ (写一条即可)。
(1)下列出土文物中属于金属材料的是___________(填字母序号)。
| A.青铜大立人 | B.金面具 | C.象牙 | D.玉石器 |
(3)被誉为“中国天眼”的FAST,是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰。某小组同学探究这三种金属的活动性顺序,请你参与:
【猜想】猜想①:Mn>Fe>Cu;猜想②:Fe>Mn>Cu;猜想③:
【实验】

①能验证铁、铜活动性顺序的现象是
②C中可观察到明显的现象,反应的化学方程式为
③通过以上实验,证明猜想
(4)实验后,对所用金属片进行回收,其意义是
您最近一年使用:0次
【推荐3】同学们在化学实验课上完成了金属活动性顺序的探究实验,请你与他们一起完成实验报告。
实验活动探究Al、Cu、Ag的金属活动性顺序
【实验目的】探究常见金属的活动性顺序。
【实验用品】
(1)砂纸,量筒,胶头滴管,______ ,铝丝,铜丝,银丝,硫酸铝溶液,硫酸铜溶液,硝酸银溶液,稀盐酸。
【实验步骤】
如图所示,在两支试管中分别加入5mL的硫酸铝溶液和硝酸银溶液,将两根用砂纸打磨光亮的铜丝分别浸入硫酸铝溶液和硝酸银溶液中,过一会儿取出,观察现象。
铜丝浸入硫酸铝溶液中,无明显现象。
(2)铜丝浸入硝酸银溶液中,现象是______ 。
【实验结论】
(3)三种金属的活动性由强到弱的顺序为______ 。
【问题与交流】
(4)写出试管②中发生反应的化学方程式:______ 。
(5)从【实验用品】中另选一组药品进行实验也能得出相同的实验结论,写出你选出的另一组药品:______ 。
实验活动探究Al、Cu、Ag的金属活动性顺序
【实验目的】探究常见金属的活动性顺序。
【实验用品】
(1)砂纸,量筒,胶头滴管,
【实验步骤】
如图所示,在两支试管中分别加入5mL的硫酸铝溶液和硝酸银溶液,将两根用砂纸打磨光亮的铜丝分别浸入硫酸铝溶液和硝酸银溶液中,过一会儿取出,观察现象。
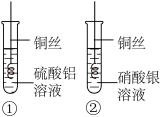
铜丝浸入硫酸铝溶液中,无明显现象。
(2)铜丝浸入硝酸银溶液中,现象是
【实验结论】
(3)三种金属的活动性由强到弱的顺序为
【问题与交流】
(4)写出试管②中发生反应的化学方程式:
(5)从【实验用品】中另选一组药品进行实验也能得出相同的实验结论,写出你选出的另一组药品:
您最近一年使用:0次
【推荐1】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与_________ 有关。
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2红砖粉后测量各生成一瓶(相同体积)O2所需要的时间。
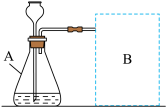
【进行实验】如图是他们进行实验的装置图,气体发生装置中A仪器名称是________ ,此实验中B处宜采用的气体收集方法是_____________
【结论】________
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_________ 和_________ 是否改变。
【假设】H2O2生成O2的快慢与
【实验方案】常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量MnO2红砖粉后测量各生成一瓶(相同体积)O2所需要的时间。
【进行实验】如图是他们进行实验的装置图,气体发生装置中A仪器名称是

【结论】
【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的
实验编号 | 1 | 2 |
反应物 | 6%H2O2溶液 | 6%H2O2溶液 |
催化剂 | 1 g红砖粉 | 1 g MnO2 |
时间 | 152 秒 | 35 秒 |
您最近一年使用:0次
【推荐2】学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝(Al2O3)是否也可作过氧化氢分解的催化剂。
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂。
(1)【实验验证】
(2)【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂。
【反思提高】经过讨论,有的同学认为只有上述不能证明Al2O3能作过氧化氢分解的催化剂,其原因是催化剂的特点为______ ;因此还要补充一个探究实验三:目的是探究______ 。
(3)【实验三】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、______ ;④对比反应前后Al2O3的质量。
(4)【交流讨论】Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
【深入反思】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验,实验的目的是探究______ 。该实验的操作方法为______ 。
(5)经过实验证明,Al2O3可作为过氧化氢分解的催化剂,用Al2O3作催化剂其反应文字表达式为______ 。
【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢?
【作出猜想】Al2O3能作过氧化氢分解的催化剂。
(1)【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 有少量气泡,木条不复燃 | 常温下过氧化氢溶液分解速率很慢。 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3, 然后将带火星的木条伸入试管中 | 产生大量的气泡,木条复燃 |
【反思提高】经过讨论,有的同学认为只有上述不能证明Al2O3能作过氧化氢分解的催化剂,其原因是催化剂的特点为
(3)【实验三】①准确称量Al2O3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、干燥、
(4)【交流讨论】Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂。
【深入反思】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验,实验的目的是探究
(5)经过实验证明,Al2O3可作为过氧化氢分解的催化剂,用Al2O3作催化剂其反应文字表达式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小峰同学腿部轻微擦伤,医务室的大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产生了小气泡,很好奇。
【提出问题】为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
请写出过氧化氢分解的化学方程式_____________ ;
【查阅资料】①人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是 37℃
【提出猜想】猜想一:过氧化氢分解加快是因为人体温比医用瓶的温度高
猜想二:过氧化氢分解加快是因为体温下伤口中有过氧化氢酶。
【实验探究】小峰用下图装置测定过氧化氢分解的快慢。若要检验生成的气体是否为氧气,采取的方法是___________ ;
【提出质疑】小红认为小峰通过实验①和②得出“猜想二”成立的结论不严密,理由是________ ;
【得出结论】 猜想二成立
【反思交流】 除了上述因素会影响过氧化氢分解速度外,_____ (写一种)也会影响过氧化氢分解速度;
【拓展延伸】决定化学反应速率的主要因素有______ (填字母)。
A.反应物的浓度 B.反应温度 C.使用催化剂 D.反应物的性质。
【提出问题】为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
请写出过氧化氢分解的化学方程式
【查阅资料】①人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是 37℃
【提出猜想】猜想一:过氧化氢分解加快是因为人体温比医用瓶的温度高
猜想二:过氧化氢分解加快是因为体温下伤口中有过氧化氢酶。
【实验探究】小峰用下图装置测定过氧化氢分解的快慢。若要检验生成的气体是否为氧气,采取的方法是
| 实验步骤 | 实验现象 | 实验结论 | |
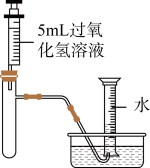 实验开始时,用注射器向试管中注入相同浓度的过氧化氢溶液,并用排水法收集氧气,记录2分钟收集的气体体积。 | ①分两次进行实验,均注入5mL过氧化氢溶液: 第一次在常温下进行 第二次将试管浸在 | 量筒中2分钟收集到的气体体积均为5mL | |
| ②分两次进行实验: 第一次向试管中加入5mL 过氧化氢溶液,将试管浸在37℃的温水中,观察。 第二次将装有一小粒过氧化氢酶的试管浸在 37℃的温水中,注入5mL 过氧化氢溶液。 | 第一次,量筒中2分钟收集到的气体体积为5mL, 第二次,量筒中2分钟收集到的气体体积为 | 猜想二 成立 | |
【得出结论】 猜想二成立
【反思交流】 除了上述因素会影响过氧化氢分解速度外,
【拓展延伸】决定化学反应速率的主要因素有
A.反应物的浓度 B.反应温度 C.使用催化剂 D.反应物的性质。
您最近一年使用:0次
【推荐1】实验室常用加热氯酸钾与二氧化锰的混合物的方法制取氧气。某化学兴趣小组发现:氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】:除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
【分析数据,得出结论】
(1)实验D中x的值应为________ ,由实验_______ 与实验D对比,证明猜想合理.
(2)实验所用的三种物质中,催化效果最好的是___________________ 。
【反思】若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和______ 不变。
【继续探究】小组同学完成上述实验后,又深一步进行“氧化铜用量与一定质量氯酸钾制取氧气反应速率关系”的探究,下表是他们的有关实验数据,请你回答有关问题:
【分析整理】
(3)据上表可知氧化铜用量过多,产生氧气的速率_________ (填“变快”、“变慢”或“不变”),氧化铜与氯酸钾的质量比为_____________ 时,反应速率最快。
【结论】在化学反应中催化剂的用量______ (填“是”或“不是”)越多越好。
【提出猜想】:除二氧化锰、氧化铜外,氧化铁也可以作氯酸钾分解的催化剂。
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好)。
| 实验编号 | 实验用品 | 分解温度 |
| A | 3.0g氯酸钾 | 580 |
| B | 3.0g氯酸钾和1.0g二氧化锰 | 350 |
| C | 3.0g氯酸钾和1.0g氧化铜 | 370 |
| D | x g氯酸钾和1.0g氧化铁 | 390 |
【分析数据,得出结论】
(1)实验D中x的值应为
(2)实验所用的三种物质中,催化效果最好的是
【反思】若要证明氧化铁是该反应的催化剂,还要验证它在化学反应前后的质量和
【继续探究】小组同学完成上述实验后,又深一步进行“氧化铜用量与一定质量氯酸钾制取氧气反应速率关系”的探究,下表是他们的有关实验数据,请你回答有关问题:
| 氧化铜与氯酸钾的质量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
| 生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
【分析整理】
(3)据上表可知氧化铜用量过多,产生氧气的速率
【结论】在化学反应中催化剂的用量
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】为做好实验室制取氧气的实验活动和评价,某兴趣小组的师生共同讨论并确定了如表所示的评价标准。
你是该小组成员,参与完成下列实验活动。
(1)选择实验方案。实验室可提供三种制取氧气的方案:
A.加热高锰酸钾
B.加热混有二氧化锰的氯酸钾
C.催化分解过氧化氢
如果你选方案B,对应反应的文字表达式为_______ 。
(2)进行实验活动。小组同学分工协作完成如下任务:
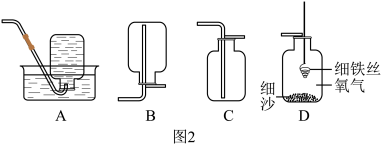
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡胶塞、水槽、试管,还应根据如图1所提供的的仪器,选择酒精灯和________ 。(填仪器名称)
③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注意到试管口应略向下的倾斜,这样做的原因是_______ 。
④你负责排水法收集氧气。开始收集的时机是________ 。收集到两瓶气体,均呈红色。
⑤用如图2中D装置做细铁丝燃烧的实验,收集所需氧气最好选用的装置是_______ (填序号,下同);做硫燃烧实验,收集所需氧气最好选用的装置是________ 。由此可见,选择气体的收集方法主要应考虑气体的性质,此外往往还要考虑________ 。
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改进意见是_______ 。
你是该小组成员,参与完成下列实验活动。
| 评价标准 |
| 1.是否根据实验条件选择实验方案,并进行可行性论证 |
| 2.是否积极参与实验操作活动,并善于与同学合作 |
| 3.是否规范取用药品,节约药品,保持实验台整洁 |
| 4.是否客观准确记录实验现象,并交流实验成果 |
| 5.是否体验到实验探究活动的乐趣 |
(1)选择实验方案。实验室可提供三种制取氧气的方案:
A.加热高锰酸钾
B.加热混有二氧化锰的氯酸钾
C.催化分解过氧化氢
如果你选方案B,对应反应的文字表达式为
(2)进行实验活动。小组同学分工协作完成如下任务:
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡胶塞、水槽、试管,还应根据如图1所提供的的仪器,选择酒精灯和

③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注意到试管口应略向下的倾斜,这样做的原因是
④你负责排水法收集氧气。开始收集的时机是
⑤用如图2中D装置做细铁丝燃烧的实验,收集所需氧气最好选用的装置是
(3)评价与反思。小组同学都认为体验到了实验活动的乐趣,但因实验过程存在不足,同意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改进意见是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小金进行如图所示实验来验证质量守恒定律。在实验中用电子天平和量筒准确测量出表中m1、m2、m3和V。(实验中操作正确,试管中原有空气体积忽略,O2的密度为ρg/cm3)。
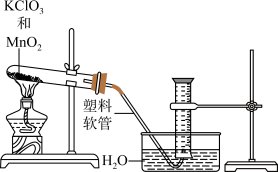
(1)给试管中的固体加热时,发现试管炸裂,可能原因为___________ 。
A 试管外壁干燥
B 试管接触灯芯
C 试管口朝向人
D 试管口没有略向下倾斜
(2)根据质量守恒定律,m1、m2、m3和V和p之间应存在的等量关系为___________ ;
(3)每次实验结束后,小金在拆卸装置时总能闻到刺激性气味。他将加热后剩余固体中的MnO2分离并测量其质量,发现总小于加热前MnO2的质量。查阅资料后发现,一般认为加热KClO3和MnO2混合物的反应过程如下:
第1步: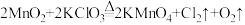 ;(其中Cl2有刺激性气味)
;(其中Cl2有刺激性气味)
第2步:
第3步: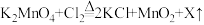 。
。
①第3步中X的化学式为___________ 。
②写出加热后剩余固体中MnO2质量小于加热前MnO2质量的原因___________ 。

| 实验序号 | 1 | 2 | … |
| m1(MnO2)/g | |||
| m2(试管+KC1O3)/g | |||
| m3(试管+加热后剩余固体)/g | |||
| 量筒内收集气体的体积V/cm3 |
A 试管外壁干燥
B 试管接触灯芯
C 试管口朝向人
D 试管口没有略向下倾斜
(2)根据质量守恒定律,m1、m2、m3和V和p之间应存在的等量关系为
(3)每次实验结束后,小金在拆卸装置时总能闻到刺激性气味。他将加热后剩余固体中的MnO2分离并测量其质量,发现总小于加热前MnO2的质量。查阅资料后发现,一般认为加热KClO3和MnO2混合物的反应过程如下:
第1步:
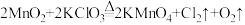 ;(其中Cl2有刺激性气味)
;(其中Cl2有刺激性气味)第2步:

第3步:
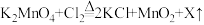 。
。①第3步中X的化学式为
②写出加热后剩余固体中MnO2质量小于加热前MnO2质量的原因
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】某实验小组利用压强传感器采集实验数据,探究外界条件对双氧水分解速率的影响。请回答下列问题:
(1)实验室用过氧化氢制取氧气的化学方程式为______ 。
(2)通过实验①和②对比可知,该化学反应快慢与______ 有关。
(3)实验②和③探究的是______ 对过氧化氢溶液分解速率的影响。
(4)已知 和
和 都对过氧化氢分解起催化作用,且
都对过氧化氢分解起催化作用,且 催化效果比
催化效果比 更好。用含
更好。用含 溶液的实验结果如图所示,请在图中画出滴加含
溶液的实验结果如图所示,请在图中画出滴加含 溶液时气体压强变化曲线图(t时刻内过氧化氢溶液未完全分解)。
溶液时气体压强变化曲线图(t时刻内过氧化氢溶液未完全分解)。
| 实验序号 | 过氧化氢溶液 浓度/% | 过氧化氢溶液 体积/mL | 二氧化锰 用量/g | 反应条件 |
| ① | 2 | 12 | 0.2 | 常温 |
| ② | 5 | 12 | 0.2 | 常温 |
| ③ | 5 | 12 | — | 常温 |
(1)实验室用过氧化氢制取氧气的化学方程式为
(2)通过实验①和②对比可知,该化学反应快慢与
(3)实验②和③探究的是
(4)已知
 和
和 都对过氧化氢分解起催化作用,且
都对过氧化氢分解起催化作用,且 催化效果比
催化效果比 更好。用含
更好。用含 溶液的实验结果如图所示,请在图中画出滴加含
溶液的实验结果如图所示,请在图中画出滴加含 溶液时气体压强变化曲线图(t时刻内过氧化氢溶液未完全分解)。
溶液时气体压强变化曲线图(t时刻内过氧化氢溶液未完全分解)。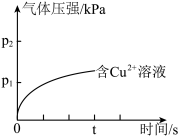
| 实验序号 | 过氧化氢溶液 浓度/% | 过氧化氢溶液 体积/mL | 二氧化锰 用量/g | 反应条件 |
| ④ |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某学习小组的同学对过氧化氢分解进行探究。
I.【探究一】影响过氧化氢分解快慢的因素
分别取5mLH2O2溶液进行实验,测定产生4mLO2所需时间,实验结果记录如下:
(1)对比①②可知,其他条件相同时,温度越高,过氧化氢分解越快,则t1_____ t2(填“>”“二”或“<”)。
(2)能说明过氧化氢分解快慢与溶质质量分数有关的实验是_________ (填实验序号),合理的结论是______ 。
【交流探讨】MnO2属于金属氧化物,其他金属氧化物能否起到类似MnO2的催化作用?
II.[探究二]探究FerOs是否对过氧化氢分解起催化作用。
【得出结论】Fe2O3能对过氧化氢的分解起催化作用。
I.【探究一】影响过氧化氢分解快慢的因素
分别取5mLH2O2溶液进行实验,测定产生4mLO2所需时间,实验结果记录如下:
| 实验序号 | H2O2溶液的溶质质量分数% | 温度℃ | MnO2粉末用量 | 反应时间 |
| ① | 30 | 35 | 0 | t1 |
| ② | 30 | 55 | 0 | t2 |
| ③ | 5 | 20 | 0.1 | 3s |
| ④ | 15 | 20 | 0.1 | 1s |
(2)能说明过氧化氢分解快慢与溶质质量分数有关的实验是
【交流探讨】MnO2属于金属氧化物,其他金属氧化物能否起到类似MnO2的催化作用?
II.[探究二]探究FerOs是否对过氧化氢分解起催化作用。
| 操作步骤 | 实验情况记录 | 结论 | |
| (1) |  | A试管上方带火星的木条未复燃,B中出现气泡快,带火星的木条复燃现象 | Fe2O3 |
| (2) | 将B试管中的混合物 | 固体质量为0.2 g | Fe2O3质量未变 |
| (3) | 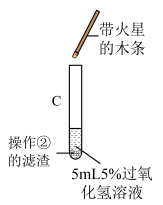 | C试管上方带火星的木条 | Fe2O3化学性质未变 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】实验小组的同学开展活性炭脱色效果的研究。脱色效果以过滤后滤液颜色为参照。
【查阅资料】活性炭具有吸附性。活性炭活化:将活性炭放入坩埚中,盖上盖子,放进马弗炉中加热至900°C并保温6h。
【进行实验】用活性炭对某品牌的陈醋进行系列脱色实验,每次实验量取5mL深褐色陈醋,实验记录如下:
【解释与结论】
(1)量取陈醋时,应选用______ (填“10”“50”或“100”)mL量筒。
(2)⑦比③的脱色效果好,其原因是_________ 。
(3)依据实验④-⑥得出的结论是_________ 。
(4)依据实验数据,得出“静置时间相同时,振荡比不振荡,活性炭脱色效果好”的结论,依据的实验是_____ (填序号)。
【反思与评价】
(5)继续实验,发现活化后的活性炭能明显提高脱色效率,其实验操作为:量取5.0mL深褐色陈醋,______ 。
【查阅资料】活性炭具有吸附性。活性炭活化:将活性炭放入坩埚中,盖上盖子,放进马弗炉中加热至900°C并保温6h。
【进行实验】用活性炭对某品牌的陈醋进行系列脱色实验,每次实验量取5mL深褐色陈醋,实验记录如下:
| 实验序号 | 活性炭质量/g | 振荡时间/s | 静置时间/min | 滤液颜色 |
| ① | 0.2 | 30 | 6 | 褐色 |
| ② | 0.3 | 30 | 60 | 淡黄色 |
| ③ | 0.4 | 30 | 60 | 近无色 |
| ④ | 0.5 | 0 | 5 | 淡黄色 |
| ⑤ | 0.5 | 0 | 8 | 近无色 |
| ⑥ | 0.5 | 0 | 10 | 无色 |
| ⑦ | 0.5 | 30 | 5 | 无色 |
| ⑧ | 0.5 | 30 | 8 | 无色 |
| ⑨ | 0.5 | 30 | 10 | 无色 |
(1)量取陈醋时,应选用
(2)⑦比③的脱色效果好,其原因是
(3)依据实验④-⑥得出的结论是
(4)依据实验数据,得出“静置时间相同时,振荡比不振荡,活性炭脱色效果好”的结论,依据的实验是
【反思与评价】
(5)继续实验,发现活化后的活性炭能明显提高脱色效率,其实验操作为:量取5.0mL深褐色陈醋,
您最近一年使用:0次



