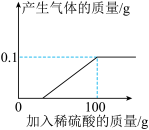
硫酸锌片在医药方面可用于治疗食欲不振、发育不良等症状,实验室可用锌和稀硫酸反应制得。学校化学兴趣小组的同学取一块表面严重氧化的锌片7.3g(不含其它杂质),剪碎,向其中慢慢滴加9.8%的稀硫酸,至恰好完全反应时,用去稀硫酸100g,并绘出如图所示的图像。
(1)小组同学在老师的指导下,配制200g 9.8%的稀硫酸;
①用98%的浓硫酸配制200g 9.8%的稀硫酸,需加水_______ g;
②将配制好的稀硫酸转移到试剂瓶中,贴上标签,标签上必须注明的是_______ (填序号)
A、200g B、9.8% C、稀硫酸
③下列操作中的_________ (填序号),可能会导致配制的溶液的溶质的质量分数低于9.8%
A、量取浓硫酸后,置于空气中时间过长
B、量水时,俯视量筒刻度
C、配制前将烧杯用水冲洗干净,没有擦干
(2)生成0.1g氢气消耗的稀硫酸的质量是多少?
____________________ (请写出完整的计算过程)。

(1)小组同学在老师的指导下,配制200g 9.8%的稀硫酸;
①用98%的浓硫酸配制200g 9.8%的稀硫酸,需加水
②将配制好的稀硫酸转移到试剂瓶中,贴上标签,标签上必须注明的是
A、200g B、9.8% C、稀硫酸
③下列操作中的
A、量取浓硫酸后,置于空气中时间过长
B、量水时,俯视量筒刻度
C、配制前将烧杯用水冲洗干净,没有擦干
(2)生成0.1g氢气消耗的稀硫酸的质量是多少?
更新时间:2016-11-28 14:05:02
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】兴趣小组同学用如图装置测定一定量某生铁样品中所含铁的质量。向生铁样品中加入足量稀硫酸,待反应完全后,调整漏斗高度,正确读出生成氢气的体积为222mL(已知:氢气密度约为0.09g/L;生铁样品中其他成分不参与反应)。
(2)小文认为利用上述装置进行实验,最终测量出的铁的含量偏大,可能的原因是_______ 。

(2)小文认为利用上述装置进行实验,最终测量出的铁的含量偏大,可能的原因是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品。为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
按要求回答下列问题:
(1)根据实验数据分析,从第________份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数。(要求写出计算过程)
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
| 取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
| 产生气体质量(g) | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |
按要求回答下列问题:
(1)根据实验数据分析,从第________份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数。(要求写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在实验室中,配制 300g 浓度10%过氧化氢,
(1)配制步骤:
①计算:需要 30%的过氧化氢溶液质量为______g;
②量取;
③______;
④装瓶贴签。
(2)现取 68g 浓度10%的过氧化氢溶液,最多能制取氧气多少克?
(1)配制步骤:
①计算:需要 30%的过氧化氢溶液质量为______g;
②量取;
③______;
④装瓶贴签。
(2)现取 68g 浓度10%的过氧化氢溶液,最多能制取氧气多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】向一定质量的石灰石中加入溶质质量分数为7.3%的稀盐酸制取二氧化碳,测得反应中溶液的pH与加入稀盐酸的质量关系如图所示。(请完整写出计算过程,结果保留1位小数)

(1)实验中共产生多少克二氧化碳?
(2)实验室用36%的浓盐酸(密度为1.2g/mL)来配制7.3%的稀盐酸,配制180g稀盐酸需要浓盐酸多少毫升?

(1)实验中共产生多少克二氧化碳?
(2)实验室用36%的浓盐酸(密度为1.2g/mL)来配制7.3%的稀盐酸,配制180g稀盐酸需要浓盐酸多少毫升?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】如图是同学们构建关于O2的知识图,请根据图中信息回答问题:
(2)实验室需要配置100g 9.8%浓度的稀硫酸溶液完成实验,问需要98%的浓硫酸______ g
(3)用100g该浓度的稀硫酸恰好与6.5g锌完全反应,计算所得溶液中溶质质量分数_______ 。

| A.Ⅰ、Ⅱ两类反应均体现了氧气有可燃性 |
| B.Ⅰ、Ⅱ均发生了氧化反应 |
| C.Fe在Ⅰ、Ⅱ两类反应中的产物不同 |
| D.实验室用来制O2三种药品都含有氧元素 |
(3)用100g该浓度的稀硫酸恰好与6.5g锌完全反应,计算所得溶液中溶质质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将6克硝酸钾完全溶于54克水中,并将形成的溶液平均分成三份,计算:
(1)根据溶液的均一性,任取其中一份,其溶质的质量分数是__________ ;
(2)另取一份,使其溶质质量分数增大一倍,需加入硝酸钾__________ 克;再取一份,欲使其溶质质量分数减小一半,需加水__________ 克;
(3)现有溶质质量分数为10%的硝酸钾溶液200g,若配制成溶质质量分数为2%的硝酸钾溶液,需要加水的质量是多少?(写出计算过程)
(1)根据溶液的均一性,任取其中一份,其溶质的质量分数是
(2)另取一份,使其溶质质量分数增大一倍,需加入硝酸钾
(3)现有溶质质量分数为10%的硝酸钾溶液200g,若配制成溶质质量分数为2%的硝酸钾溶液,需要加水的质量是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】若使100g溶质质量分数为10%的氯化钠溶液变成20%的氯化钠溶液,
(1)下列可以达到目的方法是(选填序号)_________ .
A加水 B加溶质 C.蒸发溶剂 D倒出一些原溶液 E倒入一些原溶液
F加入一定量5%的氯化钠溶液 G加入一定量25%的氯化钠溶液
(2)请在你选的方法中选择一项,计算出加入或减少物质的质量(写出计算过程).
(1)下列可以达到目的方法是(选填序号)
A加水 B加溶质 C.蒸发溶剂 D倒出一些原溶液 E倒入一些原溶液
F加入一定量5%的氯化钠溶液 G加入一定量25%的氯化钠溶液
(2)请在你选的方法中选择一项,计算出加入或减少物质的质量(写出计算过程).
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将40 g氢氧化钠溶液逐滴加入到20 g溶质质量分数为0. 365%的稀盐酸中,边滴加边搅拌。随着氢氧化钠溶液的滴加,溶液的pH变化如左图所示,溶液的温度变化如右图所示。试回答:

(1)上右图从A到B过程中,溶液的pH逐渐________ (填“增大”或“减小”)。
(2)上右图从B到C过程中,溶液温度降低的原因是_____________ 。
(3)C点对应的溶液中含有的微粒有____________ (用符号表示)。
(4)计算氢氧化钠溶液的溶质质量分数。(写出计算过程)_________________________

(1)上右图从A到B过程中,溶液的pH逐渐
(2)上右图从B到C过程中,溶液温度降低的原因是
(3)C点对应的溶液中含有的微粒有
(4)计算氢氧化钠溶液的溶质质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】将19.45克碳酸钠和氯化钠的固体混合物放置于烧杯(重50克)中,加入一定量的水,固体全部溶解,然后向烧杯中滴加一定溶质质量分数的稀盐酸,实验测得烧杯及杯中物质的总质量与加入稀盐酸的质量关系如图所示.计算:

(1)所加稀盐酸的溶质质量分数
(2)恰好完全反应时所得溶液的溶质质量分数.

(1)所加稀盐酸的溶质质量分数
(2)恰好完全反应时所得溶液的溶质质量分数.
您最近一年使用:0次




