科学施肥时农业增产的重要手段。(NH4)2SO4是常见的氮肥,对提高农作物产量有重要作用。为测定该化肥样品中氮元素的质量分数,实验探究小组的同学设计了以下方案进行实验(样品中杂质可溶,且不参与反应)。
方案1:甲同学称取13.60g样品,与足量的浓NaOH溶液混合加热,充分反应后,将获得的气体直接用浓硫酸吸收,浓硫酸增重3.91g。
方案2:乙同学另取等质量的样品溶于水,向水中加入足量的BaCl2溶液,充分反应后将沉淀过滤、洗涤、干燥,得白色固体23.3g。
你认为上述不合理的是哪个方案,并简述理由;
选用合理方案来计算 (NH4)2SO4样品中氮元素的质量分数。(写出计算过程,结果精确至0.1%)
方案1:甲同学称取13.60g样品,与足量的浓NaOH溶液混合加热,充分反应后,将获得的气体直接用浓硫酸吸收,浓硫酸增重3.91g。
方案2:乙同学另取等质量的样品溶于水,向水中加入足量的BaCl2溶液,充分反应后将沉淀过滤、洗涤、干燥,得白色固体23.3g。
你认为上述不合理的是哪个方案,并简述理由;
选用合理方案来计算 (NH4)2SO4样品中氮元素的质量分数。(写出计算过程,结果精确至0.1%)
更新时间:2017-04-25 22:25:15
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】汽车工业的迅速发展,给人们的生活带来了很大的方便。因此,汽车的安全性和汽车尾气的排放成为人们关注的问题,根据以下内容回答:
(1)研究证明,汽车尾气系统中,可以安装催化转化器,将尾气中的CO、NO在催化剂的作用下,转化成CO2和N2,以减少尾气对大气的污染。请写出该反应的化学方程式______,并根据方程式计算反应中CO、NO、CO2、N2的最简质量比______。
(2)为增加驾乘人员的安全,驾驶室中设计了安全气囊。当安全气囊受到强烈震动时,气囊中的叠氮化钠(NaN3)会发生分解,迅速产生氮气和固体金属钠,此时,气囊的体积迅速膨胀,以达到保护驾乘人员安全的目的。试计算,在通常状况下,要产生60L氮气,需要分解多少克叠氮化钠?(已知:在通常状况下,氮气的密度约为1.25g/L)
(1)研究证明,汽车尾气系统中,可以安装催化转化器,将尾气中的CO、NO在催化剂的作用下,转化成CO2和N2,以减少尾气对大气的污染。请写出该反应的化学方程式______,并根据方程式计算反应中CO、NO、CO2、N2的最简质量比______。
(2)为增加驾乘人员的安全,驾驶室中设计了安全气囊。当安全气囊受到强烈震动时,气囊中的叠氮化钠(NaN3)会发生分解,迅速产生氮气和固体金属钠,此时,气囊的体积迅速膨胀,以达到保护驾乘人员安全的目的。试计算,在通常状况下,要产生60L氮气,需要分解多少克叠氮化钠?(已知:在通常状况下,氮气的密度约为1.25g/L)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某物质4.6g在氧气中恰好完全燃烧,生成8.8g二氧化碳和5.4g水,则参与反应的氧气的质量为______ g,该物质的化学式为______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某研究性学习小组到超市买了一包碱面,包装袋上标明主要成分是碳酸钠,还含有少量的氯化钠。该兴趣小组为研究其成分,称取样品25.0g,将其配制成溶液,再向其中逐滴加入足量的溶质质量分数为14.6%的稀盐酸,反应生成二氧化碳的质量与所加入的稀盐酸质量关系如图。试回答下列问题:
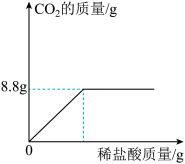
(1)样品充分反应后生成CO2的质量为_____ g
(2)原固体中Na2CO3的质量分数是多少?___________ (请写出计算过程)
(3)样品中碳酸钠与盐酸恰好完全反应时,消耗的稀盐酸的质量是_____________ g
【交流反思】研究性学习小组的甲同学认为,要求出碳酸钠的质量,还可以使用与盐酸所属类别不同的其他物质,如________ 、 _______ (填一种具体物质的化学式及该物质所属的类别)的溶液与样品反应,测定相关物质的质量,进行有关计算即可。

(1)样品充分反应后生成CO2的质量为
(2)原固体中Na2CO3的质量分数是多少?
(3)样品中碳酸钠与盐酸恰好完全反应时,消耗的稀盐酸的质量是
【交流反思】研究性学习小组的甲同学认为,要求出碳酸钠的质量,还可以使用与盐酸所属类别不同的其他物质,如
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】如图是某省生产的某加钙食盐包装标签上的部分文字,请仔细阅读后回答问题:

 包装标签上的钙含量是指________(单质/碳酸钙/钙元素)
包装标签上的钙含量是指________(单质/碳酸钙/钙元素)
 为了测定此盐中的钙元素含量,取
为了测定此盐中的钙元素含量,取 这种盐溶于水,加入足量的盐酸,生成
这种盐溶于水,加入足量的盐酸,生成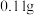 二氧化碳,计算此加钙食盐中钙元素的质量分数.________
二氧化碳,计算此加钙食盐中钙元素的质量分数.________

 包装标签上的钙含量是指________(单质/碳酸钙/钙元素)
包装标签上的钙含量是指________(单质/碳酸钙/钙元素) 为了测定此盐中的钙元素含量,取
为了测定此盐中的钙元素含量,取 这种盐溶于水,加入足量的盐酸,生成
这种盐溶于水,加入足量的盐酸,生成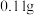 二氧化碳,计算此加钙食盐中钙元素的质量分数.________
二氧化碳,计算此加钙食盐中钙元素的质量分数.________
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱。现有含3.2t硫酸铜的工业废液,加入铁粉回收铜,反应的化学方程式为 。请计算:
。请计算:
(1)硫酸铜中铜元素的质量分数;
(2)理论上与硫酸铜反应消耗铁粉的质量。
 。请计算:
。请计算:(1)硫酸铜中铜元素的质量分数;
(2)理论上与硫酸铜反应消耗铁粉的质量。
您最近一年使用:0次



