2017届山东省济宁市任城区九年级下学期第一次模拟考试化学试卷
山东
九年级
一模
2017-05-04
276次
整体难度:
适中
考查范围:
物质的化学变化、物质构成的奥秘、身边的化学物质、化学与社会发展、化学实验
一、选择题 添加题型下试题
| A.用小苏打发酵面粉 | B.家用净水器中高分子膜净化水 |
| C.医用双氧水杀菌消毒 | D.烹饪鱼时加入料酒去除腥味 |
【知识点】 化学变化与物理变化判断解读
| A.HCl、H2SO4、NaHSO4都属于酸 |
| B.CH4 、C2H5OH、CH3COOH都属于有机物 |
| C.铁、碘、锌元素都属于人体必需微量元素 |
| D.KNO3、K2HPO4、NH4H2PO4都属于复合肥料 |
| A | 一架蔷薇满园香 | 分子由原子构成 |
| B | 冰水共存物属于纯净物 | 冰和水都由水分子构成 |
| C | 搅拌能加快蔗糖在水中的溶解 | 搅拌使蔗糖分子在水中溶解更多 |
| D | 众人拾柴火焰高 | 可燃物越多,物质的着火点越高,燃烧越剧烈 |
| A.A | B.B | C.C | D.D |
| A.正常雨水也显弱酸性的主要原因 H2O+CO2=H2CO3 |
| B.医疗上用氢氧化铝中和过多胃酸 2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O |
| C.氯化钠溶液中加入氯化钾 NaCl+KNO3= KCl+NaNO3 |
| D.证明铁的活动性比铜强 2Fe+3CuCl2=2FeCl3+3Cu |
| A.H2S、H2O、H2SO4、H2四种物质中都含有氢分子 |
| B.SO32-和SO42-中硫元素的化合价相同 |
| C.Na+、Mg2+、Al3+ 原子核内质子数均为10 |
D.由Na  和 K 和 K 得出,钠元素和钾元素的化学性质相似 得出,钠元素和钾元素的化学性质相似 |
实验操作 | 现象 | 结论 | |
A | 向集满CO2的软塑料瓶中加入约1/3体积滴有石蕊试液的水,旋紧瓶塞,振荡 | 塑料瓶变瘪, 溶液变红 | CO2能与石蕊反应 |
B | 向未知溶液中加入盐酸,再滴入氯化钡溶液 | 有白色沉淀生成 | 溶液中含有SO42- |
C | 向食醋中加入氢氧化钠溶液 | 无明显现象 | 二者之间不发生反应 |
D | 往久置空气中的氢氧化钠溶液中滴加足量稀盐酸 | 无气泡生成 | 氢氧化钠溶液未变质 |
| A.A | B.B | C.C | D.D |

| A.约在64℃时,KCl和Na2SO4的溶解度相等 |
| B.在40℃时,40gKCl固体溶于60g水得到40%的KCl溶液 |
| C.在室温至100℃区间,随温度升高,Na2SO4的溶解度先增大后减小,醋酸钙则相反 |
| D.分离含少量KCl的溶液,采用先蒸发浓缩,后降温结晶的方法 |
【知识点】 固体溶解度曲线的应用解读
A | 氯酸钾中混有氯化钾 | 加热至不再产生气体为止 |
B | 氢氧化钠溶液中混有氢氧化钙 | 加入过量的碳酸钠溶液、过滤 |
C | 二氧化碳气体中含有少量水蒸气 | 通过盛有浓硫酸的干燥剂 |
D | 硝酸钾溶液中含有少量硝酸钡 | 加入适量的硝酸钠溶液、过滤 |
| A.A | B.B | C.C | D.D |

| A.t1时,产生气体的质量:X>Y |
| B.t2时,消耗金属的质量:X>Y |
| C.t3时,消耗金属的质量:X=Y |
| D.t3时,消耗盐酸的质量:X=Y |
【知识点】 金属与酸反应的图像解读 金属活动顺序图像分析
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A。
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得到无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为
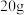 。
。③在
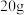 白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出。
白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出。④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀。
由上述实验得出的下列判断,正确的是( )
| A.白色粉末中不含碳酸钙、硫酸钠、硫酸铜 | B.无色溶液B中一定含有一种溶质 |
| C.白色粉末中一定含有氯化钠 | D.步骤③生成的气体质量可能是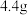 |
二、填空与简答 添加题型下试题
(1)硝酸钠溶液中的离子
(2)溶于水后显碱性的气体
(3)同种元素组成的两种不同化合物
(4)有沉淀生成的中和反应
(1)活性炭用于防毒面具
(2)氧气用于炼钢、焊接、切割金属
(3)生石灰用于干燥剂
(4)铝制品不易锈蚀
(1)在ClO2的制备方法中,有下列两种常用制备方法
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑+2H2O
用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是
(2)我国最新研制出制备二氧化氯的新方法,其微观示意图如下:
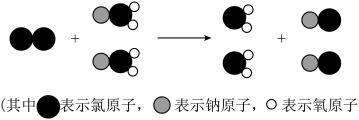
写出该反应的化学方程式
(3)消毒时,ClO2能将污水中的Fe2+、Mn2+、CN-等有明显的去除效果。某工厂污水中含有CN_,ClO2能将污水中的CN-氧化为两种无毒气体,你认为这两种气体是
【知识点】 质量守恒定律的应用 化学方程式的书写解读 微粒图像的分析及应用解读
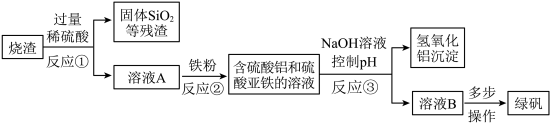
(1)反应①和反应③都要进行的操作是
(2)反应②中发生置换反应的化学方程式为
(3)用NaOH溶液控制pH的目的是
(4) 溶液B中含有的溶质一定有硫酸亚铁和
雨伞 | 尼龙绸伞布、不锈钢伞骨 |
风筝 | 竹子、棉线、尼龙线、宣纸 |
陶罐 | 高岭土、白色矿石颜料 |
笔筒 | 易拉罐、塑料瓶 |
塑料制品在生活中常被用作保鲜膜和方便袋,虽然方便了生活,还大量使用后随意丢弃会造成白色污染。为保护环境,减少“白色污染”,请结合生活提出一条合理化建议
三、科学探究题 添加题型下试题
【查阅资料】过氧化钠(Na2O2)是一种淡黄色固体,能与 CO2、H2O发生反应:
2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O===4NaOH+O2↑。

请回答下列问题:
(1)装置 A 中发生反应的化学方程式为
利用装置 A 制取 CO2 的优点是
(2)装置B的作用是吸收CO2中混有的HCl,发生反应的化学方程式 为
(3)装置D的作用是
(4)装置E中该气体还可用下图装置中

(5)为探究反应后装置 C 硬质玻璃管中固体的成分,该小组同学进行了如图实验:

根据判断,反应后装置C硬质玻璃管中固体为
Ⅱ.冬季取暖人们常用到暖宝宝(如图),其热量来源于铁的缓慢氧化。化学小组的同学突发奇想,想利用暖宝宝测定空气中氧气的含量。

【查阅资料】
(1)暖宝宝的主要成分铁粉、木炭、食盐。
(2)暖宝宝反应的主要原理是铁粉与氧气、水共同作用生成氢氧化铁,反应的化学方程式为
【设计实验】化学小组的同学设计了如图1所示装置。

【实验步骤】①检查装置气密性
②向250mL集气瓶中加入20mL水
③读取温度计示数为18℃,撕掉暖宝宝上的贴纸,塞紧橡胶塞。
④观察温度计示数的变化
⑤待温度计示数为18℃时,打开止水夹。
请回答下列问题:
(1)检查装置气密性的方法是
(2)小组同学的设计中,集气瓶内水的作用是
(3)实验结果如图2所示,根据图示数据计算得出氧气的体积分数约为
【实验反思】你认为小组同学实验产生误差的可能原因有
四、计算题 添加题型下试题
(1)皂甙的化学式量为_______________;
(2)皂甙中氢元素与氧元素的质量之比是 ____________。
方案1:甲同学称取13.60g样品,与足量的浓NaOH溶液混合加热,充分反应后,将获得的气体直接用浓硫酸吸收,浓硫酸增重3.91g。
方案2:乙同学另取等质量的样品溶于水,向水中加入足量的BaCl2溶液,充分反应后将沉淀过滤、洗涤、干燥,得白色固体23.3g。
你认为上述不合理的是哪个方案,并简述理由;
选用合理方案来计算 (NH4)2SO4样品中氮元素的质量分数。(写出计算过程,结果精确至0.1%)
试卷分析
试卷题型(共 18题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.94 | 化学变化与物理变化判断 | 单选题 |
| 2 | 0.85 | 有机物定义和常见的有机物 酸的定义 常见化肥的种类及性质 人体内的微量元素——碘、铁元素 | 单选题 |
| 3 | 0.85 | 微粒的观点解释现象 分子、原子的区别与联系 影响溶解速率的因素 着火点 | 单选题 |
| 4 | 0.85 | 化学方程式的书写 金属活动性强弱的探究 中和反应的实际应用 | 单选题 |
| 5 | 0.65 | 物质的微粒性 核外电子排布规律的理解及应用 化学式、分子式及涵义 化合价代数和的计算与应用 | 单选题 |
| 6 | 0.65 | 二氧化碳与水的反应及实验 强碱露置在空气中的变质 无明显现象的中和反应的判断 盐类参与的反应 | 单选题 |
| 7 | 0.85 | 固体溶解度曲线的应用 | 单选题 |
| 8 | 0.4 | 氯酸钾制取氧气 浓硫酸做干燥剂 碱的通性 盐类参与的反应 | 单选题 |
| 9 | 0.4 | 金属与酸反应的图像 金属活动顺序图像分析 | 单选题 |
| 10 | 0.4 | 盐类参与的反应 碳酸根离子的验证 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | 单选题 |
| 二、填空与简答 | |||
| 11 | 0.85 | 化学方程式的书写 离子符号的含义及书写 化学式书写及读法 中和反应的概念及微观本质 | 填空题 |
| 12 | 0.94 | 结构、性质与用途的关系 金属与氧气反应 生石灰的性质及用途 | 填空题 |
| 13 | 0.85 | 质量守恒定律的应用 化学方程式的书写 微粒图像的分析及应用 | 填空题 |
| 14 | 0.4 | 置换反应 碱的通性 过滤 | 填空题 |
| 15 | 0.94 | 金属材料和非金属材料 有机材料对环境的影响及应对措施 | 填空题 |
| 三、科学探究题 | |||
| 16 | 0.4 | 化学方程式的书写 测定空气中氧气的含量实验的过程 制取二氧化碳的原理 气密性检测 | |
| 四、计算题 | |||
| 17 | 0.65 | 根据化学式计算相对分子质量 根据化学式计算元素质量比 | |
| 18 | 0.65 | 根据化学方程式计算质量比 根据化学式计算元素质量分数 | |



