2020年山东省济南市中考模拟化学试题2
山东
九年级
模拟预测
2020-06-24
411次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、物质构成的奥秘、化学实验、化学与社会发展
2020年山东省济南市中考模拟化学试题2
山东
九年级
模拟预测
2020-06-24
411次
整体难度:
适中
考查范围:
物质的化学变化、身边的化学物质、物质构成的奥秘、化学实验、化学与社会发展
一、选择题 添加题型下试题
选择题-单选题
|
较难(0.4)
1. 某化学小组在完成实验室制取CO2实验后,过滤得100g混合溶液,已知其中H+和Ca2+的个数比为2:1,为了弄清所得溶液的组成,向溶液中加入20g碳酸钠样品(所含杂质不溶于水,也不与其他物质反应),恰好完全反应后,过滤得到14.4g固体,求混合液中氯化氢和氯化钙的质量分数为
| A.7.3% 11.1% | B.3.65% 20% | C.3.65% 5.55% | D.7.3% 10% |
您最近一年使用:0次
选择题-单选题
|
容易(0.94)
2. 某同学在做加热氯酸钾抽取氧气的实验中,错把高锰酸钾当成二氧化锰加入氯酸钾中,下列说法正确的是
| A.高锰酸钾是氯酸钾分解的催化剂 |
| B.反应速率加快,生成氧气的量增加 |
| C.反应速率加快,生成氧气的量不变 |
| D.很难反应,几乎收集不到氧气 |
【知识点】 催化剂的概念、性质与用途解读 氯酸钾制取氧气解读
您最近一年使用:0次
2019-10-30更新
|
519次组卷
|
12卷引用:广西北部湾经济区2019-2020学年九年级上学期第一次联考化学试题
广西北部湾经济区2019-2020学年九年级上学期第一次联考化学试题2020年福建省中考模拟化学试题2020年山东省济南市中考模拟化学试题12020年山东省济南市中考模拟化学试题22020年山东省潍坊市青州市中考模拟化学试题(已下线)《单元测试定心卷》第二单元 身边的化学物质(能力提升)-2020-2021学年九年级化学上册单元测试定心卷(沪教版)(已下线)《课时同步练》4.3.2 高锰酸钾制氧气-2020-2021学年九年级化学上册课时同步练(鲁教版)2020年贵州省贵阳市中考一模化学试题(已下线)【万唯原创】2021年安徽省中考化学试题研究卷练习册九年级第2单元河南省安阳市林州市太行国际学校2021-2022学年九年级上学期入学调研化学试题湖北省十堰市郧阳区2021-2022学年九年级上学期期中化学试题山西省忻州市静乐县2021-2022学年九年级上学期期末化学试题
选择题-单选题
|
较难(0.4)
3. 工业上,高温煅烧石灰石可制取生石灰(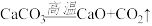 )。现有100g CaCO3样品,高温锻烧一段时间后,剩余固体的质量为67g。下列推断不符合客观事实的是
)。现有100g CaCO3样品,高温锻烧一段时间后,剩余固体的质量为67g。下列推断不符合客观事实的是
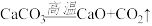 )。现有100g CaCO3样品,高温锻烧一段时间后,剩余固体的质量为67g。下列推断不符合客观事实的是
)。现有100g CaCO3样品,高温锻烧一段时间后,剩余固体的质量为67g。下列推断不符合客观事实的是| A.反应后固体质量减少的原因是逸出了二氧化碳气体 |
| B.生成物中CaO的质量是42g |
| C.剩余固体中钙元素的质量分数大于40% |
| D.剩余固体中碳元素与氧元素的质量之比大于1:4 |
您最近一年使用:0次
2020-01-11更新
|
218次组卷
|
4卷引用:江苏省苏州市吴中、吴江、相城区2019-2020学年九年级上学期期末化学试题
选择题-单选题
|
较难(0.4)
名校
4. 现有硫酸钾和碳酸钾的混合物 12.6g,向其中加入一定量的硝酸钡溶液至恰好不再产生沉淀。将沉淀过滤、洗涤、干燥后称量其质量为 24.4g,并得到不饱和溶液 188.2g。则加入硝酸钡溶液的溶质质量分数为( )
| A.5.9% | B.11.8% | C.17.6% | D.26.1% |
【知识点】 溶质质量分数结合化学方程式的计算解读
您最近一年使用:0次
2020-05-11更新
|
193次组卷
|
4卷引用:黑龙江省哈尔滨市第六十九中学 2019-2020 学年九年级下学期5月线上学习质量评估化学试题
选择题-单选题
|
适中(0.65)
5. 鉴别下列各组物质,所用三组试剂均正确的是( )
| 待鉴别的物质 | 鉴别试剂1 | 鉴别试剂2 | 鉴别试剂3 | |
| A | 稀盐酸和稀硫酸 | 氯化钡溶液 | 碳酸钠溶液 | 氧化铜 |
| B | 氯化铵和氯化钙 | 硝酸银溶液 | 熟石灰 | 碳酸钠溶液 |
| C | 硝酸铵固体和氢氧化钠固体 | 熟石灰 | 水 | 硝酸铜溶液 |
| D | 氧气、二氧化碳、氢气 | 燃着的木条 | 澄清石灰水 | 水 |
| A.A | B.B | C.C | D.D |
【知识点】 铵根离子的验证解读 物质鉴别——选用试剂鉴别解读
您最近一年使用:0次
2019-03-22更新
|
269次组卷
|
5卷引用:【区级联考】广西柳州市柳南区2018届九年级下学期二模化学试题
选择题-单选题
|
适中(0.65)
6. 能在pH为5的溶液中大量共存,且溶液为无色透明的一组物质是
| A.ZnSO4、FeCl2、NaCl | B.CaCl2、Na2SO4、NaOH |
| C.BaCl2、KNO3、AgNO3 | D.K2SO4、NaNO3、NH4Cl |
【知识点】 溶液中物质是否共存相关判断解读
您最近一年使用:0次
2020-01-15更新
|
177次组卷
|
4卷引用:2019年河南省驻马店市新蔡县中考一模化学试题
选择题-单选题
|
较易(0.85)
7. 下列离子能在pH=12的水溶液中大量共存的是( )
A. 、 、 、K+、H+ 、K+、H+  | B.Na+、Cl-、OH-、Al3+ |
C.Cl-、 、K+、Na+ 、K+、Na+  | D.Ag+、Cl-、 、K+ 、K+ |
【知识点】 复分解反应的实质与应用解读 溶液中物质是否共存相关判断解读
您最近一年使用:0次
选择题-单选题
|
适中(0.65)
8. 如图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述正确的是


| A.t1℃时,乙物质的溶解度大于丙 |
| B.t2℃时,20g丙能溶解于50g水中形成70g溶液 |
| C.若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法 |
| D.将t3℃时甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为乙>甲=丙 |
您最近一年使用:0次
2020-04-09更新
|
228次组卷
|
10卷引用:2019年6月山西省中考适应性训练化学试题
选择题-单选题
|
较难(0.4)
9. 有一包白色粉末,可能由氯化钠、硫酸钠、硫酸铜、碳酸钠、碳酸钙中的一种或几种组成,为确定其组成,进行如下实验:
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A。
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得到无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为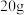 。
。
③在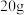 白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出。
白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出。
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀。
由上述实验得出的下列判断,正确的是( )
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A。
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得到无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为
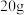 。
。③在
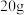 白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出。
白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出。④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀。
由上述实验得出的下列判断,正确的是( )
| A.白色粉末中不含碳酸钙、硫酸钠、硫酸铜 | B.无色溶液B中一定含有一种溶质 |
| C.白色粉末中一定含有氯化钠 | D.步骤③生成的气体质量可能是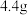 |
您最近一年使用:0次
2019-09-13更新
|
300次组卷
|
10卷引用:2015届天津市和平区九年级下学期第一次质量调查化学试卷
选择题-单选题
|
适中(0.65)
名校
10. 温度不变,对100 mL氯化钠饱和溶液进行如图所示实验。下列结论不正确的是
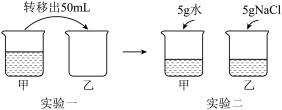

| A.实验一后,甲和乙中溶质质量分数相等 | B.实验二后,乙溶液溶质质量分数增大 |
| C.实验二后,甲溶液变为不饱和溶液 | D.实验二后,甲和乙溶液中溶质质量相等 |
【知识点】 溶液的基本特征解读 饱和溶液和不饱和溶液的转换解读 溶质的质量分数
您最近一年使用:0次
2019-05-04更新
|
879次组卷
|
19卷引用:北京市石景山区2019年九年级一模化学试题
北京市石景山区2019年九年级一模化学试题江苏省沭阳县修远中学2019届九年级下学期5月月考化学试题(已下线)北京市海淀区2019-2020学年九年级上学期期末化学试题北京市通州区2019-2020学年九年级上学期期末化学试题北京市丰台区北京十八中2019-2020学年九年级下学期4月月考化学试题上海市青浦区2019-2020学年九年级下学期期中(二模)化学试题2020年北京市密云区中考一模化学试题(已下线)2020年北京9区中考一模化学试题分类汇编-选择题2020年山东省济南市中考模拟化学试题22020年北京市门头沟区中考二模化学试题(已下线)北京市2020年一、二模汇编-溶液基础知识(已下线)上海市2020年一、二模汇编-溶液基础知识山东省菏泽市牡丹区2020-2021学年九年级上学期期末化学试题2021年湖南省永州市江华县中考一模化学试题2021年北京市海淀区中国人民大学附属中学第二分校中考零模化学试题山东省威海乳山市(五四制)2021-2022学年九年级上学期期末化学试题(已下线)6.2 溶液的组成 (基础过关)-2022-2023学年九年级化学下册课后培优分级练(沪教版)山东省菏泽市牡丹区第十一中学2022-2023学年九年级下学期3月月考化学试题2023-2024九化课后作业与单元测试 鲁教版 第三单元 单元测试B卷
二、填空与简答 添加题型下试题
填空与简答-推断题
|
适中(0.65)
名校
解题方法
11. 我国化工专家侯德榜创立了“侯氏制碱法”,促进了世界制碱技术的发展。其流程简图和部分物质的溶解度曲线如下:

已知:①母液中有一种铵态氮肥
②
请回答下列问题:
(1)操作a的名称是_____ 。
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是_____ ,从图2中还能获得的一条信息是_____ 。
(3)图1中得到的母液中一定含有的阳离子是_____ (填离子符号), 流程中可以循环使用的物质是_____ 。
(4)从图2可以看出温度高于60°C,NaHCO3的溶解度曲线“消失”了,其原因可能是_____ 。

已知:①母液中有一种铵态氮肥
②

请回答下列问题:
(1)操作a的名称是
(2)结合图2分析,图1反应1中NaHCO3作为晶体析出的原因是
(3)图1中得到的母液中一定含有的阳离子是
(4)从图2可以看出温度高于60°C,NaHCO3的溶解度曲线“消失”了,其原因可能是
您最近一年使用:0次
2020-02-26更新
|
734次组卷
|
4卷引用:2019年6月山西省太原市迎泽区太原第五中学校中考模拟化学试题
三、实验题 添加题型下试题
实验题
|
适中(0.65)
12. 如图是小明同学配制100g 10% NaCl溶液的实验操作示意图。

(1)该实验正确的操作顺序是_____ (填序号)。
(2)认真观察 指出图中错误的操作步骤_____ (填序号)。
(3)配制该溶液需要NaCl固体_____ g,需要水 _____ mL(ρ水=1g/mL),量取所需要的水应选择 _____ (选填“10mL”、“50mL”或“100mL”)量筒。
(4)下列因素会使所配溶液溶质质量分数偏小的是_____ (填序号)①药品和砝码放错了盘 ②量取水时仰视量筒刻度 ③所用烧杯内事先残留少量蒸馏水 ④将所配溶液转入试剂瓶时,不慎洒到外面少量。⑤使用粗盐代替氯化钠进行配制。

(1)该实验正确的操作顺序是
(2)认真观察 指出图中错误的操作步骤
(3)配制该溶液需要NaCl固体
(4)下列因素会使所配溶液溶质质量分数偏小的是
您最近一年使用:0次
2019-04-04更新
|
119次组卷
|
3卷引用:山东省德州市乐陵市花园中学2019届九年级上学期第二次月考化学试题
四、填空与简答 添加题型下试题
填空与简答-推断题
|
较难(0.4)
13. A~I是初中化学常见的物质,它们之间的相互关系如图所示(“→”指向生成物),其中B是铁锈的主要成分,A、C常温下是气体,H和I中含有一种相同元素,H不溶于稀硝酸。

请回答下面问题:
(1)物质I的化学式是____ ;物质E的化学式是____ 。
(2)反应②的基本反应类型是_____ 。
(3)物质F属于____ (填“酸”、“碱”、“盐”或“氧化物”)。
(4)反应③的化学方程式为____ 。

请回答下面问题:
(1)物质I的化学式是
(2)反应②的基本反应类型是
(3)物质F属于
(4)反应③的化学方程式为
您最近一年使用:0次
2019-10-25更新
|
106次组卷
|
4卷引用:2017年内蒙古巴彦淖尔市乌拉特前旗第三中学中考四模化学试题
五、科学探究题 添加题型下试题
科学探究题
|
适中(0.65)
14. 某班学生在老师指导下探究铁与水蒸气的反应,请帮助他完成下列实验报告。
(1)按图甲装好药品,连接装置(夹持仪器已略去)。其中A装置的作用是:_______

(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣。
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色;铁的三种氧化物都不与硫酸铜溶液反应。
【实验探究】
(1)按图甲装好药品,连接装置(夹持仪器已略去)。其中A装置的作用是:

(2)加热一段时间后,灰色铁粉逐渐变黑,吹泡器连续吹出气泡,且气泡向上飞起;用燃着的木条靠近气泡,能产生爆鸣。
(3)同学们讨论后认为:铁与水蒸气反应生成的固体是“铁的一种氧化物”,玻璃管内的黑色固体中还可能含有“过量的铁”。
【查阅资料】铁有三种氧化物(FeO、Fe2O3、Fe3O4),其中FeO接触到空气会立即由黑色变为红棕色;铁的三种氧化物都不与硫酸铜溶液反应。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| 倒出玻璃管中黑色固体,平铺于白纸上 | 黑色固体不变色 | 黑色固体中一定没 有 |
| 取上述黑色固体少许,装入试管,加入足量硫酸铜溶液 | 黑色固体中一定 含有 |
您最近一年使用:0次
2020-01-03更新
|
117次组卷
|
3卷引用:湖北省鄂州市梁子湖区2019-2020学年九年级上学期期末化学试题
六、实验题 添加题型下试题
实验题
|
适中(0.65)
15. 我国著名化学家侯德榜先生发明的侯氏制碱法,因原料利用率高,并能进行连续生产,从而享誉中外。某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下图所示一套实验装置。

实验室可供选用的药品有:浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化
铵、氯化钠。
(1)A、D 中最合适的试剂为:A_______ ,D _______ (填名称)。
(2)本实验在具体操作过程中,应先通______ 气体,再通 ______ 气体,原因是 _______ 。
(3)小红同学认为实验装置中存在某些不足,请指出其中的一处错误_________ 。
(4)在改进装置后,小丽同学进行了实验,实验所用的饱和氯化钠溶液中含溶质 58.5g,实验最后得到无水碳酸钠 26.0g,针对实验结果,该同学认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是___________ 。

实验室可供选用的药品有:浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化
铵、氯化钠。
(1)A、D 中最合适的试剂为:A
(2)本实验在具体操作过程中,应先通
(3)小红同学认为实验装置中存在某些不足,请指出其中的一处错误
(4)在改进装置后,小丽同学进行了实验,实验所用的饱和氯化钠溶液中含溶质 58.5g,实验最后得到无水碳酸钠 26.0g,针对实验结果,该同学认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是
您最近一年使用:0次
2019-06-01更新
|
132次组卷
|
3卷引用:山东省沂源县中庄中学2019届九年级下学期4月模拟化学试题
七、计算题 添加题型下试题
计算题
|
适中(0.65)
16. 称取BaCl2和NaCl的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如图所示。试回答下列问题:
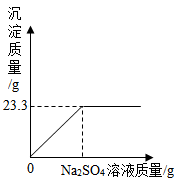
(1)Na2SO4和NaCl中均含有钠元素,钠元素位于元素周期表第_____周期。
(2)完全反应后生成BaSO4沉淀_____g。
(3)恰好完全反应时消耗Na2SO4溶液质量是_____g。
(4)恰好完全反应时所得溶液中溶质的质量分数是多少? _____(精确到0.1%)(写出计算过程)

(1)Na2SO4和NaCl中均含有钠元素,钠元素位于元素周期表第_____周期。
(2)完全反应后生成BaSO4沉淀_____g。
(3)恰好完全反应时消耗Na2SO4溶液质量是_____g。
(4)恰好完全反应时所得溶液中溶质的质量分数是多少? _____(精确到0.1%)(写出计算过程)
【知识点】 溶液和化学方程式的综合计算解读 盐类参与的反应解读
您最近一年使用:0次
2019-11-07更新
|
182次组卷
|
4卷引用:2017年四川省宜宾市叙州区宜宾市第八中学校中考二模化学试题
试卷分析
整体难度:适中
考查范围:物质的化学变化、身边的化学物质、物质构成的奥秘、化学实验、化学与社会发展
试卷题型(共 16题)
题型
数量
选择题
10
填空与简答
2
实验题
2
科学探究题
1
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、选择题 | |||
| 1 | 0.4 | 含杂质的化学方程式计算 溶质质量分数结合化学方程式的计算 盐类参与的反应 | 单选题 |
| 2 | 0.94 | 催化剂的概念、性质与用途 氯酸钾制取氧气 | 单选题 |
| 3 | 0.4 | 根据化学方程式计算质量比 计算混合物中物质或元素的质量分数 | 单选题 |
| 4 | 0.4 | 溶质质量分数结合化学方程式的计算 | 单选题 |
| 5 | 0.65 | 铵根离子的验证 物质鉴别——选用试剂鉴别 | 单选题 |
| 6 | 0.65 | 溶液中物质是否共存相关判断 | 单选题 |
| 7 | 0.85 | 复分解反应的实质与应用 溶液中物质是否共存相关判断 | 单选题 |
| 8 | 0.65 | 饱和溶液和不饱和溶液的转换 固体溶解度曲线的应用 图像分析溶质质量分数的变化 | 单选题 |
| 9 | 0.4 | 盐类参与的反应 碳酸根离子的验证 几种常见阴、阳离子的鉴别 设计实验探究物质的成分 | 单选题 |
| 10 | 0.65 | 溶液的基本特征 饱和溶液和不饱和溶液的转换 溶质的质量分数 | 单选题 |
| 二、填空与简答 | |||
| 11 | 0.65 | 晶体与非晶体 侯氏制碱法 过滤 | 推断题 |
| 13 | 0.4 | 物质推断的综合应用 各类物质间反应的总结 常见物质的颜色 | 推断题 |
| 三、实验题 | |||
| 12 | 0.65 | 配制一定质量分数溶液的仪器 固体配制一定质量分数溶液 | |
| 15 | 0.65 | 制取二氧化碳原理的拓展 碳酸氢钠、碳酸钠、碳酸钙 侯氏制碱法 | |
| 四、科学探究题 | |||
| 14 | 0.65 | 实验探究质量守恒定律 氢气的物理性质 设计实验探究物质的成分 | |
| 五、计算题 | |||
| 16 | 0.65 | 溶液和化学方程式的综合计算 盐类参与的反应 | |



