某化学兴趣小组在实验室用硫酸铜溶液和氯化钡溶液反应制取少量氯化铜溶液。他们的实验过程和相关数据如下(BaSO4不溶于水)。
第一步:称得烧杯的质量是100 g。
第二步:反应前称得烧杯、氯化钡溶液及硫酸铜溶液的总质量是346.6 g。
第三步:两者恰好完全反应后,过滤,称得烧杯及滤液的总质量是300 g。
请计算:
(1)反应后生成沉淀的质量是_______________。
(2)所得氯化铜溶液中溶质的质量分数为________(写出计算过程,精确到0.1%)。
第一步:称得烧杯的质量是100 g。
第二步:反应前称得烧杯、氯化钡溶液及硫酸铜溶液的总质量是346.6 g。
第三步:两者恰好完全反应后,过滤,称得烧杯及滤液的总质量是300 g。
请计算:
(1)反应后生成沉淀的质量是_______________。
(2)所得氯化铜溶液中溶质的质量分数为________(写出计算过程,精确到0.1%)。
2017·山东临沂·中考真题 查看更多[8]
2017年初中毕业升学考试(山东临沂卷)化学山东省菏泽市2018届九年级中考复习化学同步测试:第九单元 溶液2018年九年级化学人教版下册第十一单元测试卷2018年河南省中考化学同步测试试题:质量守恒定律的应用专项训练贵州省铜仁市思南县东华中学2017-2018学年九年级终端评估化学试题2018年贵州省铜仁市中考适应性模拟化学试题(已下线)主题 化学方程式及基本反应类型·课后特训3(已下线)【万唯原创】2018年河南省中考化学试题研究卷练习册九年级第五单元
更新时间:2017-09-14 03:20:56
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】实验室用含杂质的锌(也称粗锌)与盐酸反应制取氢气。取 该粗锌于烧杯中(杂质不溶于水,也不与盐酸反应),向其中加入
该粗锌于烧杯中(杂质不溶于水,也不与盐酸反应),向其中加入 稀盐酸,恰好完全反应后,烧杯内剩余物质质量为
稀盐酸,恰好完全反应后,烧杯内剩余物质质量为 。计算:
。计算:
(1)该粗锌中锌的质量分数。
(2)反应后所得溶液中溶质的质量分数(结果精确到 )。
)。
 该粗锌于烧杯中(杂质不溶于水,也不与盐酸反应),向其中加入
该粗锌于烧杯中(杂质不溶于水,也不与盐酸反应),向其中加入 稀盐酸,恰好完全反应后,烧杯内剩余物质质量为
稀盐酸,恰好完全反应后,烧杯内剩余物质质量为 。计算:
。计算:(1)该粗锌中锌的质量分数。
(2)反应后所得溶液中溶质的质量分数(结果精确到
 )。
)。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】实验室制取氧气时,某同学取氯酸钾和二氧化锰混合物15克,加热并进行测量记录,反应产生氧气的质量与时间的关系如图甲所示,请回答下列问题;
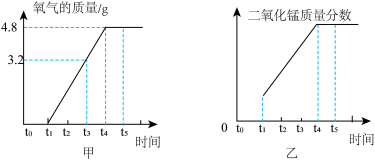
(1)t4-t5时段氧气质量不变的原因___________ 。
(2)t4时参加反应的氯酸钾的质量为多少?(写出计算过程)
(3)在反应过程中,二氧化锰在固体混合物中所占质量分数会随时间发生变化其部分变化曲线已在图乙中画出,请完善to-t1阶段的图像,并在纵坐标上标出t3时刻的数据。(结果精确到0.1%)

(1)t4-t5时段氧气质量不变的原因
(2)t4时参加反应的氯酸钾的质量为多少?(写出计算过程)
(3)在反应过程中,二氧化锰在固体混合物中所占质量分数会随时间发生变化其部分变化曲线已在图乙中画出,请完善to-t1阶段的图像,并在纵坐标上标出t3时刻的数据。(结果精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某补钙剂主要成分为碳酸钙(其他成分不溶于水也不与酸反应)。为了测定补钙剂中碳酸钙的质量分数,小明同学称取20g补钙剂放入烧杯中,再将80g稀盐酸分四次加入,充分反应后,测得的实验数据如表所示:
(1)第________ 次加入稀盐酸,充分反应后,烧杯中盐酸有剩余。
(2)表中m的值为________ 。
(3)补钙剂中碳酸钙的质量分数是多少?(写出计算过程)
| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
| 烧杯中剩余物质的质量/g | 38.2 | m | 75.6 | 95.6 |
(1)第
(2)表中m的值为
(3)补钙剂中碳酸钙的质量分数是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
名校
【推荐2】向10g大理石样品(杂质不溶于水,也不与盐酸反应)分两次加入一定溶质质量分数的稀盐酸,充分反应后烧杯内物质总质量变化如图所示。

请计算:
(1)该大理石样品中碳酸钙的质量分数是_____;
(2)计算所用稀盐酸的溶质质量分数;_____

请计算:
(1)该大理石样品中碳酸钙的质量分数是_____;
(2)计算所用稀盐酸的溶质质量分数;_____
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】现有氧化铜和铜的混合物,对其成分进行分析.取10g此样品,向其中分五次加入相同溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录于下表:(反应的化学方程式:CuO+H2SO4=CuSO4+H2O)
试回答下列问题:
(1)上述表格中m的值为______,10g样品中CuO的质量为______g.
(2)计算所加入稀硫酸中溶质的质量分数?______
(3)计算第三次加稀硫酸反应后所得溶液中溶质的质量分数?(精确到0.1%)_____
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入稀硫酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 充分反应后剩余固体质量/g | 8 | 6 | 4 | 3 | m |
试回答下列问题:
(1)上述表格中m的值为______,10g样品中CuO的质量为______g.
(2)计算所加入稀硫酸中溶质的质量分数?______
(3)计算第三次加稀硫酸反应后所得溶液中溶质的质量分数?(精确到0.1%)_____
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】取NaOH和NaCl的混合物3.63g放入烧杯中,加水溶解配制成70g溶液。向该溶液中滴加溶质质量分数为7.3%的稀盐酸,测得溶液pH与滴入稀盐酸的质量关系如图所示。当pH=7时,计算该溶液中溶质的质量分数。(写出计算过程)


您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】取碳酸钠和氯化钠的固体混合物13.6g,与质量为73g的稀盐酸恰好完全反应,产生二氧化碳气体的质量为4.4g。计算:
(1)固体混合物中碳酸钠的质量_____。
(2)该稀盐酸中溶质的质量分数_____。
(3)反应所得的溶液中溶质的质量分数_____(要计算过程,最后结果保留一位小数)。
(1)固体混合物中碳酸钠的质量_____。
(2)该稀盐酸中溶质的质量分数_____。
(3)反应所得的溶液中溶质的质量分数_____(要计算过程,最后结果保留一位小数)。
您最近一年使用:0次



