已知20 ℃时,在100 g水中达到饱和所能溶解的KNO3的最大量是31.6 g。向50 mL水(密度是1 g/mL)中溶解一定量KNO3固体如下。请回答:
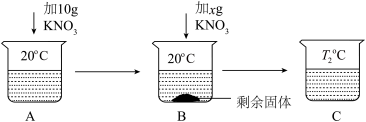
(1)A、B、C中一定是饱和溶液的是________ (填字母)。
(2)当x=________ g时,B中恰好没有固体剩余。
(3)硝酸钾晶体从溶液中析出常用______________ 的方法。

(1)A、B、C中一定是饱和溶液的是
(2)当x=
(3)硝酸钾晶体从溶液中析出常用
更新时间:2017-11-08 15:06:36
|
相似题推荐
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐1】如图是氯化钠和碳酸钠的溶解度曲线。据图回答:

(1)从海水中结晶食盐采用_______________ 方法。
(2)在严寒的冬天可以从盐碱湖中捞出纯碱(碳酸钠晶体)的原因。_____________

(1)从海水中结晶食盐采用
(2)在严寒的冬天可以从盐碱湖中捞出纯碱(碳酸钠晶体)的原因。
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】水是生命之源,我们应该了解水及溶液的相关知识。
(1)生活中可用______ 区分硬水和软水。
(2)净水时,利用活性炭的______ 性除 去水中的色素和异味。
(3)下面是氯化钠和硝酸钾在不同温度的溶解度,请回答:
若NaCl中混有少量的KNO3,提纯NaCl的方法是______ 。
(1)生活中可用
(2)净水时,利用活性炭的
(3)下面是氯化钠和硝酸钾在不同温度的溶解度,请回答:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
【推荐1】如图是甲、乙两种固体物质的溶解度曲线。

(1)t1℃时,甲、乙两种物质的溶解度的大小关系为__________ ;
(2) t2℃时,将16g甲物质放入50g水中,充分溶解后所得的溶液是__________ (填“饱和”或“不饱和”)溶液;
(3)欲使t2℃时乙物质的饱和溶液变为该温度下的不饱和溶液,可采取的方法是__________ (任填一种方法)。

(1)t1℃时,甲、乙两种物质的溶解度的大小关系为
(2) t2℃时,将16g甲物质放入50g水中,充分溶解后所得的溶液是
(3)欲使t2℃时乙物质的饱和溶液变为该温度下的不饱和溶液,可采取的方法是
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
解题方法
【推荐2】常温下,将某固态物质A溶于水,形成饱和溶液I(如下图),进行以下实验。回答下列问题:
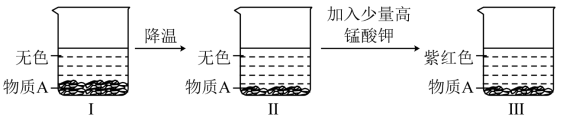
a.物质A的溶解度随温度的升高而_____________ (填“增大”或“减小”)。
b.往溶液Ⅱ中加入少量高锰酸钾完全溶解,溶液呈紫红色。据此现象说明在某物质的饱和溶液中_____ (“能”或“不能”)继续溶解其他物质。

a.物质A的溶解度随温度的升高而
b.往溶液Ⅱ中加入少量高锰酸钾完全溶解,溶液呈紫红色。据此现象说明在某物质的饱和溶液中
您最近一年使用:0次
【推荐3】点的含义及应用

如图所示,A、B、C三点代表的含义:A表示某物质15℃时的_______ (选填“饱和”或“不饱和”)溶液。B表示某物质20℃时的_______ (选填“饱和”或“不饱和”)溶液,此时该物质的溶解度为_______ ,该物质的溶解性为_______ 。20℃时,将0.6g该物质加入50g水中,得到的溶液为_______ (选填“饱和”或“不饱和”)溶液,质量为_______ g,所得溶液中溶质的质量分数为_______ 。C表示某物质30℃时的_______ (选填“饱和”或“不饱和”)溶液,且有晶体存在。

如图所示,A、B、C三点代表的含义:A表示某物质15℃时的
您最近一年使用:0次
填空与简答-填空题
|
较易
(0.85)
【推荐1】20℃时,将20g氯化钠放入50g水中,充分搅拌后所得溶液为_____ 溶液(填“饱和或不饱和”),该溶液的溶质量分数为_____ (20℃时氯化钠的溶解度为36g,结果保留一位小数)。
您最近一年使用:0次
【推荐2】完成下列问题
(1)下表列出了从探究实验中获取的部分数据,请你根据这些下表中的数据,在右边的坐标图中绘制A、B两物质的溶解度曲线(图中注明A、B)。

(2)该实验主要探究了温度对固体物质溶解度的影响在一定温度范围内,A物质的饱和溶液溶质质量分数大于B物质的饱和溶液溶质质量分数,该温度范围是___________ 。
(3)在20℃时,向100g水中加入40gA物质充分溶解后,形成的A物质溶液质量是___________ g。
(1)下表列出了从探究实验中获取的部分数据,请你根据这些下表中的数据,在右边的坐标图中绘制A、B两物质的溶解度曲线(图中注明A、B)。
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | A物质 | 30 | 35 | 41 | 50 |
| B物质 | 25 | 35 | 55 | 90 | |

(2)该实验主要探究了温度对固体物质溶解度的影响在一定温度范围内,A物质的饱和溶液溶质质量分数大于B物质的饱和溶液溶质质量分数,该温度范围是
(3)在20℃时,向100g水中加入40gA物质充分溶解后,形成的A物质溶液质量是
您最近一年使用:0次
填空与简答-简答题
|
较易
(0.85)
名校
【推荐3】某化学活动小组合作学习氢氧化钠和氢氧化钙的相关知识。如表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
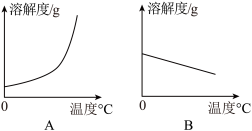
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是_____ (填“A”或“B”)。
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入适量氢氧化钙②升高温度③降低温度④加入水⑤蒸发水后再恢复到原温度⑥加入适量生石灰。
其中措施在原理上正确的是_____ (填字母)
A ②④⑥ B ③④ C ①②⑤⑥ D ①②⑤
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体。这时溶液的质量分数为_____
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____ (填“偏大”或“偏小”“不受影响”)。
(5)可鉴别氢氧化钠溶液和澄清石灰水的一个化学反应方程式为_____ 。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |

(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入适量氢氧化钙②升高温度③降低温度④加入水⑤蒸发水后再恢复到原温度⑥加入适量生石灰。
其中措施在原理上正确的是
A ②④⑥ B ③④ C ①②⑤⑥ D ①②⑤
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体。这时溶液的质量分数为
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH
(5)可鉴别氢氧化钠溶液和澄清石灰水的一个化学反应方程式为
您最近一年使用:0次




